MLR materiałów promocyjnych MLR – przegląd ogólny
Powodzenie wprowadzania produktów na rynek oraz skuteczne wejście na rynek w przypadku Produkty lecznicze wyroby medyczne od synergii między wysoko wykwalifikowanym Sprawy regulacyjne ds. promocji Sprawy regulacyjne solidnym procesem weryfikacji w zakresie spraw medycznych, prawnych i regulacyjnych (MLR). Synergia ta ma kluczowe znaczenie dla zapewnienia pełnej zgodności z przepisami dotyczącymi reklamy, etykietowania promocyjnego oraz rozpowszechniania informacji o charakterze niepromocyjnym w ramach działań medycznych.
Zapobieganie wprowadzającym w błąd twierdzeniom, dbanie o bezpieczeństwo pacjentów oraz zapewnienie etycznego rozpowszechniania informacji.
Zminimalizuj ryzyko związane z nieprzestrzeganiem przepisów, wezwaniami do usunięcia naruszeń lub karami oraz utratą reputacji.
Zapewnia zgodność oświadczeń dotyczących bezpieczeństwa, skuteczności lub działania wyrobu z faktami oraz ich poparcie dowodami naukowymi.
Spójność i zgodność z zatwierdzonymi informacjami na etykiecie produktu oraz instrukcją stosowania (IFU).
Przestrzeganie wytycznych ustanowionych przez organy regulacyjne oraz branżowych kodeksów etycznych obowiązujących w różnych krajach i regionach.
W firmie Freyr nasi eksperci ds. medycznych i regulacyjnych, dysponujący niezrównanym doświadczeniem klinicznym i biomedycznym, biegłością MLR oraz Sprawy regulacyjne dotyczących promocji w ponad 120 krajach, zapewniają całodobowe wsparcie, aby zagwarantować pełną zgodność z przepisami w zakresie promocji produktów markowych, reklam, kampanii informacyjnych dotyczących chorób oraz kampanii bez odniesień do konkretnych marek.
Usługi
- Potwierdzenie zgodności z wytycznymi obowiązującymi w poszczególnych krajach, ustanowionymi przez organy regulacyjne, takie jak FDA, EMA, EU MDR, MHRA, TGA, HSA, PMDA, ANVISA, Health Canada i inne.
- Potwierdzenie przestrzegania wytycznych obowiązujących w poszczególnych krajach dotyczących przepisów antyłapówkowych oraz branżowych kodeksów etycznych, takich jak FTC, PhRMA, EFPIA, ABPI, PAAB, TGA, Medicines New Zealand, ANVISA, ANAMED, IFPMA, AIFA, AEMPS, Mdeon i inne.
- Należy sprawdzić, czy twierdzenia i odniesienia są używane w sposób właściwy. Twierdzenia muszą być poparte odpowiednimi i właściwymi odniesieniami oraz dowodami naukowymi, a informacje dotyczące skuteczności lub bezpieczeństwa nie mogą być wyolbrzymione.
- Należy zadbać o wyważone przedstawienie zagrożeń i korzyści związanych z produktem, w tym wszelkich potencjalnych skutków ubocznych lub konsekwencji jego stosowania.
- Ocena języka, środków wyrazu wizualnego i innych elementów prezentacji informacji w celu zapewnienia jasności, dokładności oraz braku informacji wprowadzających odbiorców w błąd.
- Sprawdzanie zgodności elementów graficznych i tła z treścią w celu uniknięcia rozbieżności (np. upewnienie się, że zdjęcia dzieci nie są wykorzystywane w kontekstach, w których produkt nie jest przeznaczony dla tej grupy pacjentów).
- Poprawność nazw marek i znaków towarowych przedsiębiorstw, znaków usługowych oraz certyfikatów zgodności produktów, takich jak znak CE, UKCA mark, CCC i inne.
- Pełnienie funkcji ekspertów merytorycznych (SME) w kwestiach regulacyjnych podczas posiedzeń PRC.
- Wytyczne dotyczące wniosków HA, np. OPDP/APLP 2253 lub weryfikacja materiałów promocyjnych przez HA.
- Oznakowanie reklamowe i promocyjne; dokumenty składane do organów ds. zdrowia, takie jakForm 2253 APLB Form 2253 US FDA formacie papierowym orazFDA formacie eCTD.
Nasz zespół cechuje się dużą innowacyjnością i potrafi tworzyć treści na każdą platformę lub kanał, dlatego nasza oferta i doświadczenie nie ograniczają się do wyżej wymienionych obszarów – potrafimy znacznie więcej!
- Należy przeanalizować treści dotyczące leku, w tym wskazania, dawkowanie, instrukcje stosowania oraz mechanizm działania, w celu zapewnienia ich adekwatności i poprawności zgodnie z zatwierdzonymi materiałami informacyjnymi o produkcie, informacjami dotyczącymi przepisywania leku (PI), SmPC, ulotkami informacyjnymi dla pacjentów (PIL) oraz instrukcjami stosowania (IFU), a także popartymi odpowiednimi dowodami klinicznymi i naukowymi.
- Oceń zgodność materiałów promocyjnych z aktualnymi wytycznymi leczenia i standardami opieki w ramach określonego obszaru terapeutycznego
- Dostosowywanie punktów kontrolnych przeglądu do obszarów terapeutycznych, z uwzględnieniem wytycznych lub przepisów dotyczących działań promocyjnych, takich jak onkologia czy choroby rzadkie
- Zapewnienie "uczciwej równowagi" między przedstawieniem ryzyka a korzyści w materiałach promocyjnych, dokładnie odzwierciedlającej potencjalne wady obok zalet.
- Badania kliniczne oraz inne rzetelne i wiarygodne dane naukowe stanowią wystarczające uzasadnienie dla tych twierdzeń.
- Należy upewnić się, że twierdzenia dotyczące porównania z innymi produktami są poparte wiarygodnymi i rzetelnymi danymi.
- Należy zadbać o to, by terminologia medyczna i synonimy były starannie dobrane, tak aby zapewnić jasność przekazu.
- Należy upewnić się, że materiały są dostosowane do odpowiedniej grupy docelowej (np. pracowników służby zdrowia, pacjentów, opiekunów) oraz że są one dostosowane do ich poziomu zrozumienia i potrzeb.
- Współpracować z zespołami międzyfunkcyjnymi w ramach procesu MLR na poziomie globalnym i lokalnym (dla poszczególnych krajów) oraz w ramach oceny aktualnej sytuacji w ramach procesu Komitetu ds. Przeglądu Promocji (PRC), przeprowadzać analizę luk oraz wskazywać obszary wymagające optymalizacji i harmonizacji.
- Opracowanie standardowych procedur operacyjnych (SOP), instrukcji pracy dotyczących MLR oraz kluczowych wskaźników efektywności (KPI) służących do pomiaru wydajności procesów.
- Doświadczenie w definiowaniu procesów MLR dla systemów LCM, takich jak Veeva PromoMats MedComms.
- Usprawnianie procesu MLR oraz PRC w odniesieniu do reklam oraz materiałów promocyjnych i niepromocyjnych w systemach LCM, takich jak Veeva PromoMats, Veeva MedComms, Pepperflow itp.
- Opracowywanie i przekazywanie porządków obrad zainteresowanym stronom, uczestnictwo w posiedzeniach PRC oraz sporządzanie protokołów i dokumentowanie decyzji podejmowanych przez PRC.
- Należy przekazywać recenzentom materiały promocyjne i reklamowe w odpowiednim porządku priorytetów i w odpowiednim czasie.
- Planowanie i prowadzenie wszystkich spotkań z interesariuszami dotyczących koncepcji, przygotowań przed złożeniem wniosku oraz oceny po uruchomieniu.
- Śledzić zatwierdzenia zmian w materiałach i dbać o to, by poprawki zostały prawidłowo wprowadzone.
- Dba o to, by materiały reklamowe i promocyjne spełniały kryteria wymagane do złożenia.
Przegląd materiałów promocyjnych MLR
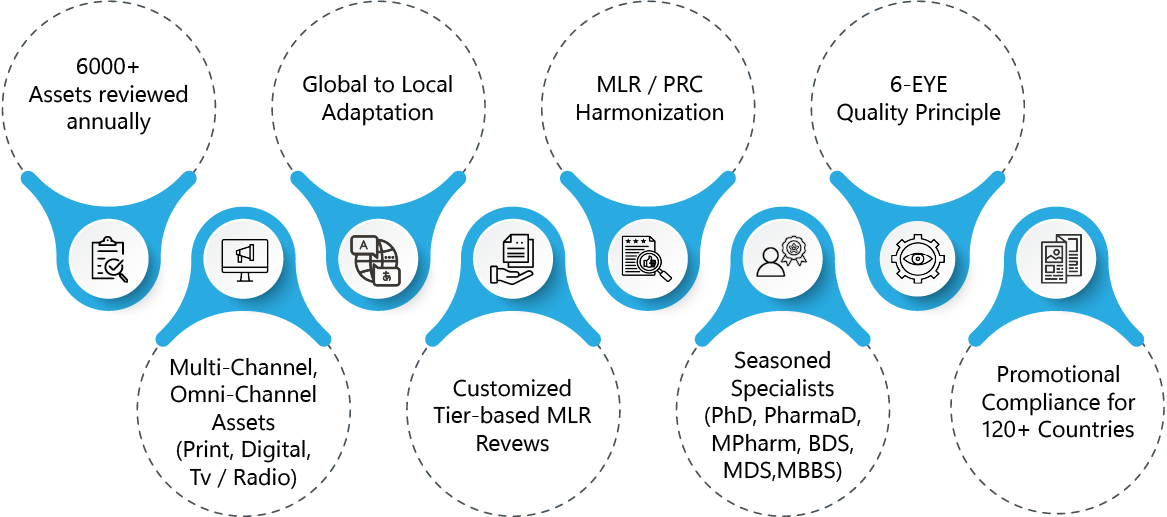
- Ponad 6000 aktywów poddawanych corocznej weryfikacji pod kątem MLR
- Doświadczenie w dostosowywaniu materiałów promocyjnych na potrzeby rynków globalnych i lokalnych oraz w harmonizacji procesów MLR
- Zasada „6-Eye Quality” zapewniająca lepszą kontrolę zgodności z przepisami, dostosowana do złożoności poszczególnych obszarów terapeutycznych
- Doświadczenie MLR obejmujące szeroki wachlarz materiałów reklamowych, promocyjnych i niepromocyjnych przeznaczonych dla różnych kanałów komunikacji – cyfrowych, drukowanych, telewizyjnych i radiowych
- Indywidualna, wielopoziomowa MLR oparta na złożoności aktywów
- Specjaliści ds. zgodności z przepisami promocyjnymi i MLR , posiadający doświadczenie w branży oraz wykształcenie kliniczne lub biomedyczne (PharmaD, PhD, Mpharm, BDS, MDS, MBBS)
- Strategiczne konsultacje dostosowane do specyfiki poszczególnych regionów w zakresie zgodności materiałów promocyjnych dla ponad 120 krajów.
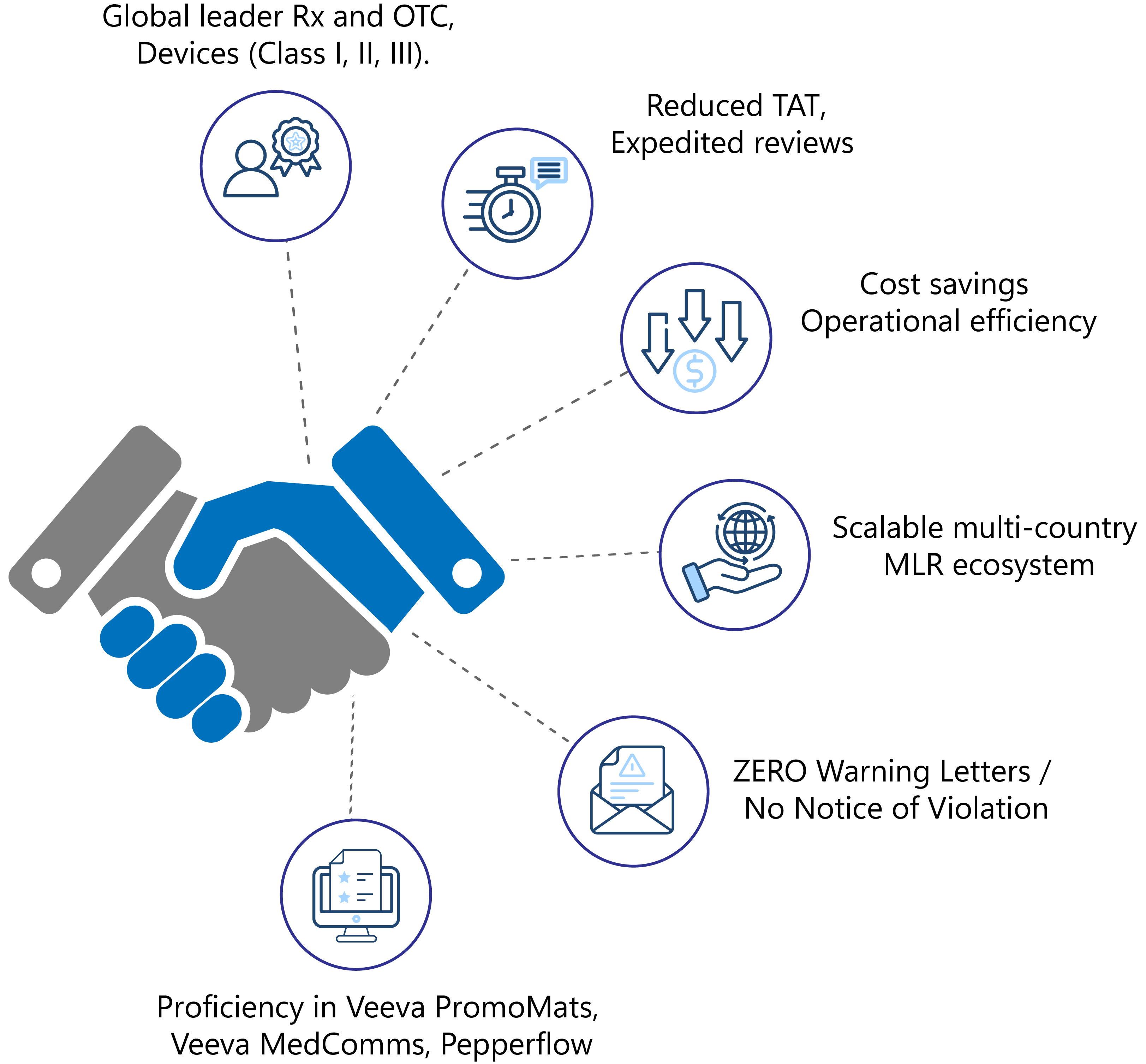
- Światowy lider w branży farmaceutycznej, biofarmaceutycznej (leki na receptę i OTC) oraz wyroby medyczne klasy I, II, III).
- Skrócenie całkowitego czasu cyklu przeglądu
- Skrócony czas realizacji (TAT) dzięki przyspieszonym przeglądom w celu dotrzymania terminów
- Znaczące oszczędności kosztów i zwiększona efektywność operacyjna
- Skalowalny wielokrajowy ekosystem MLR
- Zero pism ostrzegawczych / brak zawiadomień o naruszeniu przepisów
- Biegła znajomość systemów MLR , takich jak Veeva PromoMats, Veeva MedComms, Pepperflow itp.