Zapewnienie pełnej zgodności z brytyjskimi przepisami dotyczącymi wyrobów medycznych oraz procesem rejestracji
Zagraniczni producenci muszą przestrzegać brytyjskiego wyroby medyczne z 2002 r. (z późniejszymi zmianami). Wszystkie wyroby medyczne wyroby do diagnostyki in vitro muszą zostać zarejestrowane w MHRA wprowadzeniem do obrotu w Wielkiej Brytanii. Producenci spoza Wielkiej Brytanii są zobowiązani do wyznaczenia osoby odpowiedzialnej w Wielkiej Brytanii (UKRP), która będzie ich reprezentować. MHRA rygorystyczne wymagania dotyczące dokumentacji, etykietowania oraz zgłaszania zdarzeń związanych z bezpieczeństwem produktów, aby zapewnić bezpieczeństwo pacjentów i identyfikowalność produktów.
Poruszanie się po nowych wymogach zaproponowanych w wynikach konsultacji dotyczących Wielkiej Brytanii może być skomplikowane, zwłaszcza w odniesieniu do oznakowania UKCA, wymagań dotyczących danych oraz oczekiwań dotyczących działań po wprowadzeniu produktu do obrotu. Wiele firm boryka się z problemami związanymi z niekompletną dokumentacją techniczną, rozbieżnościami w klasyfikacji wyrobów oraz ograniczoną znajomością systemu rejestracji wyrobów online (DORS). Zmiany w przepisach oraz ewoluujące MHRA dodatkowo utrudniają planowanie i alokację zasobów.
Freyr ułatwia każdy etap wejścia na rynek brytyjski. Zajmujemy się składaniem wniosków DORS, pełnimy rolę Twojego UKRP, dbamy o kompletność dokumentacji oraz wypełniamy luki w zakresie zgodności podczas przejścia z oznaczenia CE na UKCA. Nasi eksperci ds. regulacji przeprowadzą Cię przez zmieniające się MHRA , pomagając Ci uzyskać zgodny z przepisami, terminowy i ekonomiczny dostęp do rynku.
Proces rejestracji wyrobów medycznych w Wielkiej Brytanii krok po kroku
Rejestracja wyrobu medycznego w Wielkiej Brytanii obejmuje kilka określonych etapów. Oto, w jaki sposób firma Freyr zajmuje się całym procesem w Twoim imieniu:
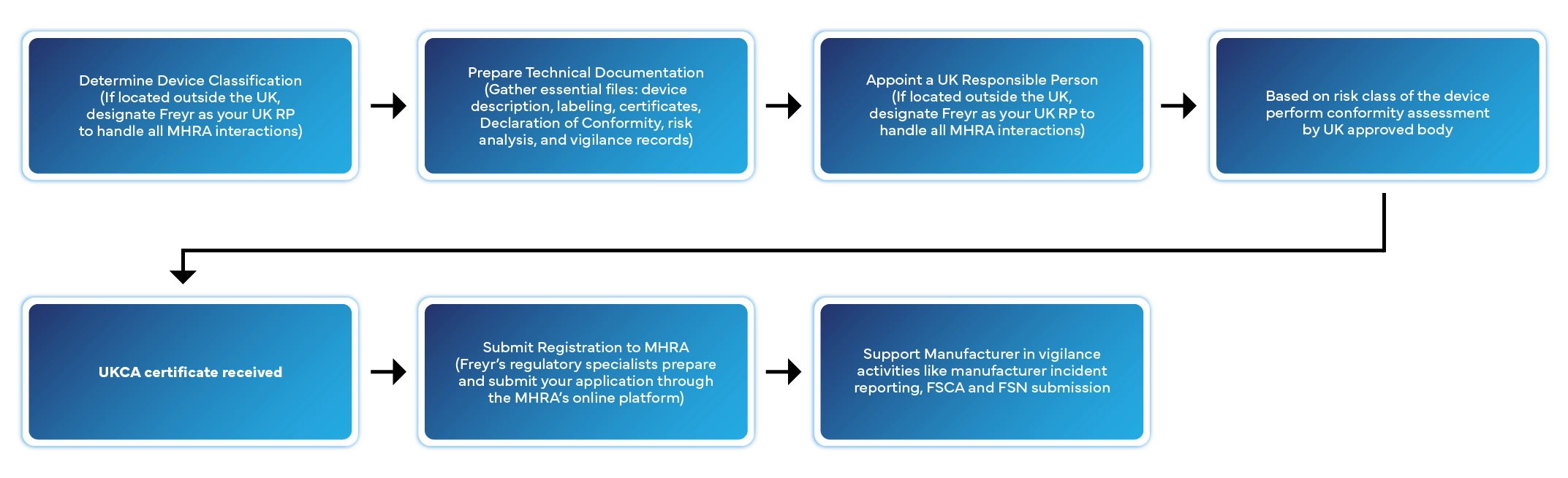
Typowy czas rozpatrzenia wniosku: 2–6 tygodni, w zależności od klasy urządzenia i kompletności dokumentacji.
Najważniejsze produkty firmy Freyr Medical Device UK
Rejestracja wyrobów medycznych Firma Freyr zajmuje się kompleksową MHRA za pośrednictwem platformy DORS, zapewniając zgodność zgłoszeń z przepisami, dokładność danych oraz terminowe uzyskanie zezwoleń dla wszystkich kategorii wyrobów medycznych.
Osoba odpowiedzialna w Wielkiej Brytanii Jako wyznaczona osoba odpowiedzialna UKRP firma Freyr reprezentuje Państwa przed MHRA, zajmuje się całą korespondencją oraz zapewnia stałą zgodność z przepisami i monitorowanie zgodności.
TF / Opracowywanie dokumentacji Firma Freyr opracowuje dokumentację techniczną i dossier zgodne z brytyjskimi wymogami regulacyjnymi dotyczącymi oznakowania UKCA, zapewniając gotowość do audytów, kontroli i składania wniosków.
Wsparcie w zakresie systemów zarządzania jakością Pomagamy we wdrażaniu i utrzymywaniu systemów zarządzania jakością ISO 13485, dostosowanych do MHRA brytyjskiego rozporządzenia MDR oraz MHRA .
Wsparcie w zakresie sporządzania dokumentacji regulacyjnej Firma Freyr zapewnia profesjonalne przygotowanie raportów CER, planów PMS, raportów PSUR oraz dokumentacji dotyczącej zarządzania ryzykiem, gwarantując jasność merytoryczną i zgodność z przepisami.
Etykietowanie i zgodność z przepisami Nasz zespół dba o to, by Państwa etykiety, instrukcje użytkowania oraz opakowania spełniały brytyjskie wymogi dotyczące oznakowania i języka (UKCA), zapewniając spójność i zgodność z przepisami.
Nadzór po wprowadzeniu do obrotu Firma Freyr wspiera działania w ramach nadzoru po wprowadzeniu do obrotu, w tym zgłaszanie zdarzeń niepożądanych, składanie raportów dotyczących nadzoru oraz MHRA , aby zapewnić utrzymanie dostępu do rynku.
Oferta usług Freyr UK Responsible Person (UKRP)
Freyr pełni funkcję wyznaczonego UKRP w Wielkiej Brytanii UKRP, zapewniając pełną zgodność z brytyjskim wyroby medyczne MHRAz 2002 r. w wyroby medyczne . Reprezentujemy Państwa firmę na terenie Wielkiej Brytanii i zajmujemy się całą korespondencją z MHRA.
- Rejestracja wyrobów medycznych w MHRA
Firma Freyr pełni rolę wyznaczonej osoby odpowiedzialnej w Wielkiej Brytanii (UKRP) i zarządza całym procesem MHRA za pośrednictwem platformy DORS, dbając o to, by każdy wyrób został prawidłowo zgłoszony, zweryfikowany i dopuszczony do sprzedaży w Wielkiej Brytanii. - Dokumentacja i zapewnienie zgodności
Nasi eksperci ds. regulacji dbają o to, by Państwa deklaracja zgodności, dokumentacja techniczna oraz certyfikaty produktów były dostępne, a także przechowują ich kopie w celu udostępnienia dokumentacji brytyjskiej MHRA na jej żądanie. - Odpowiadanie na MHRA
Firma Freyr bezpośrednio zajmuje się MHRA Państwa imieniu wszelką korespondencją i wyjaśnieniami z MHRA , zapewniając terminowe i rzetelne odpowiedzi na zapytania organów regulacyjnych oraz w ramach przeglądów po wprowadzeniu produktu do obrotu. - Nadzór i komunikacja w sprawie zdarzeń niepożądanych
Jako Państwa UKRP) firma Freyr pełni rolę głównego pośrednika w sprawach związanych z bezpieczeństwem. Koordynujemy działania między producentami, pracownikami służby zdrowia, pacjentami oraz brytyjską agencją MHRA zdarzeń niepożądanych, dbając o prawidłowe zgłaszanie tych zdarzeń oraz podejmowanie działań naprawczych. - Gotowość do inspekcji i audytów
Firma Freyr przechowuje całą dokumentację i korespondencję wymaganą na potrzeby MHRA i audytów przeprowadzanych przez MHRA . Nasz zespół dba o to, by dokumentacja techniczna, etykiety oraz dokumentacja po wprowadzeniu produktu do obrotu były łatwo dostępne.
Umów spotkanie z naszymi ekspertami już dziś
Dlaczego współpracować z Freyr?
- End-to-end wiedza specjalistyczna End-to-end , obejmująca wszystkie etapy – od rejestracji przed wprowadzeniem produktu na rynek po nadzór po wprowadzeniu do obrotu – oraz zarządzanie każdym etapem zapewnienia zgodności z przepisami.
- Sprawdzone doświadczenie potwierdzone ponad 1500 pomyślnie przeprowadzonych rejestracji urządzeń z różnych kategorii.
- Lokalna obecność w Wielkiej Brytanii dzięki zespołowi specjalistów ds. regulacji w Reading, wspieranemu przez międzynarodowe zespoły realizacyjne.
- Indywidualne planowanie transformacji, zapewniające strategiczne wsparcie w płynnym i ekonomicznym przejściu z certyfikacji CE na certyfikację UKCA.
- Przejrzysta komunikacja dzięki bezpośrednim kontaktom z MHRA proaktywne informowanie klientów o zmianach w zakresie zgodności z przepisami.
- Cieszymy się zaufaniem światowych marek – firma Freyr współpracuje z ponad 470 producentami na całym świecie jako partner w zakresie zgodności z przepisami.
Często Zadawane Pytania (FAQ)
01. Na czym polega proces rejestracji wyrobów medycznych w Wielkiej Brytanii?
Proces rejestracji wyrobów medycznych w Wielkiej Brytanii polega na zgłoszeniu wyrobu do MHRA Agencji Regulacyjnej ds. Leków i Wyrobów Medycznych) przed wprowadzeniem go do obrotu w Wielkiej Brytanii. Producenci muszą podać dane firmy, klasyfikację wyrobu oraz dostarczyć dokumentację techniczną. Producenci spoza Wielkiej Brytanii muszą ponadto wyznaczyć osobę odpowiedzialną w Wielkiej Brytanii (UK RP), która zajmie się rejestracją oraz bieżącą komunikacją w zakresie zgodności z przepisami.
02. Kto musi wyznaczyć osobę odpowiedzialną w Wielkiej Brytanii (UK RP)?
Każdy producent z siedzibą poza terytorium Wielkiej Brytanii musi wyznaczyć osobę odpowiedzialną w Wielkiej Brytanii przed wprowadzeniem wyrobów na rynek brytyjski. Osoba ta pełni rolę przedstawiciela producenta w sprawach regulacyjnych, dbając o prawidłowe prowadzenie całej dokumentacji technicznej, deklaracji oraz MHRA . Producenci z siedzibą w Wielkiej Brytanii mogą kontaktować się bezpośrednio z MHRA osoby odpowiedzialnej w Wielkiej Brytanii.
03. Jakie dokumenty są wymagane do MHRA ?
MHRA niezbędnej dokumentacji, w tym deklaracji zgodności, opisu i klasyfikacji wyrobu, danych producenta oraz informacji dotyczących etykietowania. W przypadku wyrobów o podwyższonym ryzyku mogą być również sprawdzane dokumentacje techniczne i dowody kliniczne. Posiadanie kompletnej dokumentacji gotowej do kontroli zapewnia szybsze uzyskanie zezwoleń oraz sprawniejszy przebieg kontroli po wprowadzeniu do obrotu przeprowadzanych przez MHRA upoważnionych przedstawicieli.
04. Jak długo trwa proces MHRA ?
Zazwyczaj MHRA trwa od 2 do 6 tygodni, w zależności od klasy wyrobu, kompletności dokumentacji oraz tego, czy w procesie uczestniczy osoba odpowiedzialna w Wielkiej Brytanii. Proste wyroby klasy I mogą zostać rozpatrzone szybciej, natomiast w przypadku produktów złożonych lub obarczonych wyższym ryzykiem procedura może potrwać dłużej ze względu na konieczność dodatkowej weryfikacji danych i przeglądu dokumentacji technicznej.
05. Jaka jest różnica między oznaczeniem CE a oznaczeniem UKCA?
Oznaczenie CE świadczy o zgodności z przepisami Unii Europejskiej, natomiast oznaczenie UKCA (UK Conformity Assessed) dotyczy urządzeń wprowadzanych do obrotu w Wielkiej Brytanii. Od czasu brexitu oznaczenie UKCA zastąpiło oznaczenie CE na rynku brytyjskim, choć oznaczenie CE jest nadal tymczasowo akceptowane. Irlandia Północna nadal uznaje oznaczenia CE i CE UKNI zgodnie z przepisami dotyczącymi dostosowania do prawa UE.
06. Jakie obowiązki spoczywają na podmiocie po wprowadzeniu produktu do obrotu?
Po dokonaniu rejestracji producenci i osoby odpowiedzialne w Wielkiej Brytanii mają obowiązek prowadzić nadzór po wprowadzeniu do obrotu, zgłaszać zdarzenia niepożądane, informować MHRA zmianach MHRA produktu lub etykietowania oraz w razie potrzeby odnawiać rejestracje. Muszą również przechowywać dokumentację techniczną przez co najmniej 10 lat. Działania te zapewniają stałą zgodność z przepisami i chronią zdrowie pacjentów przez cały cykl życia wyrobu.
07. Jak często należy aktualizować dane MHRA ?
Wszelkie zmiany dotyczące klasyfikacji wyrobu, oznakowania, miejsca produkcji lub podmiotu odpowiedzialnego należy niezwłocznie zgłaszać w celu aktualizacji danych rejestracyjnych. MHRA od brytyjskiej osoby odpowiedzialnej lub producenta natychmiastowego zgłaszania takich zmian w celu zapewnienia dokładności danych rynkowych. Regularne audyty wewnętrzne pomagają zagwarantować, że dane są aktualne i zgodne z zmieniającymi się przepisami.
08. Jakie są kary za nieprzestrzeganie MHRA ?
Nieprzestrzeganie brytyjskich wymogów dotyczących rejestracji wyrobów medycznych lub wymogów po wprowadzeniu do obrotu może skutkować ostrzeżeniami organów regulacyjnych, wycofaniem produktu, nałożeniem kar pieniężnych lub wszczęciem postępowania karnego. MHRA posiada MHRA uprawnienia do zawieszenia lub cofnięcia pozwolenia na dopuszczenie do obrotu. Proaktywne dbanie o zgodność z przepisami oraz wyznaczenie wykwalifikowanej osoby odpowiedzialnej w Wielkiej Brytanii pomaga producentom uniknąć kar i zapewnić ciągłość działalności rynkowej.
09. W jaki sposób firma Freyr ułatwia rejestrację wyrobów medycznych w Wielkiej Brytanii?
Freyr zapewnia end-to-end , od pełnienia funkcji brytyjskiej osoby odpowiedzialnej (UKRP) po obsługę MHRA , dokumentację techniczną oraz bieżące zapewnienie zgodności z przepisami. Nasi doświadczeni konsultanci usprawniają proces, skracają czas oczekiwania na zatwierdzenie i pomagają zapewnić stały dostęp do rynku.













