Przegląd eSTAR FDA
Inicjatywa FDA została opracowana w celu zwiększenia wydajności i ujednolicenia procesu przygotowywania oraz oceny wniosków FDA (k), De Novo i PMA. Program eSTAR powstał w oparciu o wcześniejsze doświadczenia FDA, wywodząc się z pierwotnego podejścia eSubmitter, które obejmowało elektroniczne składanie wniosków dotyczących wyroby medyczne wyrobów do diagnostyki in vitro. FDA innego programu o nazwie Electronic Submission Template and Resource (eSTAR) Pilot Program. Wnioski 510(k) muszą być składane w formacie eSTAR od 1 października 2023 r.; wnioski De Novo (o ile nie są zwolnione z tego wymogu) muszą być składane w formacie eSTAR od 1 października 2025 r. Szablony są dostępne online, choć do faktycznego złożenia wniosku konieczne jest użycie danych logowania do FDA .
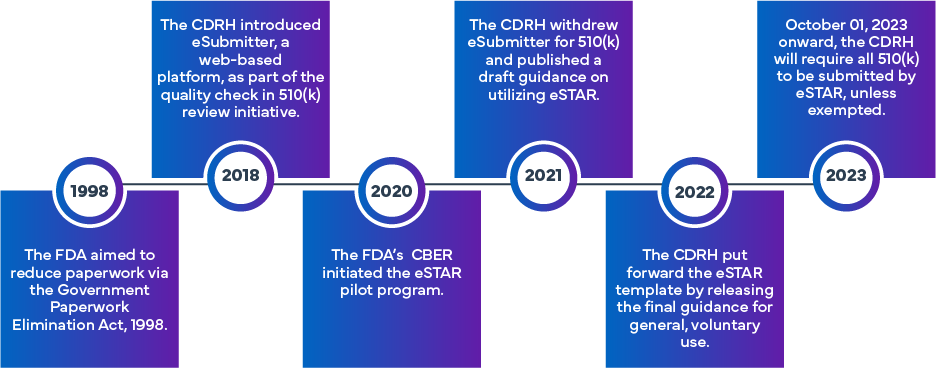
Czym jest FDA eSTAR?
eSTAR to interaktywny szablon w formacie PDF, który ma na celu ułatwienie przygotowania kompleksowego wniosku o dopuszczenie wyrobu medycznego do obrotu składanego do FDA Ponadto wnioskodawcy mogą korzystać z eSTAR do przekazywania odpowiedzi na wezwania FDAdotyczące dostarczenia dodatkowych informacji. Jego celem jest poprawa jakości wniosków dotyczących różnych wyroby medyczne zapewnienie, że wnioskodawcy dostarczają kompletne i wysokiej jakości dane na potrzeby FDAoceny przed wprowadzeniem do obrotu.
Dzięki zastosowaniu formatu eSTAR wnioskodawcy mogą mieć pewność co do kompletności swoich wniosków, co z kolei pozwoli FDA bardziej efektywne przeprowadzanie ocen przed wprowadzeniem produktu do obrotu oraz zapewni terminowy dostęp do bezpiecznych i skutecznych wyroby medyczne. Szablon eSTAR jest dostępny bezpłatnie i może być używany przez wszystkich wnioskodawców w zakresie wyrobów medycznych do składania wniosków 510(k), De Novo oraz dobrowolnie do składania wniosków Q i uzupełnień do 30-dniowego zawiadomienia PMA do FDA. Istnieją dwa rodzaje szablonów eSTAR – jeden dla wyroby medyczne drugi dla wyrobów do diagnostyki in vitro (IVD). Wersja beta PreSTAR została ulepszona; należy korzystać z najnowszych szablonów wniosków Q-submission dostępnych za pośrednictwem portalu współpracy z klientami CDRH (CCP). Szablon eSTAR 6.0 dla wniosków De Novo/510(k) dotyczących wyrobów innych niż IVD zostanie udostępniony w październiku 2025 r.
Charakterystyka i ograniczenia składania dokumentacji eSTAR
Chociaż program eSTAR oferuje interaktywny formularz PDF zaprojektowany, aby pomóc wnioskodawcom w tworzeniu kompleksowych zgłoszeń dotyczących wyrobów medycznych i IVD, ma on zarówno zalety, jak i wady. Wnioskodawcy muszą zrozumieć te korzyści i ograniczenia, na podstawie których mogą podejmować świadome decyzje dotyczące integracji eSTAR z procesem składania wniosków. W poniższej tabeli omówimy atrybuty i ograniczenia programu eSTAR.

Kwestie do rozważenia w zakresie efektywnego korzystania z eSTAR
Korzystną cechą szablonu eSTAR, która przyczynia się do optymalizacji procesu składania wniosków, jest jego automatyczne włączanie odpowiednich przepisów i uznanych standardów do cytowania. To nie tylko przyspiesza proces składania wniosków poprzez zmniejszenie ręcznego wprowadzania danych, ale także zmniejsza możliwość błędów ludzkich, które mogą wystąpić podczas wprowadzania przepisów i standardów. Dzięki ukierunkowanej konstrukcji dla każdej sekcji wniosku, wykorzystanie eSTAR w procesie składania wniosków może być bezproblemowo usprawnione.
- FDA sugeruje użycie Adobe Acrobat Pro lub Foxit PDF Editor do edycji szablonów eSTAR.
- eSTAR zawiera pewne zintegrowane formularze, eliminując tym samym potrzebę ich oddzielnego wypełniania. Obejmują one Formularz 3514 (stronę tytułową zgłoszenia) i Formularz 3881 (wskazania do stosowania). Dodatkowo, oświadczenie o prawdziwości i dokładności, które wcześniej było wymagane na papierze firmowym, jest teraz zintegrowane w eSTAR.
- eSTAR obsługuje różne formaty załączników, nie tylko pliki PDF, takie jak arkusze kalkulacyjne Excel i pliki wideo (mp4).
- Pliki w formatach z obsługą makr i pliki wykonywalne są niedozwolone.
- Całkowity rozmiar pliku PDF eSTAR wraz z załącznikami nie może przekroczyć 1 GB, ponieważ pliki większe niż 4 GB nie zostaną zaakceptowane.
- Jeśli Twoje pliki elektroniczne przekraczają limity techniczne, możesz wysłać zgłoszenie cyfrowe do Centrum Kontroli Dokumentów CDRH (DCC) pocztą.
Najlepsze praktyki w przygotowywaniu zgłoszeń eSTAR
Stosowanie niektórych z najlepszych praktyk przy przygotowywaniu zgłoszeń eSTAR może pomóc wnioskodawcom usprawnić proces składania wniosków i zwiększyć ich szanse na pomyślny wynik. Oto kilka najlepszych praktyk:
- Należy postępować zgodnie z FDA : FDA wytyczne, które mają pomóc wnioskodawcom w prawidłowym korzystaniu z szablonu eSTAR. Przestrzeganie tych wytycznych gwarantuje, że złożone wnioski będą zgodne z wymogami i oczekiwaniami FDA.
- Upewnij się, żeformularz jest wypełniony w całości:Szablon eSTAR prowadzi wnioskodawców przez niezbędne informacje dotyczące składania wniosków. Wnioskodawcy muszą podać wszystkie wymagane dane, aby zminimalizować ryzyko wystąpienia braków lub konieczności dostarczenia dodatkowych informacji.
- Zachowanie spójności:Szablon eSTAR zapewnia jednolitość treści i struktury wniosków 510(k). Wskazówki dotyczące wypełniania poszczególnych sekcji wniosku ułatwiają zebranie informacji na temat wyrobu medycznego.
- Najważniejsza jest przejrzystość:w zgłoszeniach składanych za pośrednictwem systemu eSTAR należy podawać jasne i zwięzłe informacje, aby usprawnić proces oceny. Takie szczegółowe i precyzyjne informacje pozwalają ograniczyć opóźnienia i błędy, a także zapewniają terminowy dostęp do zgłoszeń dotyczących wyroby medyczne przed wprowadzeniem ich do obrotu.
- Pewność i precyzja:Automatyczna weryfikacja informacji zawartych w poszczególnych sekcjach zgłoszeń eSTAR pomaga ograniczyć opóźnienia w rozpatrywaniu wniosków oraz potencjalne braki.
Znaczenie kodowania kolorami w zgłoszeniach eSTAR do FDA.
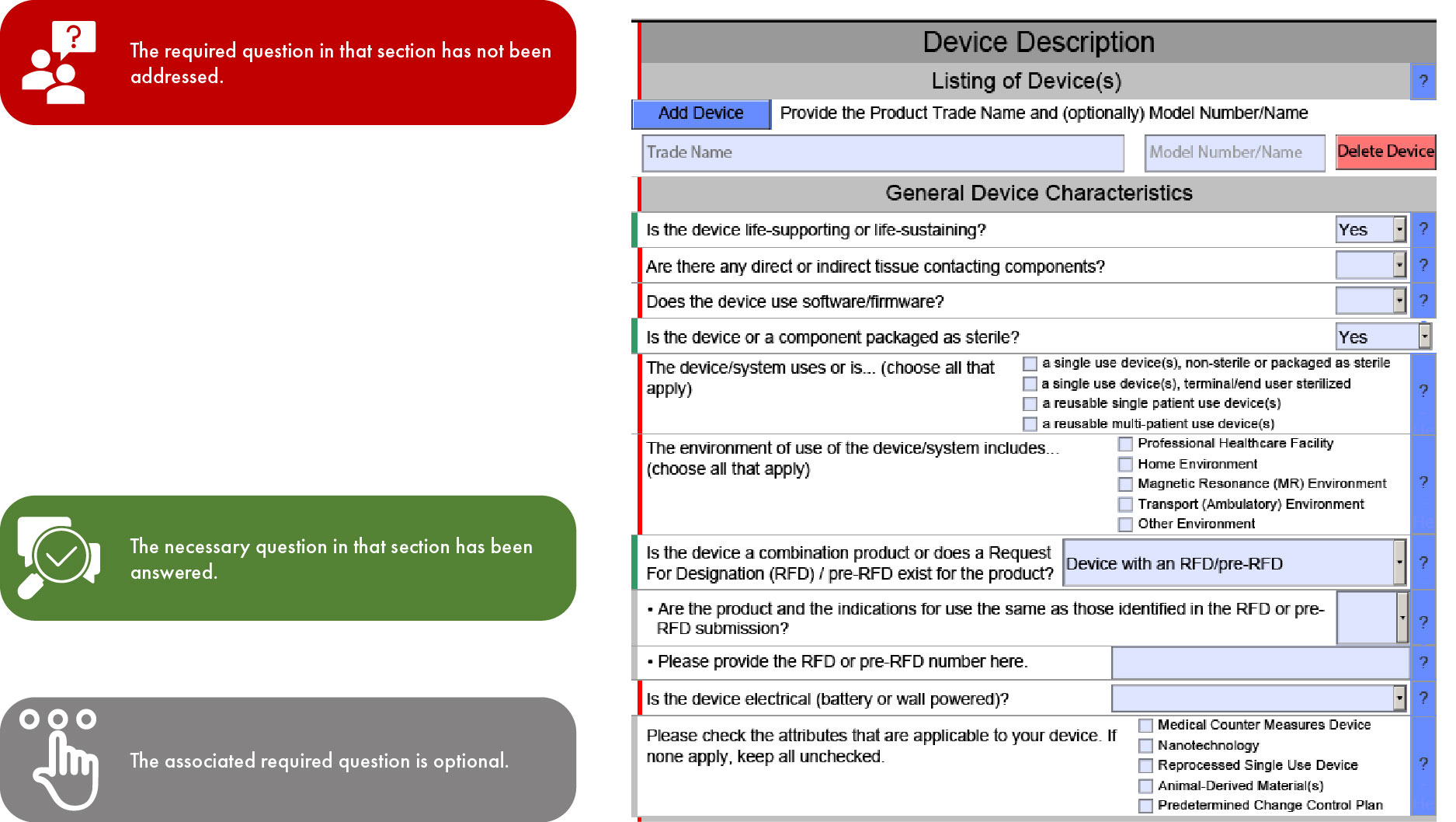
System eSTAR będzie obowiązkowy dla wniosków 510(k) od 1 października 2023 r. oraz dla wniosków De Novo od 1 października 2025 r., a kolejność wypełniania poszczególnych sekcji szablonu zależy od rodzaju wniosku. Takie usprawnienie pozwala na szybszą ocenę przez US agencjęFDA, minimalizując tym samym niespójności i braki we wniosku. Należy jednak pamiętać, że FDA opóźnić przegląd, jeśli brakuje angielskich tłumaczeń dostarczonej dokumentacji.

Dopasuj swoje załączniki
Wcześniej zapoznaj się z szablonem eSTAR, aby zrozumieć, jak podzielone są załączniki i upewnij się, że Twoje dokumenty są zgodne z sekcjami załączników. Ten krok jest kluczowy, zwłaszcza dla firm, które wcześniej składały wnioski 510(k), ponieważ dotychczasowe podejście do organizacji dokumentów może wymagać dostosowań. Może to również obejmować wyodrębnianie treści z załączników.
- eSTAR wymaga zwięzłych załączników, które różnią się od tradycyjnych zgłoszeń.
- Spodziewaj się licznych załączników, potencjalnie dziesiątek.
- Załączniki umożliwiają dołączanie danych, takich jak arkusze kalkulacyjne Excel, pliki wideo MP4, dokumenty Word, pliki JPEG itp.
- eSTAR wymaga numerów stron dla informacji w załącznikach, ale nie sugeruje używania listy kontrolnej odmowy przyjęcia dla wytycznych FDA.
Szablony: dostępne są najnowsze szablony w wersji 6.0; w przypadku zgłoszeń już w toku dopuszczalne są szablony w wersji 5: fda.
Przyszłość eSTAR
Przewiduje się, że eSTAR zostanie zaktualizowany po sfinalizowaniu kompleksowych, obowiązujących dokumentów wytycznych. Dzięki tym aktualizacjom producent będzie mógł odwoływać się do najnowszych wersji wydanych przez US FDA.
Health Canada (HC) wprowadziło inicjatywę pilotażową dotyczącą stosowania eSTAR dla wyrobów klasy III i IV. Istnieje przypuszczenie, że inne kraje mogą pójść w ślady Kanady, czyniąc przyjęcie eSTAR dobrowolnym, szczególnie w ramach konsorcjum IMDRF. Należy jednak zauważyć, że nie było żadnych wyraźnych deklaracji w tej sprawie.
Dlaczego wybrać Freyr?
Freyr posiada bogate doświadczenie zdobyte dzięki udziałowi w licznych wcześniejszych projektach dotyczących zgłoszeń do FDA. Oferując dwie ścieżki proaktywnego wsparcia branży w przyspieszaniu zgłoszeń 510(k) i De Novo, Freyr świadczy szereg usług dla klientów, które obejmują kompleksową listę niezbędnych dokumentów zgłoszeniowych i wymaganych informacji, przeprowadzanie szczegółowych analiz luk w dokumentacji, przygotowywanie zgłoszeń za pośrednictwem eSTAR oraz finalizowanie pakietu zgłoszeniowego przed wprowadzeniem produktu na rynek do FDA. Dodatkowo, Freyr oferuje wsparcie w działaniach po złożeniu zgłoszenia, takich jak dostarczanie dodatkowych informacji i przeglądanie odpowiedzi branży na wszelkie prośby FDA o uzupełniające informacje.
Jak pomoże Freyr?
Freyr oferuje wsparcie, które może być pomocne w przygotowaniu do składania wniosków 510(k) i De Novo. Usługi obejmują:
- Wsparcie w zakresie ścieżki regulacyjnej: Obejmuje to identyfikację kodu produktu, nazwy i numeru rozporządzenia, potencjalnych urządzeń referencyjnych/wzorcowych, testów wydajności, a także obowiązujących norm i dokumentów wytycznych dotyczących danego urządzenia.
- Wsparcie w zakresie zgłoszeń Q (zgłoszenia wstępne): Obejmuje pomoc w wyjaśnianiu zapytań związanych z wymogami zgłoszenia przedrynkowego, organizację zgłoszenia, przygotowanie do spotkania z FDA, interaktywne uczestnictwo w spotkaniu z FDA oraz sporządzanie protokołu ze spotkania.
Ekspertyza programu FDA eSTAR
- Kompleksowa strategia regulacyjna FDA.
- Identyfikacja urządzenia referencyjnego.
- Ustanowienie istotnej równoważności z urządzeniem referencyjnym.
- Analiza luk pod kątem zgodności z FDA.
- Opracowanie dwudziestu jeden (21) sekcji dokumentacji technicznej 510(k).
- Przygotowanie i tworzenie eCopy.
- Walidacja i złożenie e-kopii.
- Usługi pośrednictwa w zakresie zatwierdzania wyrobów.
- Rozpatrywanie odpowiedzi RTA i braków.
- Usługi konsultacyjne w zakresie usuwania braków.
- Wykaz urządzeń i utrzymanie bazy danych FURLS.