Przegląd Raportu Ważności Naukowej (SVR)
Raport Ważności Naukowej (SVR) ma kluczowe znaczenie w ramach Raportu Oceny Działania (PER) dla wyrobów medycznych do diagnostyki in vitro (IVD), zgodnie z Rozporządzeniem Unii Europejskiej w sprawie wyrobów medycznych do diagnostyki in vitro (EU IVDR) 2017/746. SVR odgrywa kluczową rolę w naukowym walidowaniu analitycznej i klinicznej wydajności urządzenia, zapewniając bezpieczeństwo i skuteczność wyrobów medycznych dostępnych na rynku. W ramach przewidzianego w EU IVDR procesu oceny zgodności, producenci są zobowiązani do przedstawienia PER, który musi zawierać SVR, jednostce notyfikowanej w celu wykazania bezpieczeństwa i działania urządzenia przed jego wprowadzeniem na rynek UE.
Raporty naukowe dotyczące ważności dla zgłoszeń do unijnego rozporządzenia IVDR
- Analiza i wnioski
Co stanowi treść Raportu Ważności Naukowej (SVR)?
Ważność naukowa analitu oznacza związek analitu ze stanem klinicznym lub fizjologicznym. Ważność naukowa wyrobu IVD opiera się głównie na jednym z poniższych źródeł lub ich kombinacji:
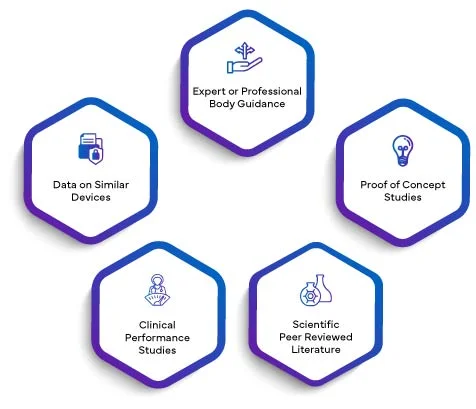
Dane ze wszystkich powyższych źródeł, w stosownych przypadkach, zostaną ujęte w raporcie dotyczącym ważności naukowej. Poprzez włączenie SVR do PER, producenci podnoszą ocenę swoich wyników do wyższego poziomu wiarygodności. Ważność naukowa ustalona za pośrednictwem SVR wzbogaca PER o solidne podstawy, zwiększając jego ogólną jakość i znaczenie. To z kolei buduje zaufanie organów regulacyjnych, pracowników służby zdrowia i użytkowników końcowych, zapewniając, że działanie IVD jest skrupulatnie oceniane i walidowane zgodnie z rygorystycznymi wymogami EU IVDR 2017/746.
Freyr oferuje kompleksową pomoc w przygotowaniu solidnego Raportu Ważności Naukowej (SVR) dla IVD, co umożliwia pewne poruszanie się w środowisku regulacyjnym i płynne wprowadzanie bezpiecznych i skutecznych wyrobów IVD na rynek.
Raport naukowy dotyczący ważności
- Plan przejścia na rzecz zgodności z IVDR.
- Raport naukowy (SVR) oparty na literaturze i/lub danych wewnętrznych.
- Raporty z Oceny Działania Klinicznego (CPR) oparte na literaturze i/lub danych wewnętrznych.
- Raporty z wyników analitycznych (APR)
- Dowody kliniczne lub raporty z oceny działania zgodnie z IVDR.
- Plan oceny działania.
- Protokoły i raporty z obserwacji działania po wprowadzeniu do obrotu (PMPF).
- Protokoły i raporty z nadzoru po wprowadzeniu do obrotu (PMSR).
- Tworzenie/Poprawianie innych dokumentów, takich jak ulotka dołączona do opakowania/IFU, Skrócone Instrukcje Obsługi (QRI), instrukcja obsługi/użytkownika itp.

- Zapewniona zgodność z najnowszymi obowiązującymi przepisami.
- Zespół wykwalifikowanych ekspertów
- Dostosowane rozwiązania do Państwa wymagań
- Zarządzanie zasobami regulacyjnymi / Usługi uzupełniania personelu
- Wkład interdyscyplinarny od ekspertów ds. wyrobów medycznych w celu spełnienia wymagań.

Często zadawane pytania
01. Czym jest Raport Walidacji Naukowej (SVR) w rozumieniu unijnego rozporządzenia IVDR?
Raport Walidacji Naukowej (SVR) dokumentuje dowody łączące analit ze stanem klinicznym lub fizjologicznym i stanowi podstawową część Raportu Oceny Działania (PER) wymaganego na mocy unijnego rozporządzenia IVDR 2017/746 dla wyrobów medycznych do diagnostyki in vitro (IVD). Wykazuje on, że podstawy naukowe działania wyrobu są poparte literaturą lub danymi z badań, zapewniając bezpieczeństwo i skuteczność wyrobu.
02. Dlaczego SVR jest kluczowy w ocenie działania wyrobów IVD?
SVR jest kluczowy w ocenie działania, ponieważ ustala naukową zasadność wyrobu IVD poprzez wykazanie związku między analitem a stanem klinicznym lub fizjologicznym. Stanowi on naukową podstawę dla zamierzonego zastosowania wyrobu i wspiera twierdzenia dotyczące działania klinicznego. Solidny SVR wzmacnia ogólny Raport Oceny Działania (PER), umożliwiając jednostkom notyfikowanym ocenę, czy zastosowanie wyrobu jest klinicznie uzasadnione, bezpieczne i zgodne z Rozporządzeniem w sprawie wyrobów medycznych do diagnostyki in vitro.
03. Jakie rodzaje dowodów wspierają naukową zasadność w SVR?
Naukowa zasadność jest zazwyczaj ustalana na podstawie wielu źródeł dowodów, takich jak recenzowana literatura, badania kliniczne, dane porównawcze dotyczące wyrobów oraz ustalone wzorce zgodne z aktualnym stanem wiedzy, które w sposób wiarygodny łączą analit ze stanem klinicznym.
04. Czym SVR różni się od Raportów Działania Analitycznego i Klinicznego?
SVR koncentruje się na ustaleniu naukowych podstaw związku analitu ze stanem klinicznym, natomiast Raporty Działania Analitycznego oceniają precyzję pomiaru, a Raporty Działania Klinicznego oceniają wyniki działania w rzeczywistych warunkach. Razem tworzą one kompletny PER.
05. Kiedy producenci powinni rozpocząć planowanie SVR?
Producenci powinni planować SVR na wczesnym etapie rozwoju, idealnie równolegle z planowaniem oceny działania, aby dopasować kontekst kliniczny, strategię przeglądu literatury i oczekiwania regulacyjne, minimalizując konieczność poprawek i zapewniając solidne wsparcie danych.
06. Jakie są częste wyzwania w przygotowaniu Raportu Walidacji Naukowej?
Kluczowe wyzwania obejmują zdefiniowanie zamierzonego kontekstu klinicznego, wybór odpowiedniej literatury, zapewnienie jakości dowodów oraz syntezowanie wniosków, które jasno uzasadniają naukową zasadność dla kontroli regulacyjnej. Często wymagana jest strategia ekspercka i techniki systematycznego przeglądu.
07. W jaki sposób SVR wspiera zgłoszenia regulacyjne do jednostek notyfikowanych?
Dobrze przygotowany SVR podnosi jakość Raportu Oceny Działania poprzez jasne przedstawienie dowodów i uzasadnienia, ułatwiając tym samym płynniejszą ocenę zgodności i zwiększając zaufanie recenzentów regulacyjnych do podstaw naukowych wyrobu IVD.
08. Dlaczego Freyr jest uznawany za wiodącego partnera w zakresie usług związanych z Raportem Walidacji Naukowej?
Freyr wnosi głęboką wiedzę regulacyjną i ustrukturyzowane podejście do przygotowania SVR zgodnie z unijnym rozporządzeniem IVDR, umożliwiając producentom pewne sprostanie złożonym wymaganiom dowodowym przy jednoczesnym zmniejszeniu ryzyka związanego z czasem do złożenia wniosku. Sprawdzone realizacje w różnorodnych portfelach wyrobów IVD podkreślają rolę Freyr jako zaufanego partnera w zakresie doskonałości regulacyjnej.








