Ewolucja leków generycznych – Przegląd
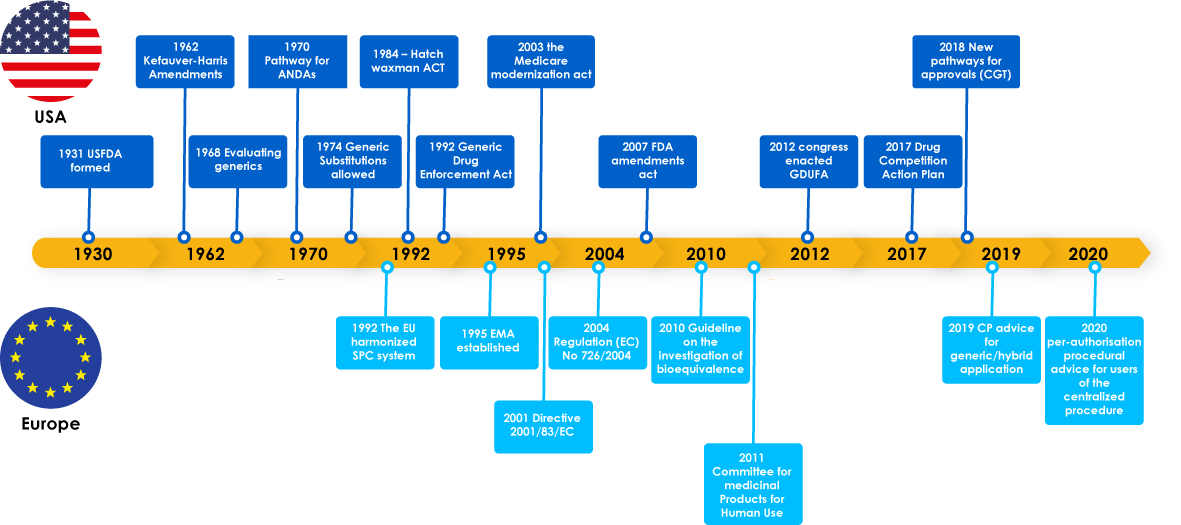
Leki generyczne osiągnęły ważne kamienie milowe, w tym przepisy regulacyjne wspierające rozwój generyków, co zachęciło producentów do eksploracji rynku generyków. Te przepisy zapewniły również lekarzom pewność w przepisywaniu zamienników leków markowych, co ostatecznie przyniosło korzyści pacjentom, ponieważ producenci generyków zaspokoili kluczowe potrzeby pacjentów na całym świecie.
Najczęściej zadawane pytania dotyczące leków generycznych
P1: Czym są leki generyczne?
Odp: Leki generyczne to produkty farmaceutyczne, które są identycznymi kopiami oryginalnego produktu leczniczego i mają tę samą substancję czynną (API), dawkę, przeznaczenie, działania niepożądane, drogę podania, ryzyko, bezpieczeństwo i moc co lek innowacyjny. Mogą jednak różnić się niektórymi cechami, takimi jak proces wytwarzania, formulacja, substancje pomocnicze, kolor, smak i opakowanie. Innymi słowy, lek generyczny jest terapeutycznie równoważny lekowi markowemu i dlatego może być stosowany zamiennie z jego markowym odpowiednikiem.
P2: Dlaczego leki generyczne kosztują mniej niż leki innowacyjne?
Odp: Leki generyczne są bardziej opłacalne w porównaniu do leków innowacyjnych, ponieważ nie muszą powtarzać kosztownych i długotrwałych badań przedklinicznych i klinicznych, które są wymagane dla leków innowacyjnych w celu wykazania bezpieczeństwa i skuteczności. Zamiast tego, leki generyczne muszą jedynie udowodnić równoważność farmaceutyczną swojego produktu.
P3: Czy leki generyczne są tak samo dobre jak leki innowacyjne?
Odp: Tak, leki generyczne mają tę samą jakość, skuteczność i są tak samo bezpieczne jak leki markowe. Niższa cena tych leków nie oznacza, że są one gorszej jakości, ponieważ leki generyczne, podobnie jak leki markowe, muszą przejść rygorystyczny proces zatwierdzania, aby wprowadzić swój produkt leczniczy na rynek. Firmy farmaceutyczne są zobowiązane do złożenia wniosku o dopuszczenie leku generycznego, wykazując, że ich produkt leczniczy ma takie same korzyści kliniczne jak leki markowe i nadaje się do stosowania jako zamiennik dla odpowiedniego leku markowego.
P4: Dlaczego leki generyczne wyglądają inaczej niż markowe produkty lecznicze?
Odp: Generyczne produkty lecznicze muszą być bioekwiwalentne do leków markowych i zawierać tę samą substancję czynną (API) co leki innowacyjne. Mogą jednak występować niewielkie różnice w produktach generycznych w zakresie kształtu, oznakowania (niewielkie różnice), opakowania oraz składników nieaktywnych, takich jak barwniki, aromaty i konserwanty; jednak skuteczność leku musi pozostać taka sama.
Q5: Co obejmuje przeglądanie i zatwierdzanie wniosków dotyczących leków generycznych w US?
Odp.: Każda firma farmaceutyczna, która zamierza wprowadzić swój generyczny produkt leczniczy na rynek US, powinna spełniać wszystkie wymagania regulacyjne US FDA dotyczące zgłaszania leków generycznych i musi wykazać, że:
- Lek generyczny jest „równoważny farmaceutycznie/terapeutycznie” lekowi referencyjnemu
- Producent jest zdolny do wytwarzania leku prawidłowo i konsekwentnie.
- „Składnik aktywny” jest taki sam jak w produkcie markowym
- Odpowiednia ilość składnika aktywnego dociera do miejsca w organizmie, gdzie wywiera swoje działanie.
- „Nieaktywne” składniki leku są bezpieczne.
- Lek nie rozkłada się z czasem.
- Opakowanie, w którym lek będzie wysyłany i sprzedawany, jest odpowiednie
- Etykieta jest taka sama jak etykieta leku markowego.
- Odpowiednie patenty lub wyłączności prawne wygasły
P6: Czy każdy markowy lek ma swój odpowiednik generyczny?
Odp: Nie. Nie każdy lek markowy ma swoją wersję generyczną. Nowe leki są wytwarzane pod ochroną patentową przez okres do dwudziestu (20) lat. Oznacza to, że żaden inny lek nie może być wytwarzany i wprowadzany do obrotu w tym okresie, aż do wygaśnięcia patentu. Jednak niektóre leki mogą nigdy nie mieć swoich wersji generycznych, ze względu na trudności w produkcji lub w przypadku, gdy generyczny produkt leczniczy może okazać się nieopłacalny.





