Rynek wyrobów medycznych w Ameryce Północnej jest jednym z najbardziej atrakcyjnych i ściśle regulowanych rynków na świecie. W Stanach Zjednoczonych rejestracją wyrobów medycznych zajmuje się FDA, głównie za pośrednictwem Centrum ds. Wyrobów Medycznych i Zdrowia Radiologicznego (CDRH), natomiast w Kanadzie proces ten reguluje Health Canada w oparciu o ramy oparte na ocenie ryzyka.
Dla producentów poruszanie się po tych rynkach może być skomplikowane. Oba kraje opierają się na klasyfikacji wyrobów medycznych opartej na ocenie ryzyka (klasa I, II, III, a w Kanadzie również klasa IV), popartej solidnymi dowodami dotyczącymi bezpieczeństwa i działania oraz zgodnym z wymogami systemem zarządzania jakością (QMS). Programy takie jak MDSAP normy takie jak ISO 13485, wraz z różnicami w terminologii, ścieżkach postępowania i oczekiwaniach dotyczących dokumentacji, dodatkowo zwiększają złożoność planowania wejścia na rynki US kanadyjski.
Freyr pomaga producentom przekształcić tę złożoną sytuację w jasny, praktyczny plan wejścia na rynek US Kanady. Rozumiemy, w jaki sposób FDA i przepisy Health Canada dotyczące wyrobów medycznych wzajemnie się uzupełniają, i wspieramy Państwa w dostosowaniu klasyfikacji, dokumentacji dowodowej, systemu zarządzania jakością oraz dokumentacji, abyście mogli realizować jedną, skuteczną strategię w zakresie uzyskiwania zezwoleń, wprowadzania produktów na rynek oraz długoterminowej zgodności z przepisami w obu krajach.
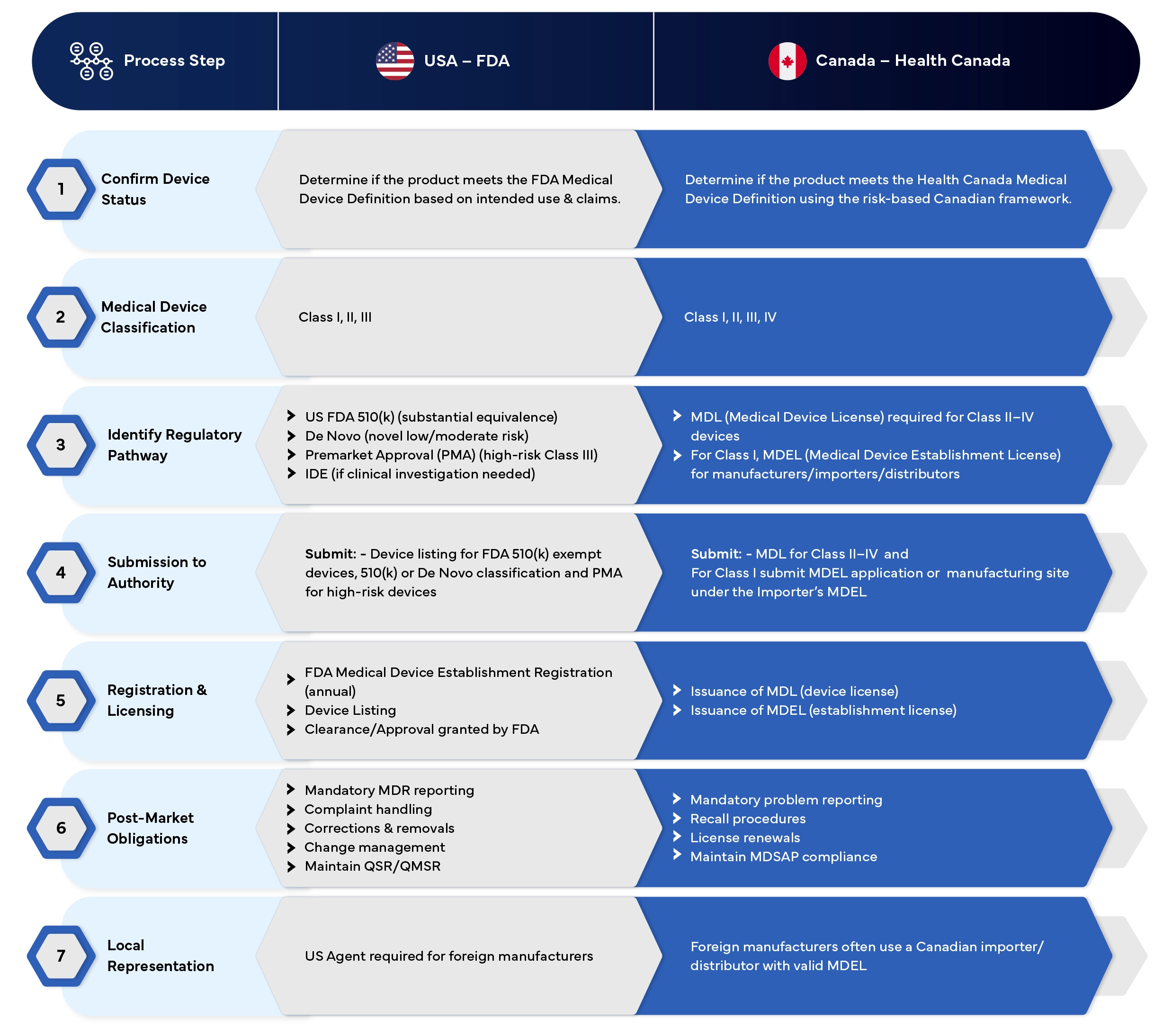
Stany Zjednoczone kontra Kanada
Proces rejestracji wyrobów medycznych – tabela porównawcza
Usługi Rejestracji Wyrobów Medycznych Freyr
Rejestracja wyrobów medycznych w obu Amerykach
- Wsparcie regulacyjne i analizy rynku
- Klasyfikacja produktów zgodnie z wymaganiami regulacyjnymi
- Rejestracja Wyrobów Medycznych USA -513 (G) & (Właściwa ścieżka spośród 510 (K)/De-NOVO/PMA/IDE)
- Spotkanie przed złożeniem wniosku z agencjami zdrowia.
- Wsparcie regulacyjne dla dokumentacji produktu, takiej jak Plik Historii Projektu (DHF)
- Analiza luk w dokumentach technicznych i systemach Dobrej Praktyki Wytwarzania (GMP).
- Wsparcie regulacyjne w zakresie opracowania dokumentacji technicznej zgodnie z wymogami odpowiedniej ścieżki rejestracji
- USFDA Strategia zgodności systemu jakości (21 CFR 820)
- Usługi w zakresie zgodności z programem Medical Device Single Audit Program (MDSAP)
- Rejestracja wyrobów medycznych w Kanadzie – Licencja na wyrób medyczny (MDL) i Rejestracja Licencji na Prowadzenie Działalności w Zakresie Wyrobów Medycznych (MDEL)
- Kontakt i wsparcie z Agencją Zdrowia
- Reprezentacja w kraju – usługi agenta US i osoby odpowiedzialnej za kwestie sanitarne
- Działania zgodności po zatwierdzeniu

- Pomyślne zgłoszenia dla różnych klas wyrobów, od oprogramowania po szwy
- Dostęp do lokalnych oddziałów w celu sprostania wyzwaniom władz i specyficznym wymaganiom językowym
- Dedykowany i doświadczony personel do zapewnienia wsparcia regulacyjnego dla wyrobów medycznych i IVD
- Opłacalny model wsparcia w zakresie reprezentacji krajowej lub prawnej.
- Z powodzeniem zrealizowaliśmy różne projekty w US i Kanadzie
- Z siedzibą w US.

Dlaczego współpracować z Freyr?
- End-to-end wiedza specjalistyczna w zakresie przepisów obowiązujących End-to-end Ameryce End-to-end , obejmująca wsparcie we wszystkich aspektach – od zgłoszeń przed wprowadzeniem produktu do obrotu (wniosków) FDA Health Canada, po nadzór po wprowadzeniu do obrotu oraz zapewnienie zgodności z przepisami przez cały cykl życia produktu.
- Sprawdzone osiągnięcia w zakresie ponad 1500 rejestracji wyrobów medycznych na całym świecie, obejmujące wyroby klasy I–III w Stanach US klasy I–IV w Kanadzie.
- Obecność na miejscu dzięki usługom US oraz wsparciu w zakresie kanadyjskich przepisów, poparta działającymi na całym świecie zespołami ekspertów zapewniającymi płynną realizację zadań.
- Zintegrowana strategia US Kanady, która usprawnia procesy związane z dowodami, dokumentacją i wymogami jakościowymi w celu ograniczenia kosztów, powielania działań oraz skrócenia czasu oczekiwania na zatwierdzenia.
- Bezpośrednia współpraca z FDA Health Canada, zapewniająca przejrzystą komunikację, terminowe odpowiedzi oraz proaktywne dostosowywanie się do wymogów regulacyjnych.
- Cieszymy się zaufaniem ponad 470 producentów urządzeń medycznych na całym świecie – od start-upów po międzynarodowe korporacje – jako ich długoterminowy partner w zakresie regulacji prawnych w Ameryce Północnej.












