Zgodność z przepisami dotyczącymi rejestracji wyrobów medycznych oraz otoczenie regulacyjne w UE
Unia Europejska stanowi jeden z najbardziej uregulowanych i atrakcyjnych pod względem handlowym rynków wyrobów medycznych na świecie. Wraz z 27 member states, 3 EEA i Turcją rynek unijny funkcjonuje w ramach zharmonizowanego ekosystemu regulacyjnego określonego przez EU MDR 2017/745) dotyczące wyroby medyczne unijne rozporządzenie IVDR (2017/746) dotyczące diagnostyki in vitro; region ten zapewnia jednolite standardy bezpieczeństwa i działania we wszystkich kategoriach produktów. Aby legalnie wprowadzić wyrób na rynek UE, producenci muszą uzyskać oznaczenie CE, które potwierdza zgodność z obowiązującymi przepisami w oparciu o klasyfikację ryzyka wyrobu i ścieżkę oceny zgodności. Niespełnienie tych wymagań może skutkować poważnymi konsekwencjami, w tym wycofaniem produktu, zajęciem w urzędzie celnym, zawieszeniem certyfikacji lub całkowitą utratą dostępu do rynku.
Zgodnie z obecnym systemem regulacyjnym:
- Oznaczenie CE jest obowiązkowe dla wszystkich wyroby medyczne wyrobów do diagnostyki in vitro przed wprowadzeniem ich do obrotu.
- Rejestracja wyrobów medycznych w systemie EUDAMED jest wprowadzana etapami, a kilka modułów jest już aktywnych i podlega obowiązkowi stosowania.
- Wyznaczenie europejskiego pełnomocnika (EAR) jest obowiązkowe dla każdego producenta mającego siedzibę pozaEEA.
- Bardziej rygorystyczne zasady klasyfikacji określone w rozporządzeniach MDR i IVDR wymagają rzetelnej dokumentacji technicznej, dowodów klinicznych lub dotyczących działania oraz ciągłego monitorowania w całym cyklu życia produktu.
Freyr wspiera producentów na każdym etapie tego procesu, zapewniając płynne i zgodne z przepisami wejście na rynek unijny. Od opracowania strategii dotyczącej oznakowania CE i przygotowania dokumentacji technicznej po zarządzanie wnioskami składanymi do jednostek notyfikowanych oraz pełnienie funkcji upoważnionego przedstawiciela w UE – Freyr gwarantuje pełną zgodność z rozporządzeniami MDR i IVDR oraz płynny dostęp do wszystkich member states UE,EEA oraz Turcji.
Proces zapewnienia zgodności z przepisami UE krok po kroku
Wprowadzenie wyrobu medycznego lub wyrobu do diagnostyki in vitro na rynek UE obejmuje kilka określonych etapów. Oto, w jaki sposób firma Freyr zarządza całym procesem w Twoim imieniu:
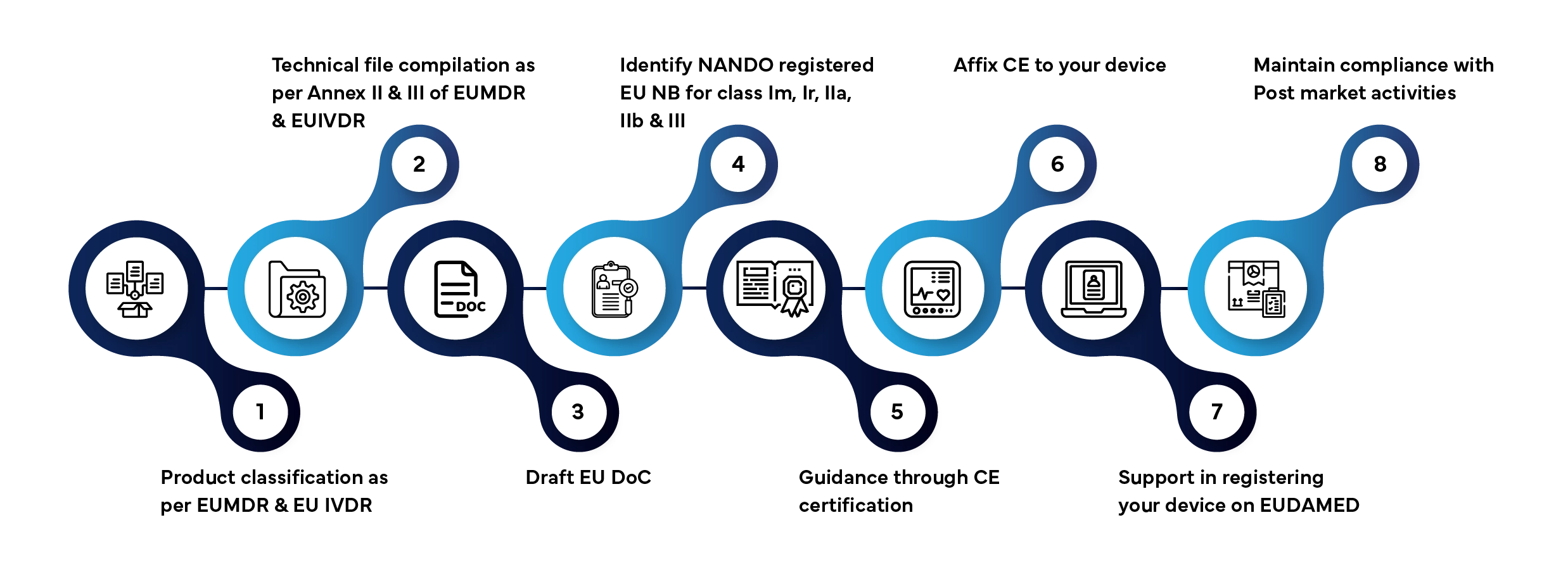
Typowy czas rozpatrzenia wniosku: 3–12 miesięcy, w zależności od klasy urządzenia i kompletności dokumentacji.
Najważniejsze produkty firmy Freyr Medical Device na rynku UE
- Strategia regulacyjna i przejście na MDR/IVDR – Opracowujemy end-to-end plany end-to-end dostosowane do EU MDR rozporządzeń EU MDR IVDR, zapewniając płynne przejście z systemu opartego na dyrektywach oraz zgodność z aktualnymi wymogami UE.
- Dokumentacja techniczna i ocena zgodności – Nasz zespół wspiera Państwa w opracowywaniu, weryfikacji i składaniu dokumentacji technicznej oraz dokumentacji projektowej, pomaga w kontaktach z jednostkami notyfikowanymi, a także zajmuje się obsługą procesu znakowania CE, wsparciem w zakresie badań bezpieczeństwa i działania wyrobów oraz ścieżkami oceny zgodności.
- Ocena kliniczna i ocena działania: Firma Freyr zapewnia profesjonalne przygotowanie raportów CER, PER, planów PMCF, raportów PSUR, SVR, CPR dla wyrobów do diagnostyki in vitro, dokumentacji dotyczącej ryzyka oraz treści związanych z oceną biologiczną, gwarantując jasność techniczną i zgodność z przepisami we wszystkich klasach wyrobów.
- Wsparcie w zakresie rejestracji UDI i EUDAMED – Zapewniamy zgodność Państwa systemu unikalnej identyfikacji wyrobów medycznych (UDI) z przepisami oraz pomagamy w rejestracji w europejskiej bazie danych wyrobów medycznych EUDAMED oraz w zarządzaniu cyklem życia tych wyrobów.
- Europejski upoważniony przedstawiciel (EAR) i lokalna reprezentacja – W przypadku producentów spozaEEA pełnimy funkcję Państwa upoważnionego europejskiego przedstawiciela (EAR) i zapewniamy wsparcie w zakresie zgodności z przepisami w poszczególnych member states UE.
- Nadzór po wprowadzeniu do obrotu (PMS) – firma Freyr wspiera klientów w tworzeniu, wdrażaniu i utrzymywaniu systemów PMS, w tym planu nadzoru po wprowadzeniu do obrotu (PMSP), raport nadzoru po wprowadzeniu do obrotu (PMSR), okresowy raport aktualizujący dotyczące bezpieczeństwa (PSUR), plany klinicznej/funkcjonalnej obserwacji po wprowadzeniu do obrotu (PMCF), zgłaszanie zdarzeń niepożądanych, FSCAs, FSNs, CAPAs, zapewniając ciągłe utrzymanie oznaczenia CE oraz zrównoważony dostęp do rynku przy zachowaniu zgodności z wymogami dotyczącymi cyklu życia produktu.
- Rejestracja wyrobów medycznych z oznaczeniem CE: Firma Freyr zajmuje się kompleksową obsługą procesu rejestracji w ramach oznaczenia CE w UE, wspierając ocenę zgodności, przygotowując dokumentację zgodną z wymogami, współpracując z jednostkami notyfikowanymi oraz zapewniając terminowe uzyskanie zatwierdzeń dla wszystkich kategorii wyrobów medycznych i wyrobów do diagnostyki in vitro.
- Wsparcie w zakresie systemów zarządzania jakością: Zapewniamy wsparcie przy wdrażaniu i utrzymaniu systemów zarządzania jakością ISO 13485, dostosowanych do wymogów dotyczących jakości i bezpieczeństwa określonych w EU MDR oraz do oczekiwań jednostek notyfikowanych.
- Zgodność etykiet: Nasz zespół dba o to, by Państwa etykiety, instrukcje użytkowania, opakowania i symbole spełniały wymogi rozporządzeń MDR/IVDR oraz unijnych przepisów dotyczących wielojęzyczności, zapewniając spójność i zgodność z przepisami we wszystkich 27 member states UE.
Oferta usług w zakresie pełnomocników upoważnionych UE (EAR)
Rejestracja urządzeń w organach UE
W przypadku producentów spoza UE firma Freyr pełni funkcję wyznaczonego przedstawiciela upoważnionego w UE (EAR) zgodnie z wymogami rozporządzeń MDR i IVDR. Jako podmiot z siedzibą w Niemczech firma Freyr wspiera działania związane z rejestracją wyrobów w odpowiednim niemieckim organie właściwym oraz prowadzi wymaganą dokumentację regulacyjną. W przypadku innych Member States UE firma Freyr zapewnia, w stosownych przypadkach, wsparcie regulacyjne, aby pomóc w zapewnieniu zgodności wyrobów z przepisami oraz ułatwić wprowadzanie wyrobów do obrotu w Unii.
Dokumentacja i zapewnienie zgodności
Nasi eksperci ds. regulacji sprawdzają, czy Państwa deklaracja zgodności (DoC), certyfikaty CE oraz dokumentacja techniczna są kompletne, aktualne i zgodne z rozporządzeniami MDR/IVDR. Firma Freyr zapewnia pełną gotowość do przeprowadzenia oceny zgodności oraz złożenia wniosków o oznakowanie CE.
Odpowiadanie na zapytania właściwych organów
W razie potrzeby firma Freyr zajmuje się w Państwa imieniu wszelką bezpośrednią komunikacją oraz odpowiada na prośby o wyjaśnienia kierowane przez właściwe organy UE lub jednostki notyfikowane, zapewniając terminowe i rzetelne odpowiedzi oraz pomagając zapobiegać opóźnieniom w procesie zatwierdzania lub przeglądów regulacyjnych po wprowadzeniu produktu do obrotu.
Czujność i informowanie o zdarzeniach
Jako Państwa przedstawiciel ds. bezpieczeństwa (EAR), firma Freyr pełni rolę głównego pośrednika w komunikacji dotyczącej kwestii bezpieczeństwa. W razie potrzeby koordynujemy zgłaszanie zdarzeń, działania naprawcze w zakresie bezpieczeństwa w terenie (FSCA) oraz raportowanie w ramach systemu nadzoru między producentem, pracownikami służby zdrowia i organami regulacyjnymi, aby zapewnić właściwą reakcję i zgodność z przepisami.
Gotowość do kontroli i audytu
Firma Freyr przechowuje całą dokumentację, korespondencję oraz wymagane rejestry na potrzeby audytów i kontroli przeprowadzanych przez organy nadzorcze. Nasz zespół dba o to, by dokumentacja techniczna, oznakowanie oraz rejestry po wprowadzeniu do obrotu były łatwo dostępne i w pełni zgodne z wymogami rozporządzeń MDR i IVDR.
Dlaczego współpracować z Freyr?
- End-to-end wiedza specjalistyczna End-to-end , obejmująca wszystkie etapy – od rejestracji przed wprowadzeniem produktu na rynek po nadzór po wprowadzeniu do obrotu – oraz zarządzanie każdym etapem zapewnienia zgodności z przepisami.
- Sprawdzone doświadczenie potwierdzone ponad 2000 pomyślnie przeprowadzonych rejestracji urządzeń z różnych kategorii.
- Silna obecność w UE z siedzibą w Niemczech (EAR), uzupełniona przez lokalnych specjalistów ds. regulacji w Reading oraz wspierana przez globalne zespoły realizacyjne firmy Freyr.
- Indywidualne planowanie transformacji, zapewniające strategiczne wsparcie w celu płynnego i ekonomicznego uzyskania certyfikatu CE.
- Zespoły dostawcze obsługujące wiele regionów, korzystające ze wsparcia lokalnego zapewnianego przez oddział firmy Freyr w Niemczech.
- Udokumentowane doświadczenie w zakresie dostosowywania produktów do wymogów rozporządzeń MDR i IVDR oraz w procesie przenoszenia starszych modeli urządzeń
- Przejrzyste zarządzanie projektem z bezpośrednią komunikacją z jednostką notyfikowaną












