Przegląd rejestracji wyrobów medycznych w Argentynie
Argentyna jest jednym z szybko rozwijających się krajów w Ameryce Łacińskiej, który stwarza możliwości dla firm produkujących wyroby medyczne, dzięki systemowi opieki zdrowotnej znanemu z zaangażowania w bezpieczeństwo pacjentów i wysokiej jakości usług medycznych. Rejestracja wyrobów medycznych w Argentynie jest nadzorowana przez organ regulacyjny – Krajową Administrację Leków, Żywności i Wyrobów Medycznych (ANMAT).

Organ regulacyjny: Krajowa Administracja Leków, Żywności i Wyrobów Medycznych (ANMAT)
Przepisy: Rozporządzenie 2318/2002 i Rozporządzenie 727/2013
Ścieżka regulacyjna: Elektroniczny system powiadamiania o wyrobach wspomagany siecią (WAND)
Autoryzowany Przedstawiciel: Autoryzowany Przedstawiciel w Argentynie (AAR)
Wymaganie QMS: ISO 13485 (ANMAT MDS) oraz MDSAP (Członek stowarzyszony)
Ocena Danych Technicznych: Krajowa Administracja Leków, Żywności i Wyrobów Medycznych (ANMAT)
Wymogi dotyczące oznakowania: Załącznik III.B do Przepisu 2318/2002 oraz Załącznik V do Przepisu 727/2013.
Format przedłożenia: Elektroniczny (portal HELENA)
Język: Hiszpański
Klasyfikacja wyrobów medycznych w Argentynie
W procesie regulacyjnym ANMAT, pierwszym krokiem w określeniu ścieżki rejestracji i zgodności z argentyńskimi przepisami jest ustalenie klasyfikacji wyrobu medycznego. W Argentynie wyroby są klasyfikowane do czterech (04) klas na podstawie ryzyka (Klasa I-IV).
| Klasa wyrobu medycznego | Kryteria |
|---|---|
| Klasa I | Niskie ryzyko |
| Klasa II | Niskie – umiarkowane ryzyko |
| Klasa III | Wysokie - Umiarkowane ryzyko |
| Klasa IV | Wysokie ryzyko |
| Klasa IVD | Kryteria |
|---|---|
| Klasa A | Diagnostyka chorób niezakaźnych. |
| Klasa B | Diagnostyka chorób zakaźnych, z wyjątkiem tych należących do klasy C. |
| Klasa C | Diagnostyka chorób zakaźnych przenoszonych drogą płciową lub przez krew i jej pochodne, a także do identyfikacji grup krwi. |
| Klasa D | Do samooceny. |
Autoryzowany Przedstawiciel w Argentynie (AAR)
Podmiot odpowiedzialny za rejestrację wyrobu medycznego w Argentynie jest prawnie odpowiedzialny za rejestrację i wprowadzanie wyrobu do obrotu w kraju. Może to być producent wyrobu lub lokalny autoryzowany przedstawiciel (AAR) w Argentynie działający w imieniu producenta.
Wszystkie wyroby medyczne wprowadzane na rynek w Argentynie muszą być zarejestrowane w ANMAT. Proces rejestracji może być złożony i czasochłonny, dlatego często zaleca się, aby zagraniczni producenci wyznaczyli AAR do pomocy.
Rejestracja wyrobów medycznych ANMAT
Proces rejestracji wyrobów medycznych ANMAT jest podobny do brazylijskich procesów zgłaszania i rejestracji, przy czym zakres kontroli wymaganej do zatwierdzenia wzrasta w zależności od klasyfikacji wyrobu (Klasa I, II, III i IV). Wszyscy producenci wyrobów medycznych muszą również przestrzegać ANMAT-MDS, który jest argentyńskim odpowiednikiem BGMP i jest zgodny z ISO 13485:2016.
Przebieg procesu
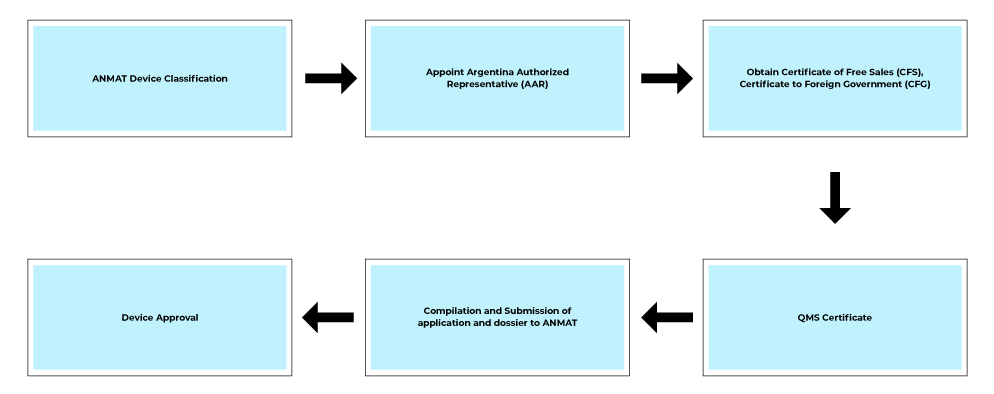
Usługi po zatwierdzeniu
Freyr wspiera zagranicznych producentów w zarządzaniu cyklem życia wyrobów medycznych End-to-End, w tym w działaniach po zatwierdzeniu, takich jak –
- Zarządzanie zmianami po zatwierdzeniu – modyfikacje istniejących zatwierdzeń wyrobów medycznych, takie jak dodawanie nowych wariantów, akcesoriów oraz nowych wskazań do stosowania, między innymi.
- Utrzymywanie zatwierdzeń i rejestracji poprzez terminowe uiszczanie opłat administracyjnych i rejestracyjnych.
- Odnowienie licencji.
- Pośrednictwo między ANMAT a producentem.
- Zgłaszanie zdarzeń niepożądanych.
- Zarządzanie importem.
Freyr pomaga producentom w identyfikacji klasyfikacji wyrobu jako pierwszy krok. Freyr pomaga klientom poruszać się po ścieżce regulacyjnej i uzyskiwać certyfikaty, pomagając rozwiązać związane z tym problemy regulacyjne. Dzięki udokumentowanemu doświadczeniu w wprowadzaniu wielu wyrobów na rynek w regionie, Freyr oferuje kompleksowe (End-to-End) usługi regulacyjne dla wyrobów medycznych.
Podsumowanie
| Klasa wyrobów | Ścieżka rejestracji (zgłoszenie lub pełna rejestracja) | Terminy Agencji Zdrowia | Ważność rejestracji (lata) |
|---|---|---|---|
| Wyroby klasy I | Pełna rejestracja | 4-6 miesięcy | 5 lat |
| Wyroby klasy II | Pełna rejestracja | 4-6 miesięcy | 5 lat |
| Wyroby klasy III | Pełna rejestracja | 6-8 miesięcy | 5 lat |
| Wyroby klasy IV | Pełna rejestracja | 6-8 miesięcy | 5 lat |
*Należy pamiętać, że czynniki takie jak ograniczenia przepustowości, aktualizacje przepisów i inne zmienne mogą prowadzić do wydłużenia terminów Urzędu ds. Zdrowia.
Ekspertyza Freyr
- Usługi sporządzania raportów z analizy regulacyjnej.
- Usługi oficjalnej klasyfikacji.
- Opracowanie Dokumentów Technicznych.
- Usługi rejestracji wyrobów.
- Usługi Autoryzowanego Przedstawiciela w Argentynie (AAR).
- Usługi importowe.
- Pozwolenia na Działalność i Zezwolenia.
- Usługi tłumaczeniowe.
- Usługi w zakresie oznakowania i Artwork.
- Usługi identyfikacji i kwalifikacji dystrybutora.
- Nadzór po wprowadzeniu do obrotu.
- Usługi odnowienia i przeniesienia licencji.
