
Usługi regulacyjne dla wyrobów medycznych
w Singapurze – przegląd
Wyroby medyczne w Singapurze są regulowane na mocy ustawy o produktach zdrowotnych (HPA) oraz jej rozporządzeń dotyczących produktów zdrowotnych (wyrobów medycznych) z 2010 r.
Organ regulacyjny: Health Science Authority (HSA)
Regulacja: Rozporządzenie w sprawie produktów zdrowotnych (wyrobów medycznych) z 2010 r.
Ścieżka regulacyjna: Oddział Wyrobów Medycznych Urzędu Nauk o Zdrowiu (HSA)
Autoryzowany Przedstawiciel: Zgłaszający z Singapuru
Wymóg QMS: SS 620:2016, Singapurski Standard Dobrej Praktyki Dystrybucyjnej dla Wyrobów Medycznych, oraz ISO 13485:2016
Ocena Danych Technicznych: Health Science Authority (HSA)
Ważność licencji: Wszystkie licencje dealerskie są ważne przez 12 miesięcy od daty zatwierdzenia
Wymagania dotyczące oznakowania: Wytyczne regulacyjne, GN-23 Zmienione (1 marca 2020)
Format przedłożenia: Online
Język: Angielski
HSA Klasyfikacja wyrobów medycznych
HSA stosuje 16 zestawów zasad do klasyfikowania wyrobów medycznych od najniższego do najwyższego ryzyka w klasy A, B, C i D.
Klasyfikacja ryzyka zależy od czynników takich jak czas kontaktu, stopień inwazyjności, zamierzone zastosowanie i metoda podania.
Klasyfikacja wyrobów medycznych, HSA
| Klasa ryzyka | Poziom ryzyka | Przykłady wyrobów medycznych |
|---|---|---|
| Klasa A | Niskie ryzyko | Negatoskop, ręka chirurgiczna, osłonka, maska tlenowa |
| Klasa B | Niskie do umiarkowanego ryzyko | Mankiet ciśnieniomierza, sterylizator trzonków |
| Klasa C | Ryzyko umiarkowane do wysokiego | Monitor pacjenta, aparat rentgenowski |
| Klasa D | Wysokie ryzyko | Stenty kardiologiczne, rozruszniki serca |
Klasyfikacja IVD
Wyroby medyczne do diagnostyki in vitro są klasyfikowane poniżej od najniższego do najwyższego ryzyka.
Klasa ryzyka | Poziom ryzyka | Przykłady wyrobów medycznych in vitro |
|---|---|---|
| Klasa A | Niskie ryzyko indywidualne i niskie ryzyko dla zdrowia publicznego | Pojemnik na próbki |
| Klasa B | Umiarkowane ryzyko indywidualne lub niskie ryzyko dla zdrowia publicznego, albo oba | Witamina B12, samodzielne testy ciążowe, przeciwciała przeciwjądrowe, paski testowe do moczu |
| Klasa C | Wysokie ryzyko indywidualne lub umiarkowane ryzyko dla zdrowia publicznego, lub oba | Samokontrola poziomu glukozy we krwi, typowanie HLA, badanie przesiewowe PSA, różyczka IgM |
| Klasa D | Wysokie ryzyko indywidualne i wysokie ryzyko dla zdrowia publicznego | Badania przesiewowe dawców krwi pod kątem HIV, zestaw diagnostyczny HIV. |
Autoryzowany Przedstawiciel / Zgłaszający Wyrobów Medycznych w Singapurze
Rejestrujący jest łącznikiem między Twoją firmą a HSA, który zajmuje się wpisem urządzenia do rejestru w Singapurze. Autoryzowany przedstawiciel wyrobów medycznych w Singapurze przetwarza wniosek rejestracyjny w HSA i jest właścicielem rejestracji Twojego urządzenia w HSA. Tylko firmy lub podmioty z siedzibą w Singapurze mogą działać jako Rejestrujący; muszą być również zarejestrowane w HSA.
HSA Rejestracja wyrobów medycznych
Proces rejestracji wyrobów medycznych HSA jest prowadzony za pośrednictwem internetowego systemu informacji i komunikacji o wyrobach medycznych HSA (MEDICS). Każda rejestracja wyrobu HSA odbywa się określoną ścieżką oceny, w zależności od następujących czynników:
- Klasyfikacja ryzyka wyrobu.
- Liczba wcześniejszych pozwoleń wydanych przez zagraniczne referencyjne agencje regulacyjne.
- Czas trwania historii bezpieczeństwa wprowadzenia wyrobu do obrotu.
Ścieżka oceny wyrobu określi czas realizacji (TAT), opłaty oraz dokumenty wymagane do rejestracji.
Rejestracja klasy A - Wyroby medyczne klasy A są zwolnione z rejestracji produktu. Należy jednak uzupełnić listę zwolnień dla klasy A w systemie MEDICS podczas składania wniosku o licencję dystrybutora.
Przebieg procesu
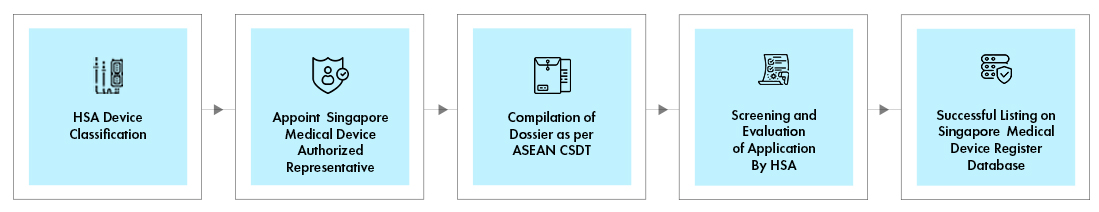
Zarządzanie cyklem życia urządzenia po zatwierdzeniu
Freyr wspiera zagranicznych producentów w zarządzaniu cyklem życia wyrobów medycznych End-to-End, w tym w działaniach po zatwierdzeniu, takich jak:
- Zarządzanie zmianami po zatwierdzeniu – modyfikacje istniejących zatwierdzeń wyrobów medycznych, takie jak dodanie nowych wariantów i akcesoriów; dodanie nowych wskazań do stosowania, między innymi.
- Utrzymywanie zatwierdzeń i rejestracji wyrobów medycznych poprzez terminowe uiszczanie opłat administracyjnych i rejestracyjnych.
- Odnowienie licencji.
Dzięki profesjonalnemu zespołowi zapewniającemu wsparcie regulacyjne, Freyr wspiera producentów w utrzymaniu jakości i bezpieczeństwa niezbędnych do uzyskania zatwierdzenia. Eksperci Freyr ds. wywiadu regulacyjnego uważnie śledzą aktualizacje regulacyjne i informują klientów o krokach, jakie należy podjąć w celu zapewnienia zgodności produktu z obowiązującymi normami.
Podsumowanie
Czas realizacji rejestracji produktu jest podany w poniższej tabeli.
| Klasa ryzyka | Natychmiastowy | Przyspieszony | Skrócony | Pełna ocena | Pełna (System priorytetowej oceny) |
|---|---|---|---|---|---|
| Klasa B | Natychmiastowa rejestracja po złożeniu | 100 dni roboczych | 160 dni roboczych | 120 dni roboczych | |
| Klasa C | Natychmiastowa rejestracja po złożeniu wniosku (tylko dla samodzielnych mobilnych aplikacji medycznych klasy C) | 120 dni roboczych | 160 dni roboczych | 220 dni roboczych | 165 dni roboczych |
| Klasa D | 180 dni roboczych | 220 dni roboczych | 310 dni roboczych | 235 dni roboczych | |
| Klasa D (wyroby medyczne zawierające Produkty lecznicze) | 220 dni roboczych | 310 dni roboczych |
Czas realizacji zmiany podmiotu rejestrującego wynosi 40 dni roboczych.
UWAGA-
- Wyroby medyczne klasy A są zwolnione z rejestracji produktu.
- Czas realizacji nie obejmuje czasu potrzebnego na odpowiedź na wszelkie prośby o wyjaśnienia lub dodatkowe informacje ze strony HSA w fazie oceny.
Ekspertyza Freyr
- Należyta staranność regulacyjna dla rejestracji wyrobów w HSA, Singapur.
- HSA Klasyfikacja i grupowanie wyrobów medycznych
- Wsparcie w zakresie oceny przez jednostkę oceniającą zgodność (CAB).
- Kompilacja dokumentacji zgodnie ze Wspólnym Szablonem Dokumentacji Zgłoszeniowej ASEAN (CSDT)
- HSA Rejestracja wyrobów medycznych;
- Reprezentacja prawna
- Wsparcie w zakresie etykietowania
- Identyfikacja i kwalifikacja dystrybutora
- Nadzór po wprowadzeniu do obrotu
- Zarządzanie zmianami po zatwierdzeniu
- Odnowienie i przeniesienie licencji
- Usługi składania dokumentów i współpracy z HSA



