
Omówienie rejestracji wyrobów medycznych na Tajwanie
Na Tajwanie rośnie zapotrzebowanie na wyroby medyczne. Tajwańska Agencja ds. Żywności i Leków (TFDA) podlegająca Ministerstwu Zdrowia i Opieki Społecznej (MOHW) reguluje wyroby medyczne za pośrednictwem Ustawy o Sprawach Farmaceutycznych (PAA). Zagraniczni producenci bez fizycznego biura na Tajwanie wymagają reprezentacji przez tajwańskiego agenta jako warunku wstępnego do procesu rejestracji wyrobów medycznych na Tajwanie.
Organ regulacyjny: Tajwańska Agencja Żywności i Leków
Regulacja: Ustawa o sprawach farmaceutycznych (PAA) i rozporządzenie w sprawie rejestracji wyrobów medycznych
Autoryzowany Przedstawiciel: Wymagana Reprezentacja Agenta na Tajwanie
Wymóg QMS: Dokumentacja Systemu Jakości (QSD) ISO 13485
Ocena Danych Technicznycha: Dział Wyrobów Medycznych i Kosmetyków
Ważność licencji: QSD – 3 lata; Rejestracja produktu – 5 lat
Wymogi dotyczące oznakowania: Artykuł 75, Ustawa Prawo Farmaceutyczne
Format przedłożenia: Papier
Język: Angielski i chiński
Klasyfikacja wyrobów medycznych na Tajwanie
TFDA klasyfikuje wyroby medyczne na 3 klasy w oparciu o ryzyko: Klasa I dla niskiego ryzyka, Klasa II dla umiarkowanego ryzyka i Klasa III dla wyrobów wysokiego ryzyka. Potrzeba wyrobu referencyjnego stanowi wyzwanie dla nowych wyrobów wchodzących na rynek. Zwiększony czas trwania procedur dla wyrobów Klasy II i III wymagających dokumentacji systemu jakości to kolejna związana z tym złożoność. Wszystkie importowane wyroby medyczne muszą uzyskać świadectwo rejestracji od TFDA.
| Klasa wyrobu | Ryzyko |
|---|---|
| Klasa I | Niskie ryzyko |
| Klasa II | Umiarkowane ryzyko |
| Klasa III | Wysokie ryzyko |
Reprezentacja Agenta na Tajwanie
Zagraniczni producenci bez fizycznego biura na Tajwanie powinni wyznaczyć Agenta Tajwańskiego jako warunek wstępny do wprowadzania wyrobów na rynek Tajwanu. Wyznaczenie organizacji zewnętrznej jako Agenta Tajwańskiego zamiast dystrybutora zapewnia elastyczność w poszukiwaniu wielu dystrybutorów w celu lepszej penetracji rynku. Agent Tajwański musi posiadać podmiot prawny zarejestrowany na Tajwanie, posiadający Certyfikat Licencji na Sprzedaż Produktów Farmaceutycznych.
Rejestracja wyrobów medycznych na Tajwanie
Zanim wyrób medyczny zostanie sprzedany na Tajwanie, wymagana jest rejestracja Dokumentacji Systemu Jakości (QSD) dla zakładu produkcyjnego, oprócz rejestracji wyrobu medycznego. Rejestracja QSD jest zwolniona jedynie dla wyrobów medycznych klasy I (niesterylnych). Licencja QSD (otrzymana po zatwierdzeniu rejestracji QSD) na Tajwanie jest podobna do Dobrej Praktyki Wytwarzania (GMP) dla wyrobów medycznych.
TFDA ogłosiła, że od 1 czerwca 2022 r. posiadacze licencji na wyroby medyczne klasy III są zobowiązani do przesyłania UDI i odpowiednich informacji o produkcie do bazy danych UDI (UDID). Producenci wyrobów medycznych są również zobowiązani do umieszczania UDI na etykiecie produktu. Ponadto, od 1 czerwca 2023 r., wyroby medyczne klasy II muszą spełniać odpowiednie przepisy dotyczące UDI.
Przebieg procesu
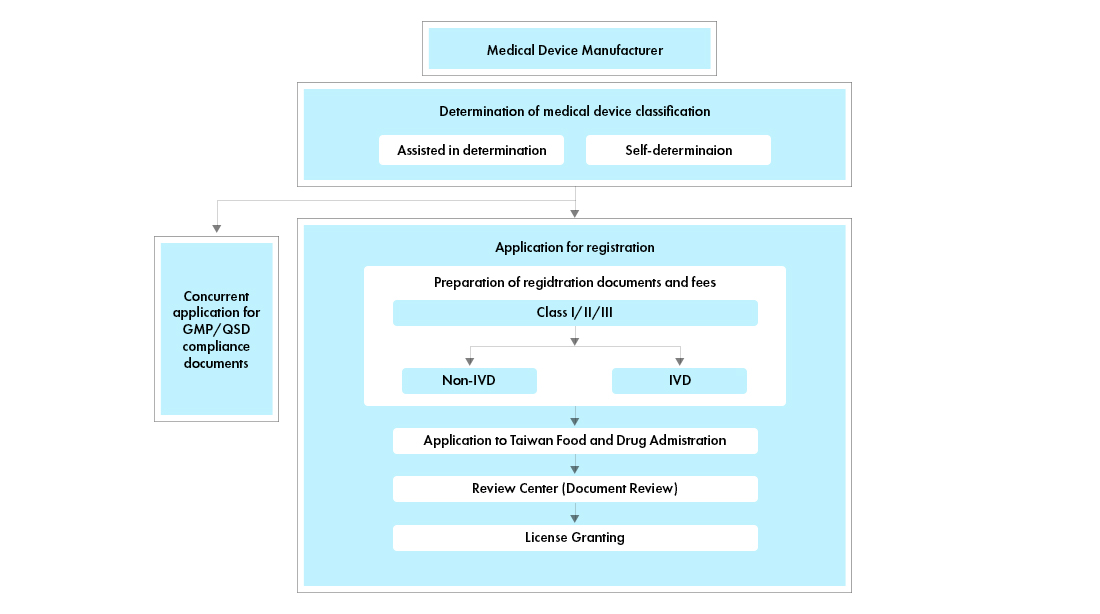
Zarządzanie cyklem życia wyrobu medycznego po zatwierdzeniu
Freyr wspiera zagranicznych producentów w zarządzaniu cyklem życia wyrobów medycznych End-to-End, w tym w działaniach po zatwierdzeniu, takich jak:
- Zarządzanie zmianami po zatwierdzeniu – modyfikacje istniejących zatwierdzeń wyrobów medycznych, takie jak dodawanie nowych wariantów, akcesoriów; dodawanie nowych wskazań do stosowania i inne
- Utrzymywanie zatwierdzeń i rejestracji poprzez terminowe uiszczanie opłat administracyjnych i rejestracyjnych
- Odnowienie licencji
- Pośrednictwo między TFDA a producentem
- Zarządzanie importem
Freyr specjalizuje się w zaspokajaniu potrzeb regulacyjnych wyrobów medycznych na Tajwanie. Dzięki rozległej sieci, Freyr pomaga w wyznaczeniu wiarygodnego lokalnego agenta, którego obecność jest niezwykle ważna przez cały okres Nadzoru po wprowadzeniu do obrotu. Nasi eksperci pomagają również w wyborze odpowiedniego urządzenia referencyjnego i istniejących zatwierdzeń z innych rynków w celu wsparcia wejścia nowego urządzenia na rynek.
Podsumowanie
| Klasa wyrobu | Ryzyko / Kryteria klasyfikacji | QMS | Rejestracja produktu |
|---|---|---|---|
| Klasa I | Niskie ryzyko | Zwolniony (niesterylne wyroby klasy I) | Tak |
| Klasa II | Umiarkowane ryzyko | QSD | Tak |
| Klasa III | Wysokie ryzyko | QSD | Tak |
Ekspertyza Freyr
- Należyta staranność regulacyjna
- Oficjalna Klasyfikacja
- Zgody QSD
- Rejestracja wyrobów
- Przedstawiciel prawny
- Wsparcie w zakresie etykietowania
- Wsparcie tłumaczeniowe
- Identyfikacja i kwalifikacja dystrybutora
- Nadzór po wprowadzeniu do obrotu
- Zarządzanie zmianami po zatwierdzeniu
- Odnowienie i przeniesienie licencji
- Złożenie dokumentów i kontakt


