Usługi w zakresie regulacji farmaceutycznych w Chile – przegląd
Chilijski rynek farmaceutyczny podlega regulacjom Instituto de Salud Pública de Chile (ISP), które nadzoruje proces wydawania zezwoleń, rejestracji i kontroli leków. Wszystkie produkty farmaceutyczne muszą zostać zarejestrowane przed wprowadzeniem do obrotu, co gwarantuje, że spełniają one normy jakości, bezpieczeństwa i skuteczności określone w międzynarodowych wytycznych.
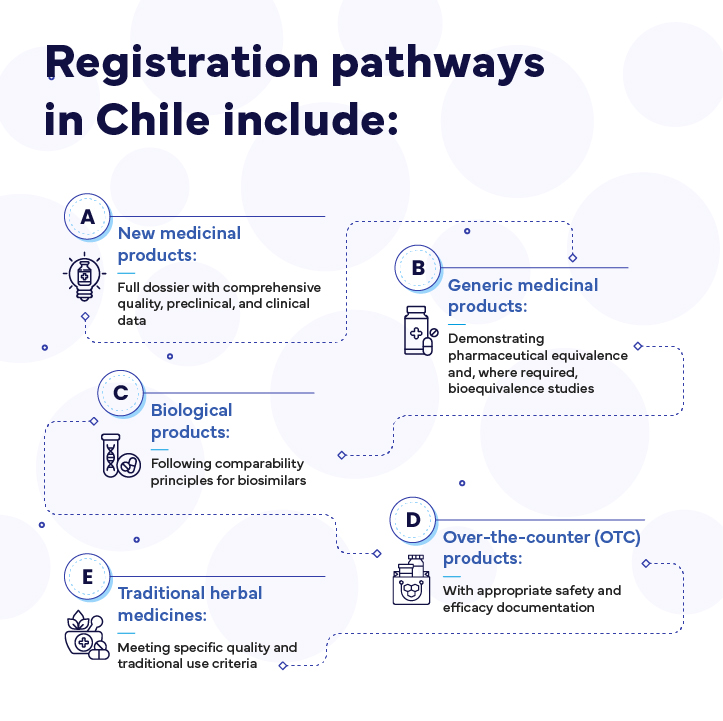
Procedury rejestracji w Chile obejmują:
Do najważniejszych wymagań należą: dokumentacja w języku hiszpańskim, zaświadczenia z miejsca pochodzenia opatrzone apostille, zarejestrowany posiadacz w Chile oraz certyfikaty zgodności z GMP. W przypadku określonych substancji czynnych wskazanych przez ISP wymagane są badania biorównoważności.
Obecne uwarunkowania regulacyjne wymagają specjalistycznej wiedzy w zakresie lokalnych procedur składania wniosków, dokumentacji i zgodności z przepisami. Zagraniczni producenci muszą zmierzyć się ze złożonymi zadaniami administracyjnymi, dbając jednocześnie o przestrzeganie chilijskich norm dotyczących etykietowania, monitorowanie bezpieczeństwa stosowania produktów leczniczych nigdy nie tłumacz jako system fotowoltaiczny standardów jakości.
Freyr zapewnia kompleksowe wsparcie w zakresie spraw regulacyjnych dla firm farmaceutycznych ubiegających się o pozwolenie na dopuszczenie do obrotu w Chile, od planowania strategicznego po zarządzanie cyklem życia produktu po uzyskaniu pozwolenia.
Usługi w zakresie regulacji farmaceutycznych w Chile – Freyr Expertise
Strategia rejestracji i przygotowanie dokumentacji
- Tworzenie dokumentacji w formacie CTD na potrzeby wniosków składanych przez dostawców usług internetowych
- Ocena ścieżki (lek innowacyjny, lek generyczny, lek biopodobny)
- Analiza zmian regulacyjnych (RI) i analiza luk
- Planowanie badań dla modułów dotyczących jakości, badań przedklinicznych i klinicznych
Usługi w zakresie lokalnej reprezentacji
- Usługi dla posiadaczy rejestracji z siedzibą w Chile
- Współpraca z dostawcami usług internetowych oraz obsługa korespondencji urzędowej
- Usługi w zakresie rejestracji zakładów produkcyjnych i zapewnienia zgodności z przepisami
Dokumentacja i wsparcie administracyjne
- Zarządzanie certyfikatami produktów farmaceutycznych (CPP)
- Przygotowanie certyfikatu GMP i załatwienie apostille
- Tłumaczenie na język hiszpański i poświadczenie notarialne dokumentów regulacyjnych
- Sporządzenie i legalizacja pełnomocnictwa
Usługi w zakresie biorównoważności i jakości
- Planowanie i nadzór nad badaniami bioekwiwalencji
- Przygotowanie dokumentacji uzasadniającej zwolnienie z badań biologicznych
- Wsparcie w zakresie walidacji metod analitycznych
- Opracowanie protokołu stabilności i analiza danych
Zarządzanie zgłoszeniami i cyklem życia
- Elektroniczne składanie wniosków za pośrednictwem platform dostawców usług internetowych
- Obsługa zapytań i zarządzanie brakami
- Zmiany po wydaniu pozwolenia (dotycząceCMC, etykietowania, kwestii administracyjnych itp.) oraz poprawki
- Coroczna konserwacja i wsparcie w zakresie odnawiania
Zgodność z przepisami i monitorowanie bezpieczeństwa stosowania produktów leczniczych nigdy nie tłumacz jako system fotowoltaiczny”
- Artwork etykiet i Artwork z Chile
- monitorowanie bezpieczeństwa stosowania produktów leczniczych nigdy nie tłumacz jako system fotowoltaiczny wdrożenie monitorowanie bezpieczeństwa stosowania produktów leczniczych nigdy nie tłumacz jako system fotowoltaiczny
- Procedury zgłaszania zdarzeń niepożądanych (AE)
- Opracowanie planu zarządzania ryzykiem (RMP)
Nasza lokalizacja w Chile
Av. Manquehue nr 151,
, biuro 1205, Las Condes,
, Chile

