Usługi audytu zgodności i walidacji w farmacji
Wykorzystaj dziesięcioletnie doświadczenie dzięki naszym usługom, realizowanym poprzez oceny zgodności, skrupulatne audyty i solidne procesy walidacji.
Przeglądaj tematy
- Czym jest zgodność, audyt i walidacja w farmacji?
- Jakie jest znaczenie zgodności, audytu i walidacji w przemyśle farmaceutycznym?
- Główne wyzwania w obszarze zgodności, audytu i walidacji.
- Czym są audyty GxP?
- Zrozumienie audytów zdalnych
- Czym jest Walidacja Systemów Komputerowych (CSV) i dlaczego jest to kluczowe w przemyśle farmaceutycznym?
- Czym różni się CSV od Computer System Assurance (CSA)
- Jakie są elementy programu CSA?
- Jak CSA przyczynia się do integralności danych w przemyśle farmaceutycznym?
- Jaką rolę odgrywa zgodność regulacyjna w CSA?
- Jak pomaga strategiczny partner w zakresie zgodności regulacyjnej?
- Dlaczego wybrać Freyr?
- Nasze usługi
Czym jest zgodność, audyt i walidacja w farmacji?
Ostatnia aktualizacja: wrzesień 2024
W sektorze farmaceutycznym procesy zgodności, audytu i walidacji są integralne, zapewniając przestrzeganie norm regulacyjnych, integralność danych oraz produkcję bezpiecznych i skutecznych produktów. Zgodność oznacza dostosowanie operacji do przepisów branżowych i wewnętrznych polityk. Audyty, czyli systematyczne przeglądy, weryfikują zgodność, identyfikują obszary do poprawy i łagodzą ryzyka. Walidacja gwarantuje, że systemy, procesy i sprzęt konsekwentnie spełniają z góry określone wymagania.
Firmy poszukują fachowego doradztwa, aby sprawnie funkcjonować na rynku. Liderzy branży umiejętnie zarządzają tymi procesami, zapewniając zgodność z globalnymi standardami bez uszczerbku dla skuteczności i bezpieczeństwa produktów. Wraz z ewolucją sektora farmaceutycznego strategiczne podejście do kwestii zgodności z przepisami, audytów i walidacji staje się kluczowe dla trwałego sukcesu. Dzięki przestrzeganiu tych procesów firmy spełniają wymogi regulacyjne oraz budują kulturę doskonałości i innowacyjności w tej dynamicznej i pełnej wyzwań branży.
Współpracuj z zaufanym partnerem, aby uzyskać strategiczne doradztwo i dopasowane rozwiązania, które umożliwią Twoim operacjom farmaceutycznym rozwój w dynamicznym środowisku regulacyjnym.

Jakie jest znaczenie zgodności, audytu i walidacji w przemyśle farmaceutycznym?
Zgodność, audyt i walidacja są kluczowymi elementami w przemyśle farmaceutycznym, zapewniając, że produkty są bezpieczne, skuteczne i wytwarzane zgodnie ze standardami regulacyjnymi.
- Zapewnia bezpieczeństwo i skuteczność produktu: Zgodność z przepisami zapewnia, że produkty farmaceutyczne spełniają rygorystyczne normy bezpieczeństwa i skuteczności przed wprowadzeniem na rynek. Obejmuje to rygorystyczne testy i procesy walidacji w celu potwierdzenia, że produkty działają zgodnie z przeznaczeniem i nie stanowią zagrożenia dla pacjentów.
- Utrzymywanie zgodności z przepisami: Regularne audyty i walidacja pomagają firmom przestrzegać złożonych i zmieniających się przepisów ustanowionych przez organy ds. zdrowia. Obejmuje to zgodność z Dobrą Praktyką Wytwarzania (GMP), Dobrą Praktyką Kliniczną (GCP) i innymi standardami branżowymi, zmniejszając ryzyko kar regulacyjnych i wycofań produktów.
- Zwiększa zapewnienie jakości: Procesy walidacji, w tym walidacje sprzętu i systemów, zapewniają, że procesy produkcyjne i testowe konsekwentnie wytwarzają produkty wysokiej jakości. Audyty weryfikują, czy te procesy są prawidłowo przestrzegane, co prowadzi do poprawy jakości i niezawodności produktu.
- Wspiera dostęp do rynku i buduje reputację: Skuteczne praktyki w zakresie zgodności z przepisami i walidacji ułatwiają dostęp do rynku poprzez wykazanie przestrzegania wymogów regulacyjnych. Wzmacnia to reputację i wiarygodność firmy, budując zaufanie wśród pracowników służby zdrowia, pacjentów i organów regulacyjnych.
- Ułatwia ciągłe doskonalenie: Audyty dostarczają wglądu w efektywność procesów i obszary wymagające poprawy, co prowadzi do lepszej kontroli jakości i praktyk operacyjnych. Ta ciągła ocena i dostosowywanie pomagają w utrzymaniu wysokich standardów oraz adaptacji do zmian w przepisach i najlepszych praktykach branżowych.
Główne wyzwania w obszarze zgodności, audytu i walidacji.
Obszar zgodności, audytu i walidacji stoi przed kilkoma poważnymi wyzwaniami, które mogą wpływać na zdolność firm farmaceutycznych do spełniania wymagań regulacyjnych oraz utrzymania wysokich standardów jakości i bezpieczeństwa:
| Wyzwanie | Opis |
|---|---|
| Zgodność regulacyjna | Firmy farmaceutyczne muszą przestrzegać rygorystycznych przepisów agencji takich jak FDA i EMA, które wymagają szczegółowej dokumentacji i środków kontroli jakości. Nieprzestrzeganie przepisów może prowadzić do surowych kar, w tym grzywien i wycofania produktów z rynku. |
| Kontrola dostępu i bezpieczeństwo | Kluczowe jest zapewnienie, że tylko upoważniony personel ma dostęp do wrażliwych obszarów i informacji. Wiąże się to z wdrażaniem zaawansowanych systemów kontroli dostępu i utrzymaniem cyberbezpieczeństwa przed zagrożeniami, co może być złożone i kosztowne. |
| Walidacja systemów komputerowych (CSV) | Walidacja systemów komputerowych używanych w środowiskach GxP jest niezbędna, ale często uciążliwa i słabo zdefiniowana. Proces ten wymaga znacznego czasu i zasobów, zwłaszcza gdy standardowe podejście jest stosowane bezkrytycznie. |
| Szkolenia i świadomość pracowników | Ciągłe programy szkoleniowe są niezbędne, aby pracownicy rozumieli protokoły zgodności i ich znaczenie. Niewystarczające szkolenia mogą prowadzić do niezgodności i błędów w procesach. |
| Dokumentacja i prowadzenie rejestrów | Utrzymywanie dokładnej i kompleksowej dokumentacji jest kluczowe dla zgodności. Niewystarczająca dokumentacja to częsty problem, który może prowadzić do uwag organów regulacyjnych i niepowodzeń podczas audytów. |
| Integralność danych | Zapewnienie integralności i dokładności danych jest kluczowe, zwłaszcza przy zarządzaniu dużymi ilościami informacji. Wyzwania obejmują ręczne przetwarzanie danych i potrzebę solidnych systemów zarządzania danymi. |
| Zarządzanie dostawcami | Korzystanie z usług zewnętrznych dostawców oprogramowania i usług wymaga dokładnej walidacji i kontroli zgodności. Zarządzanie tymi relacjami i zapewnienie, że spełniają one standardy regulacyjne, może być wyzwaniem. |
| Złożoność technologiczna | Rosnąca złożoność technologii, w tym systemów AI i Cloud-based, stwarza nowe wyzwania walidacyjne i wymaga ciągłego dostosowywania się do zmieniających się krajobrazów regulacyjnych. |
| Niewystarczająca kontrola jakości | Wiele firm farmaceutycznych zmaga się z utrzymaniem wysokich standardów jakości we wszystkich procesach, co może prowadzić do zanieczyszczeń, zanieczyszczeń krzyżowych i innych problemów jakościowych. |
| Ciągłe doskonalenie i monitorowanie | Regularne audyty i inspekcje są kluczowe dla identyfikacji słabych punktów w systemach zgodności. Jednak wiele organizacji nie wdraża proaktywnych działań na rzecz ciągłego doskonalenia. |
- Zmieniające się przepisy: Nadzorowanie szybko zmieniających się przepisów i wytycznych w różnych regionach może być wyzwaniem. Firmy farmaceutyczne muszą stale aktualizować swoje praktyki zgodności, aby dostosować się do nowych lub zmienionych standardów regulacyjnych, co może wymagać znacznych zasobów i dostosowań.
- Złożoność globalnych standardów: Poruszanie się po zróżnicowanych i złożonych wymaganiach regulacyjnych różnych krajów i regionów stanowi dodatkowe wyzwanie. Każda jurysdykcja może mieć własny zestaw zasad i standardów, co utrudnia osiągnięcie spójnej zgodności na rynkach globalnych.
- Integralność i bezpieczeństwo danych: Zapewnienie integralności i bezpieczeństwa danych w całym procesie zgodności, audytu i walidacji jest kluczowe. Firmy muszą wdrożyć solidne systemy i kontrole, aby chronić przed naruszeniami danych, manipulacją lub niedokładnościami, które mogą mieć poważne konsekwencje dla zatwierdzenia produktu i bezpieczeństwa pacjentów.
- Ograniczenia Zasobów: Ograniczone zasoby, w tym czas, personel i budżet, mogą utrudniać skuteczność działań związanych z zgodnością i audytami. Firmy często mają trudności z pogodzeniem wymagań dotyczących utrzymania zgodności z potrzebą alokacji zasobów na inne kluczowe funkcje biznesowe.
- Zarządzanie dokumentacją i prowadzenie rejestrów: Właściwa dokumentacja i prowadzenie rejestrów są niezbędne do wykazania zgodności i przeprowadzania skutecznych audytów. Jednak zarządzanie ogromnymi ilościami dokumentacji, zapewnienie jej dokładności i utrzymanie dostępności może być wyzwaniem, zwłaszcza w środowisku silnie regulowanym.
- Integracja nowych technologii: Włączanie innowacyjnych technologii do istniejących procesów zgodności i walidacji może być złożone. Chociaż technologie takie jak automatyzacja i AI (sztuczna inteligencja) oferują znaczne korzyści, ich integracja musi być starannie zarządzana, aby zapewnić zgodność z wymaganiami regulacyjnymi i nie wprowadzać nowych zagrożeń.
- Szkolenia i kompetencje: Kluczowe jest zapewnienie, aby personel był odpowiednio przeszkolony i kompetentny w zakresie procesów zgodności, audytu i walidacji. Ciągłe programy szkoleniowe są niezbędne, aby personel był na bieżąco ze zmianami regulacyjnymi i najlepszymi praktykami, co może być zasobochłonne.
- Reagowanie na ustalenia audytu: Skuteczne reagowanie i korygowanie problemów zidentyfikowanych podczas audytów może być wyzwaniem. Firmy muszą niezwłocznie wdrażać działania korygujące i zapobiegawcze, jednocześnie dbając o to, aby działania te nie zakłócały bieżących operacji ani nie wpływały na jakość produktu.
- Równoważenie zgodności z innowacjami: Utrzymanie równowagi między przestrzeganiem rygorystycznych przepisów a dążeniem do innowacji może być trudne. Firmy muszą poruszać się po krajobrazie regulacyjnym, jednocześnie kontynuując rozwój i wprowadzanie nowych produktów i technologii.
- Zapewnienie spójności w działaniach: Utrzymywanie spójności w praktykach zgodności i procesach walidacji w różnych działach, placówkach i na różnych etapach cyklu życia produktu jest kluczowe, ale stanowi wyzwanie. Zmienność w praktykach może prowadzić do niezgodności i problemów z jakością.
Czym są audyty GxP?
Czym jest niezależny audyt zgodności GxP i kto go przeprowadza?
Audyt GxP to proces mający na celu zapewnienie, że przedsiębiorstwa przestrzegają ustalonych norm jakości, bezpieczeństwa i zgodności z przepisami. Może on obejmować różne aspekty produktów i procesów farmaceutycznych, takie jak dobra praktyka laboratoryjna (GLP), dobra praktyka kliniczna (GCP), dobra praktyka wytwarzania (GMP) oraz dobra monitorowanie bezpieczeństwa stosowania produktów leczniczych nigdy nie tłumacz jako system fotowoltaiczny (GVP).
Audyt ocenia stopień zgodności z obowiązującymi przepisami, regulacjami, wytycznymi i standardowymi procedurami operacyjnymi (SOP) oraz wskazuje luki, zagrożenia i możliwości wprowadzenia ulepszeń. W ramach audytu przedstawiane są również zalecenia i działania naprawcze mające na celu uwzględnienie ustaleń oraz udoskonalenie systemów jakości.
Korzyści z audytu GxP obejmują:
- Dostarczanie bezstronnej i obiektywnej oceny systemów jakości oraz poziomu zgodności.
- Wzmacnianie zaufania organów regulacyjnych, klientów, dostawców i innych zainteresowanych stron.
- Zmniejszenie prawdopodobieństwa i dotkliwości kontroli regulacyjnych, uwag i sankcji.
- Poprawa jakości, bezpieczeństwa i skuteczności produktów oraz procesów.
- Zwiększenie wydajności i skuteczności operacji oraz zmniejszenie kosztów i błędów.
- Wspieranie ciągłego doskonalenia i innowacji produktów oraz procesów.
Audyt GxP jest przeprowadzany przez wykwalifikowanego i doświadczonego audytora lub zespół audytorów posiadających odpowiednią wiedzę, umiejętności i kwalifikacje w przemyśle farmaceutycznym oraz w konkretnym obszarze GxP. Audytor lub zespół audytowy powinien być niezależny od audytowanej firmy i przestrzegać profesjonalnych standardów oraz zasad etycznych audytu. Powinni również stosować odpowiednie narzędzia i metody do przeprowadzenia audytu, takie jak listy kontrolne, wywiady, obserwacje, przeglądy dokumentów, próbkowanie, testowanie itp. Freyr oferuje kompleksowe (End-to-End) wsparcie w audytach GxP. Jako lider branży, nasi eksperci sprawią, że Twoja droga do zgodności będzie płynna.
Ramy regulacyjne dla audytów GxP
Zgodność z GxP to zbiór przepisów, które regulują różne branże podlegające regulacjom, w tym farmaceutyczną, wyrobów medycznych, spożywczą, napojów i biotechnologiczną. Głównym celem zgodności z GxP jest utrzymanie jakości produktów i zapewnienie bezpieczeństwa publicznego. Oto kilka kluczowych kwestii:
- Przegląd zgodności z GxP:
- GxP obejmuje kilka standardów, w tym Dobrą Praktykę Laboratoryjną (GLP), Dobrą Praktykę Kliniczną (GCP), Dobrą Praktykę Wytwarzania (GMP) i Dobrą Praktykę monitorowania bezpieczeństwa stosowania produktów leczniczych (GVP).
- Normy te zapewniają, że produkty są dokładnie testowane, wytwarzane i obsługiwane przez cały cykl ich życia.
- Międzynarodowa Konferencja Harmonizacji (ICH):
- ICH dostarcza wytycznych dotyczących zgodności z GxP.
- The Wytyczne Dobrej Praktyki Wytwarzania ICH Q7A konkretnie dotyczą praktyk wytwarzania aktywnych składników farmaceutycznych (APIs).
- Inspekcje FDA:
- Amerykańska Agencja Żywności i Leków (FDA) przeprowadza inspekcje w celu oceny zgodności z przepisami GxP.
- Inspekcje te oceniają zgodność z określonymi przepisami i wytycznymi FDA.
- Inspekcje Health Canada:
- Health Canada, organ regulacyjny w Kanadzie, przeprowadza również inspekcje w celu zapewnienia zgodności z GxP.
- Inspekcje te koncentrują się na różnych aspektach, w tym na produkcji, kontroli jakości i dystrybucji.
- Kryteria oceny dla audytów GxP:
Zgodność w niezależnych audytach GxP jest zazwyczaj oceniana na podstawie szeregu kryteriów, które mogą obejmować:
- Wymogi regulacyjne: Zgodność ze szczegółowymi przepisami, wytycznymi i prawem mającymi zastosowanie w obszarze GxP (np. przepisy FDA, wytyczne ICH lub normy ISO).
- Systemy jakości: Ocena systemów zarządzania jakością, praktyk dokumentacyjnych i prowadzenia rejestrów.
- Walidacja procesów: Weryfikacja, czy procesy są zwalidowane i spełniają z góry określone kryteria.
- Szkolenia i kompetencje: Ocena szkoleń i kwalifikacji personelu.
- Zarządzanie Ryzykiem: Identyfikacja i łagodzenie ryzyka związanego z jakością i bezpieczeństwem produktu.
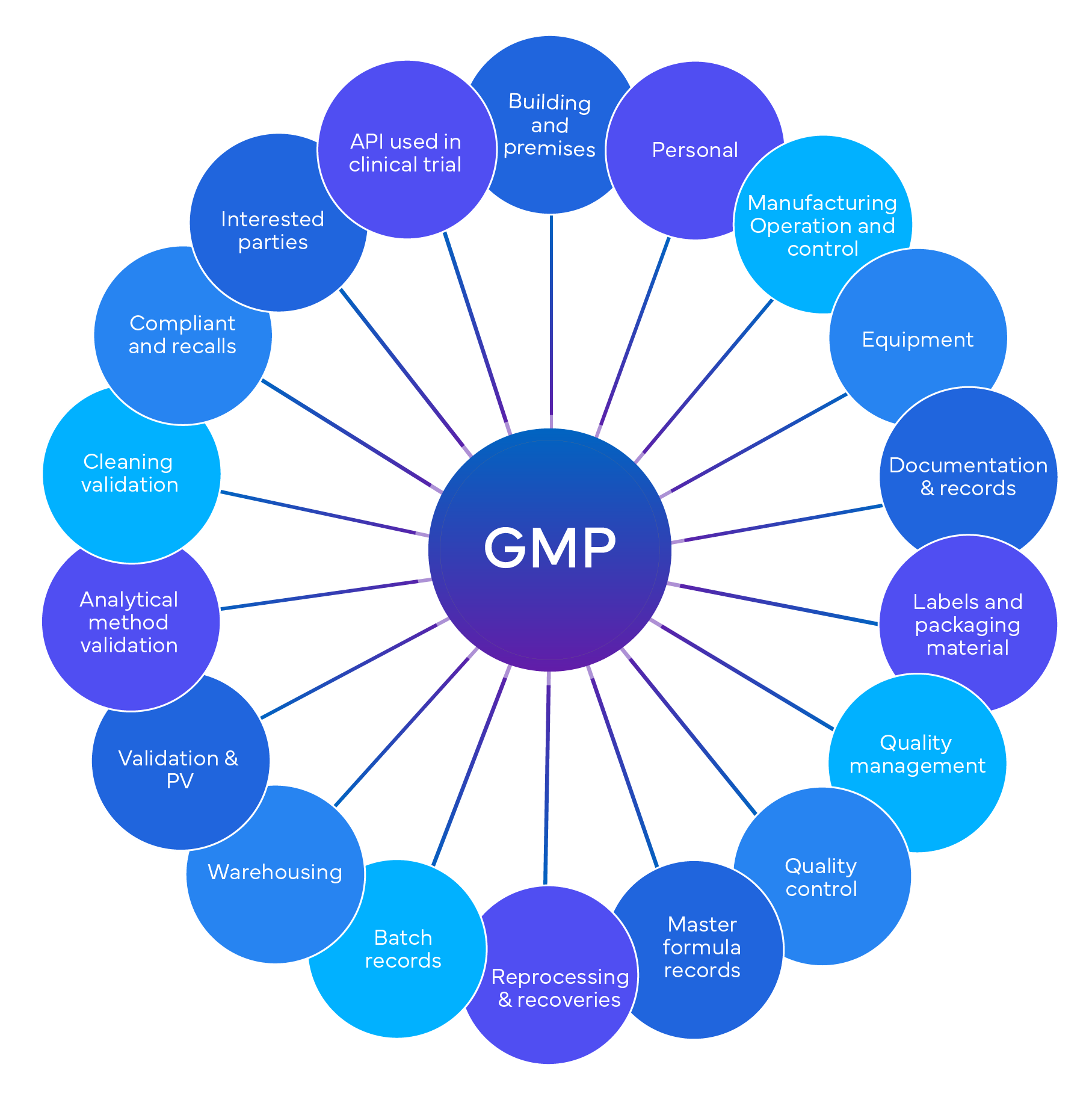
Dowiedz się, jak sprawdzony ekspert w dziedzinie spraw regulacyjnych może pomóc Ci stworzyć idealne ramy audytu GxP dostosowane do Twoich potrzeb i pomóc Ci pozostać w zgodzie z globalnymi przepisami.
Korzyści z przeprowadzania audytów zgodności GxP
Audyty GxP przynoszą liczne korzyści każdej organizacji. Po pierwsze, zapewniają bezstronną i niezależną ocenę ryzyka i zgodności w organizacji, umożliwiając firmom identyfikację obszarów niezgodności lub potencjalnego ryzyka, które mogłyby zostać przeoczone podczas audytów wewnętrznych. Audyty te są kluczowe dla zapewnienia, że firmy przestrzegają określonych standardów jakości, bezpieczeństwa i zgodności regulacyjnej.
| Aspekt | Opis |
|---|---|
| Kompleksowy przegląd | Dokładna ocena przeprowadzona przez wykwalifikowaną stronę trzecią w celu identyfikacji obszarów niezgodności. |
| Standardy regulacyjne | Przestrzeganie standardów GxP (dobrych praktyk), takich jak GMP, GCP i GLP. |
| Dostosowany zakres | Dostosowany zakres audytu oparty na konkretnych produktach i procesach. |
| Wykwalifikowani audytorzy | Doświadczeni audytorzy zaznajomieni z przepisami. |
| Ramy regulacyjne | Zgodnie z wytycznymi ICH Q7A, FDA i Health Canada. |
| Korzyści | Bezstronne oceny, zapobieganie ryzyku, utrzymanie jakości i skalowalność. |
Oto kilka kluczowych kwestii dotyczących audytów zgodności z GxP:
- Kompleksowy przegląd: Audyty GxP obejmują dokładny proces przeglądu przeprowadzany przez wykwalifikowaną organizację zewnętrzną lub konsultanta. Celem jest zidentyfikowanie wszelkich obszarów niezgodności w organizacji i przedstawienie zaleceń dotyczących poprawy.
- Standardy regulacyjne: Przepisy weryfikowane podczas tych audytów są określone przez standardy GxP (dobre praktyki), takie jak Dobre Praktyki Wytwarzania (GMP), Dobrej Praktyki Klinicznej (GCP) i Dobrej Praktyki Laboratoryjnej (GLP). Standardy te zapewniają, że produkty, usługi i procesy konsekwentnie spełniają odpowiednie wymogi regulacyjne.
- Dostosowany zakres: Zakres niezależnego audytu jest dostosowany do konkretnych produktów i procesów organizacji. Może obejmować zarządzanie personelem, zarządzanie obiektami, prowadzenie dokumentacji, zapewnienie i kontrolę jakości, projektowanie produktów i procesów oraz operacje techniczne.
- Wykwalifikowani audytorzy: Audyt musi być przeprowadzony przez wykwalifikowanego i doświadczonego audytora, który zna obowiązujące przepisy i posiada niezbędną wiedzę do skutecznej oceny procedur i procesów organizacji.
- Ramy regulacyjne: Audyty GxP są zgodne z ramami takimi jak Wytyczne Dobrej Praktyki Wytwarzania ICH Q7A (International Conference on Harmonization), inspekcje FDA oraz inspekcje Health Canada. Ramy te dostarczają wytycznych dotyczących podstawowych wymogów w zakresie produkcji, zapewnienia jakości, dystrybucji i innych kluczowych działań związanych z bezpieczną produkcją produktów.
- Korzyści: Audyty GxP oferują bezstronne oceny, pomagają zapobiegać problemom z niezgodnością, utrzymywać standardy jakości i zapewniać odpowiedzialność. Zlecanie tych audytów na zewnątrz zapewnia dostęp do wiedzy specjalistycznej, obiektywności, efektywności kosztowej i skalowalności, jednocześnie pozwalając firmom skupić się na kluczowych kompetencjach.
Jeśli szukasz rozwiązań w zakresie zgodności z GxP, rozważ Freyr. Specjalizujemy się w zgodności regulacyjnej, zapewnieniu jakości i bezpieczeństwie w całej branży nauk przyrodniczych. Dzięki naszemu doświadczeniu możesz zapewnić przestrzeganie standardów GxP, usprawnić procesy i utrzymać wysoką jakość produktów i usług.
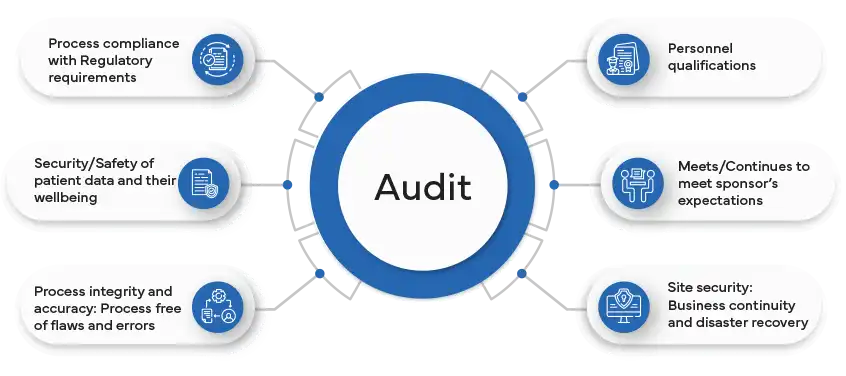
Wskazówki, jak przygotować swoją organizację do audytu
Przygotowanie organizacji do audytu to strategiczny proces, który wymaga skrupulatnego planowania i proaktywnego podejścia. Po pierwsze, upewnij się, że wszystkie rejestry, dokumentacja i odpowiednie pliki są uporządkowane i łatwo dostępne. Dobrze zorganizowany system archiwizacji ułatwia płynniejszy proces audytu i pozytywnie wpływa na profesjonalizm Twojej organizacji.
Po drugie, przeprowadź wewnętrzny audyt wstępny, aby zidentyfikować potencjalne obszary wymagające uwagi. Ta samoocena pozwala na rozwiązanie wszelkich problemów lub rozbieżności przed audytem zewnętrznym. Proaktywne rozwiązywanie problemów świadczy o zaangażowaniu w zgodność i przejrzystość.
Po trzecie, skutecznie komunikuj się i współpracuj z zespołem audytowym. Zapewnij niezbędne informacje, dostęp do odpowiedniego personelu oraz sprzyjające środowisko pracy. Jasna komunikacja pomaga budować pozytywne relacje z audytorami, sprzyjając atmosferze współpracy podczas procesu audytu.
Na koniec, upewnij się, że Twój zespół jest dobrze przeszkolony i świadomy procesu audytu. Edukuj pracowników w zakresie ich ról, obowiązków oraz znaczenia zgodności z przepisami. Wdrażając kulturę gotowości i współpracy, Twoja organizacja może przechodzić audyty z pewnością siebie i profesjonalizmem.
Zrozumienie audytów zdalnych
Czym jest audyt zdalny w przemyśle farmaceutycznym i czym różni się od tradycyjnych audytów na miejscu?
Audyt zdalny w branży farmaceutycznej to kompleksowa ocena procesów, obiektów i systemów danej firmy, przeprowadzana przez organy regulacyjne lub audytorów bez fizycznej obecności na miejscu. Audyt ten odbywa się przy użyciu narzędzi komunikacji cyfrowej, oprogramowania do współpracy oraz zdalnego dostępu do odpowiednich dokumentów i systemów. Jego celem jest zapewnienie zgodności z normami regulacyjnymi, ocena systemów zarządzania jakością oraz weryfikacja przestrzegania zasad dobrej praktyki wytwarzania (GMP), dobrej praktyki klinicznej (GCP) lub innych obowiązujących przepisów.
Różnica między audytami zdalnymi a tradycyjnymi audytami na miejscu polega na braku fizycznej obecności podczas audytu zdalnego. Zamiast odwiedzać siedzibę firmy, audytorzy polegają na wirtualnych interakcjach, dokumentacji elektronicznej i zdalnym dostępie do systemów. Takie podejście oferuje elastyczność i wydajność, umożliwiając przeprowadzanie audytów niezależnie od odległości geograficznych i ograniczeń w podróżowaniu. Należy jednak rozwiązać takie wyzwania, jak ograniczona bezpośrednia obserwacja obiektów i potencjalne obawy dotyczące cyberbezpieczeństwa, aby zapewnić skuteczność audytów zdalnych.
Pomimo różnic, cele zarówno audytów zdalnych, jak i tradycyjnych pozostają takie same – weryfikacja zgodności, identyfikacja obszarów do poprawy oraz zapewnienie jakości i bezpieczeństwa produktów farmaceutycznych. Wybór między audytami zdalnymi a stacjonarnymi zależy od takich czynników jak charakter audytu, wymogi regulacyjne oraz możliwości firmy w zakresie przeprowadzenia dokładnej oceny za pomocą środków zdalnych.
Freyr wykorzystuje dziesięcioletnie doświadczenie, aby dostarczać niezrównane rozwiązania regulacyjne, zapewniając zgodność i sukces w dynamicznym środowisku farmaceutycznym.
Odkryj doskonałość regulacyjną z nami – Twoim strategicznym partnerem w osiąganiu sukcesu w zakresie zgodności w stale zmieniającej się branży farmaceutycznej. Skontaktuj się z nami, aby bezproblemowo poruszać się po złożonościach regulacyjnych.
Jakie wyzwania mogą pojawić się podczas audytów zdalnych i jak się je rozwiązuje, aby zapewnić dokładne oceny?
Podczas zdalnych audytów może pojawić się kilka wyzwań, ale organizacje mogą podjąć kroki w celu ich rozwiązania i zapewnienia dokładnych ocen. Oto kluczowe wyzwania i ich potencjalne rozwiązania:
- Budowanie kluczowych relacji z interesariuszami audytu:
- Wyzwanie: Praca zdalna może utrudniać rozwój silnych relacji z interesariuszami audytu.
- Rozwiązanie: Regularne wirtualne spotkania, otwarta komunikacja i aktywne zaangażowanie mogą pomóc w budowaniu i utrzymywaniu relacji. Korzystaj z połączeń wideo, aby nawiązać osobisty kontakt.
- Inwestowanie w technologię do pracy zdalnej:
- Wyzwanie: Audyty zdalne w dużym stopniu polegają na technologii, a nieodpowiednie narzędzia mogą utrudniać efektywność.
- Rozwiązanie: Zainwestuj w solidne oprogramowanie do zarządzania audytami, bezpieczne platformy komunikacyjne i narzędzia do współpracy. Upewnij się, że audytorzy posiadają niezbędny sprzęt i oprogramowanie.
- Rozwój pracowników i promowanie pozytywnej kultury pracy zdalnej:
- Wyzwanie: Praca zdalna może prowadzić do izolacji i utrudniać rozwój zawodowy.
- Rozwiązanie: Zapewnij wirtualne szkolenia, mentoring i możliwości rozwoju umiejętności. Wspieraj pozytywną kulturę poprzez działania integracyjne, docenianie i regularne spotkania kontrolne.
- Rozwijanie świadomego i adaptacyjnego sposobu myślenia:
- Wyzwanie: Audytorzy zdalni muszą dostosować się do zmieniających się okoliczności i pozostać skoncentrowani.
- Rozwiązanie: Zachęcaj do elastyczności, zdolności adaptacji i nastawienia na rozwój. Szkol audytorów, aby radzili sobie z nieoczekiwanymi sytuacjami i dostosowywali swoje podejście w razie potrzeby.
Freyr jest zaufanym partnerem w zakresie zgodności regulacyjnej i rozwiązań bezpieczeństwa dla branży life science. Dzięki głębokiej wiedzy branżowej, innowacyjnej technologii i globalnemu zasięgowi, Freyr umożliwia organizacjom płynne poruszanie się w złożonym środowisku regulacyjnym. Zapoznaj się z naszymi usługami i skontaktuj się z nami już dziś, aby usprawnić swoją drogę do zgodności.
Jak Freyr jest lepiej przygotowany, aby pomóc Państwu w zdalnych audytach?
Freyr, z dziesięcioletnim doświadczeniem, doskonale radzi sobie w ułatwianiu płynnych audytów zdalnych dla przemysłu farmaceutycznego. Wykorzystując zaawansowane technologie i głębokie zrozumienie wymagań regulacyjnych, Freyr zapewnia dokładny i efektywny proces audytu, rozwiązując wyzwania takie jak ograniczona obecność fizyczna i obawy dotyczące cyberbezpieczeństwa.
Nasz dedykowany zespół ekspertów ds. regulacji sprawnie wykorzystuje innowacyjne rozwiązania cyfrowe, zapewniając kompleksową wirtualną ocenę Państwa procesów, obiektów i dokumentacji. Nasze udokumentowane osiągnięcia w zakresie audytów zdalnych odzwierciedlają nasze zaangażowanie w dostarczanie niezawodnych i skutecznych rozwiązań regulacyjnych, dostosowanych do zmieniających się potrzeb branży farmaceutycznej. Z Freyr zyskują Państwo zaufanego partnera, który rozumie złożoność audytów zdalnych i stosuje proaktywne oraz współpracujące podejście, aby usprawnić Państwa drogę do zgodności.
Czym jest Walidacja Systemów Komputerowych (CSV) i dlaczego jest to kluczowe w przemyśle farmaceutycznym?
Walidacja systemów komputerowych (CSV) to kluczowy proces w przemyśle farmaceutycznym, który zapewnia integralność, niezawodność i zgodność systemów skomputeryzowanych używanych do różnych celów. Przyjrzyjmy się szczegółom:
- Definicja i Cel:
- CSV to udokumentowany proces, który zapewnia, że system komputerowy będzie generować informacje lub dane spełniające z góry określone wymagania.
- Jego głównym celem jest walidacja i weryfikacja, czy systemy komputerowe konsekwentnie działają zgodnie z przeznaczeniem, zachowując dokładność, niezawodność i bezpieczeństwo danych.
- Znaczenie w farmacji:
- Zgodność z przepisami: Przemysł farmaceutyczny działa w oparciu o ścisłe przepisy (takie jak Dobre Prakaktyki Wytwarzania, czyli GMP), aby zapewnić jakość, bezpieczeństwo i skuteczność produktów.
- Integralność danych: Dokładne i wiarygodne dane są kluczowe dla rozwoju leków, badań klinicznych, produkcji i dystrybucji.
- Łagodzenie Ryzyka: CSV pomaga identyfikować i łagodzić ryzyka związane z systemami komputerowymi, zapobiegając błędom, utracie danych i niezgodnościom.
- Bezpieczeństwo pacjenta: Prawidłowo zwalidowane systemy przyczyniają się do bezpieczeństwa pacjentów poprzez zapewnienie stałej jakości i zgodności ze standardami.
- Kluczowe aspekty CSV:
- Definiowanie Wymagań: Jasne określenie wymagań systemowych, funkcjonalności i oczekiwań użytkowników.
- Projektowanie i konfiguracja: Opracowanie i konfiguracja systemu zgodnie ze specyfikacjami.
- Testowanie i kwalifikacja: Rygorystyczne testowanie (w tym testy jednostkowe, testy integracyjne i testy akceptacyjne użytkownika) w celu weryfikacji wydajności systemu.
- Dokumentacja: Utrzymywanie kompleksowej dokumentacji przez cały cykl życia systemu.
- Kontrola zmian: Zarządzaj zmianami w systemie, zapewniając, że nie naruszą jego integralności.
- Wyzwania rozwiązywane przez CSV:
- Integralność danych: Zapobieganie nieautoryzowanemu dostępowi, uszkodzeniu danych lub manipulacji.
- Bezpieczeństwo systemu: Ochrona przed zagrożeniami cybernetycznymi i nieautoryzowanymi modyfikacjami.
- Ścieżka audytu: Utrzymuj niezmywalną elektroniczną ścieżkę danych dla audytów regulacyjnych.
- Utrzymanie walidacji: Regularnie przeglądaj i aktualizuj walidację, aby dostosować ją do zmian w systemie.
Czym różni się CSV od Computer System Assurance (CSA)?
Walidacja systemów komputerowych (CSV) i Zapewnienie Systemów Komputerowych (CSA) reprezentują odrębne podejścia do zapewnienia integralności i zgodności skonputeryzowanych systemów w przemyśle farmaceutycznym. CSV, długoletnia praktyka, koncentruje się głównie na fazie walidacji cyklu życia systemu, zapewniając, że systemy oprogramowania spełniają wymagania regulacyjne poprzez z góry określone protokoły. Z drugiej strony, CSA przyjmuje bardziej ekspansywne i dynamiczne podejście, obejmujące cały cykl życia skonputeryzowanego systemu, od rozwoju i wdrożenia, poprzez użytkowanie operacyjne, aż do ostatecznego wycofania.
CSV odpowiada na potrzebę rygorystycznych procesów walidacji, kładąc nacisk na podejścia oparte na ryzyku w celu identyfikacji i łagodzenia potencjalnych problemów. Jednakże, krajobraz farmaceutyczny ewoluuje, co sprzyja pojawieniu się CSA jako bardziej kompleksowej strategii. CSA rozszerza swoje działania poza walidację, adaptując zwinne metodologie i włączając ciągłe monitorowanie przez cały cykl życia systemu. Ta holistyczna perspektywa pozwala organizacjom proaktywnie zarządzać ryzykiem, zwłaszcza w obszarze cyberbezpieczeństwa i integralności danych, co jest zgodne z rosnącym naciskiem branży na technologię i bezpieczeństwo danych.
Elastyczność podejścia CSA stanowi cenną zaletę w szybko zmieniającym się otoczeniu regulacyjnym. Podczas gdy CSV opiera się na tradycyjnych praktykach walidacyjnych, CSA dostosowuje się do ewoluujących oczekiwań organów regulacyjnych. Wykracza ono poza okresowe działania walidacyjne, obejmując ciągłe monitorowanie, analizę danych w czasie rzeczywistym oraz proaktywne strategie zarządzania ryzykiem, aby zapewnić stałą zgodność z przepisami i optymalną wydajność. W miarę jak przemysł farmaceutyczny przechodzi transformację cyfrową, zrozumienie niuansów między CSV a CSA staje się niezbędne dla firm, które chcą utrzymać przewagę w zakresie zgodności z przepisami i integralności systemów.
W tym kontekście Freyr, dzięki swojemu bogatemu doświadczeniu i wiedzy, jest dobrze przygotowany, aby prowadzić firmy farmaceutyczne przez złożoności zarówno CSV, jak i CSA, oferując dopasowane rozwiązania, które sprostają zmieniającym się wymaganiom zgodności regulacyjnej i postępu technologicznego.
Jakie są elementy programu CSA?
Zapewnienie jakości oprogramowania komputerowego (CSA) to nowoczesne podejście, które zwiększa niezawodność, bezpieczeństwo i zgodność w systemach skomputeryzowanych. Przyjrzyjmy się jego elementom i długoterminowym korzyściom:
- Podejście Oparte na Ryzyku:
- Komponent: CSA koncentruje się na ocenie i zarządzaniu ryzykiem.
- Znaczenie: Identyfikacja krytycznych obszarów pomaga efektywnie alokować wysiłki walidacyjne.
- Nieskryptowane testowanie:
- Komponent: CSA obejmuje testy nieskryptowane wykraczające poza tradycyjne przypadki testowe oparte na skryptach.
- Znaczenie: Testowanie bez scenariusza naśladuje rzeczywiste scenariusze, ujawniając ukryte problemy.
- Ciągłe monitorowanie wydajności:
- Komponent: CSA obejmuje ciągłe monitorowanie wydajności systemu.
- Znaczenie: Wczesne wykrywanie anomalii zapobiega awariom systemu i problemom z integralnością danych.
- Nadzór nad danymi:
- Komponent: CSA kładzie nacisk na jakość i integralność danych.
- Znaczenie: Zapewnia dokładne dane do podejmowania decyzji i zgodności.
- Zewnętrzne działania walidacyjne:
- Komponent: CSA współpracuje z dostawcami oprogramowania w celu zewnętrznej walidacji.
- Znaczenie: Niezależna walidacja zwiększa zaufanie i zmniejsza stronniczość.
- Przejście z CSV na CSA:
- Początkowe kroki:
- Zrozumienie zasad CSA.
- Ocena istniejących systemów pod kątem ryzyka.
- Priorytetyzuj kluczowe funkcjonalności.
- Korzyści:
- Zmniejszone obciążenie pracą walidacyjną.
- Elastyczna reakcja na zmiany.
- Zwiększona niezawodność systemu.
- Początkowe kroki:
- Długoterminowa niezawodność systemu:
- CSA zapewnia:
- Elastyczność: Systemy ewoluują bez uszczerbku dla niezawodności.
- Bezpieczeństwo: Ochrona przed zagrożeniami cybernetycznymi.
- Zgodność: Ciągłe dostosowywanie się do przepisów.
- Jakość: Spójna jakość danych i produktów.
- CSA zapewnia:
Jak CSA przyczynia się do integralności danych w przemyśle farmaceutycznym?
CSA wspiera integralność danych w przemyśle farmaceutycznym, zapewniając dokładność, spójność i niezawodność danych przez cały cykl życia systemu. W przeciwieństwie do tradycyjnych podejść, CSA przyjmuje holistyczną strategię, która wykracza poza walidację, aktywnie zajmując się potencjalnymi wyzwaniami i rozbieżnościami, które mogą pojawić się z czasem.
Jednym z wkładów CSA w integralność danych są jego możliwości ciągłego monitorowania. Zamiast polegać wyłącznie na okresowych działaniach walidacyjnych, CSA obejmuje analizę danych w czasie rzeczywistym i proaktywne środki zarządzania ryzykiem. Takie podejście umożliwia organizacjom wykrywanie i rozwiązywanie potencjalnych rozbieżności w danych, zapobiegając gromadzeniu się niedokładności w czasie. Nacisk CSA na dynamiczny i adaptacyjny model cyklu życia zapewnia, że integralność danych pozostaje stałym priorytetem, zgodnie z oczekiwaniami regulacyjnymi.
Aby zapobiec rozbieżnościom danych w czasie, CSA wdraża kilka strategicznych środków. Po pierwsze, stosuje solidne procesy kontroli zmian, skrupulatnie dokumentując wszelkie modyfikacje systemów skomputeryzowanych lub procesów, które mogłyby wpłynąć na integralność danych. Regularnie przeprowadzane są audyty i oceny systemów w celu identyfikacji i naprawy potencjalnych problemów, zanim się nasilą. Ponadto, CSA podkreśla znaczenie programów szkoleniowych i uświadamiających dla użytkowników, aby zapewnić, że personel rozumie znaczenie utrzymania integralności danych i przestrzega najlepszych praktyk.
Podsumowując, proaktywne i kompleksowe podejście CSA do integralności danych wyróżnia je jako strategiczne rozwiązanie w przemyśle farmaceutycznym. Dzięki włączeniu ciągłego monitorowania, zarządzania ryzykiem i rygorystycznych środków kontroli zmian, CSA utrzymuje integralność danych i zapewnia, że firmy farmaceutyczne są dobrze przygotowane do poruszania się w zmieniającym się krajobrazie oczekiwań regulacyjnych. Ponieważ organizacje dążą do utrzymania najwyższych standardów w zakresie integralności danych, CSA jawi się jako kluczowy sojusznik w ich podróży, dostosowując się do trendów branżowych i postępów regulacyjnych.
Dla organizacji poszukujących wskazówek dotyczących wdrażania skutecznych strategii CSA, Freyr jest niezawodnym partnerem oferującym dostosowane rozwiązania, aby sprostać wyjątkowym wyzwaniom krajobrazu farmaceutycznego.
Jaką rolę odgrywa zgodność regulacyjna w CSA?
Zgodność regulacyjna jest podstawą CSA, zapewniając, że firmy farmaceutyczne przestrzegają ewoluujących standardów i wytycznych przez cały cykl życia systemu. W przeciwieństwie do tradycyjnego podejścia Walidacji Systemów Komputerowych (CSV), CSA kładzie nacisk na ciągłą zgodność i zdolność adaptacji do zmieniających się krajobrazów regulacyjnych. W miarę przechodzenia firm z CSV na CSA, bycie na bieżąco z ewoluującymi przepisami staje się kluczowe.
W kontekście CSA, zgodność regulacyjna polega na dostosowaniu systemów skomputeryzowanych do globalnych i lokalnych wymagań regulacyjnych, od etapu rozwoju, poprzez użytkowanie operacyjne, aż do ich wycofania. CSA kładzie nacisk na ciągłą zgodność, a nie na okresową walidację, promując proaktywne podejście do szybkiego reagowania na potencjalne zmiany regulacyjne. To strategiczne dostosowanie zapewnia, że firmy farmaceutyczne są dobrze przygotowane do spełniania oczekiwań regulacyjnych, chroniąc integralność danych, bezpieczeństwo pacjentów i ogólną niezawodność systemu.

Regularna współpraca z organami regulacyjnymi, udział w forach branżowych oraz subskrypcja publikacji regulacyjnych dostarczają cennych informacji na temat ewoluujących standardów. Wykorzystanie wiedzy konsultantów regulacyjnych oraz inwestowanie w ciągłe szkolenia dla personelu zaangażowanego w procesy CSA dodatkowo zwiększa świadomość regulacyjną. Współpraca z partnerami regulacyjnymi, takimi jak Freyr Solutions, oferuje proaktywne podejście, zapewniając dostęp do aktualnych informacji regulacyjnych i dopasowanych rozwiązań, aby płynnie przejść przez zmiany.
Zgodność regulacyjna w CSA jest dynamicznym i ciągłym zobowiązaniem, które jest zgodne z przejściem branży w kierunku elastyczności i ciągłego doskonalenia. Bycie na bieżąco, proaktywność i współpraca z ekspertami regulacyjnymi są kluczowe dla firm przechodzących z CSV na CSA, ułatwiając płynną i zgodną z przepisami ewolucję w ciągle zmieniającym się krajobrazie farmaceutycznym.
Jako zaufany partner regulacyjny, Freyr zapewnia niezbędne wsparcie i wiedzę specjalistyczną, aby przeprowadzić firmy przez tę transformację, zapewniając doskonałość regulacyjną i zgodność w erze CSA.
Jak pomaga strategiczny partner w zakresie zgodności regulacyjnej?
Strategiczny partner ds. zgodności regulacyjnej odgrywa kluczową rolę w zapewnieniu, że firmy farmaceutyczne spełniają wymagania regulacyjne i utrzymują wysokie standardy jakości. Oto, jak mogą pomóc:
- Doradztwo ekspertów: Partner strategiczny udziela fachowych porad dotyczących poruszania się w złożonych i zmieniających się przepisach w różnych regionach. Oferuje wgląd w najnowsze zmiany regulacyjne, pomagając firmom dostosować swoje praktyki i utrzymać zgodność.
- Usprawnione procesy: Pomagają usprawnić procesy zgodności poprzez wdrażanie najlepszych praktyk i efektywnych przepływów pracy. Obejmuje to opracowywanie solidnych systemów dokumentacji, audytu i walidacji, zmniejszanie obciążeń administracyjnych i poprawę ogólnej wydajności.
- Łagodzenie Ryzyka: Identyfikując potencjalne ryzyka i słabe punkty w zakresie zgodności, partner strategiczny pomaga łagodzić ryzyka, zanim staną się one problemami. Przeprowadzają oni szczegółowe audyty i oceny, aby upewnić się, że wszystkie procesy są zgodne i proaktywnie eliminują wszelkie luki.
- Szkolenia i wsparcie: Oferują szkolenia i wsparcie, aby zapewnić, że personel jest dobrze poinformowany o wymaganiach regulacyjnych i najlepszych praktykach. Pomaga to budować wewnętrzne kompetencje i zapewnia, że wszyscy zaangażowani w działania związane ze zgodnością są na bieżąco z aktualnymi standardami.
- Integracja technologii: Partner strategiczny pomaga w integracji innowacyjnych technologii, takich jak automatyzacja i sztuczna inteligencja, z procesami zgodności. Zapewniają, że technologie te są wdrażane skutecznie i zgodnie z wymaganiami regulacyjnymi, zwiększając integralność danych i efektywność procesów.
- Dokumentacja i prowadzenie rejestrów: Zarządzają tworzeniem, organizacją i utrzymaniem kluczowej dokumentacji zgodności. Zapewnia to, że wszystkie rejestry są dokładne, kompletne i łatwo dostępne do audytów i inspekcji.
- Zgłoszenia i zatwierdzenia regulacyjne: Zajmują się przygotowaniem i składaniem dokumentów i wniosków regulacyjnych. Obejmuje to zapewnienie, że zgłoszenia spełniają wszystkie niezbędne wymagania oraz zarządzanie komunikacją z organami regulacyjnymi w celu ułatwienia terminowych zatwierdzeń.
- Działania korygujące i zapobiegawcze: Strategiczny partner wspiera rozwój i wdrażanie działań korygujących i zapobiegawczych w odpowiedzi na wyniki audytów lub problemy ze zgodnością. Pomaga zapewnić, że te działania są skuteczne i nie zakłócają bieżących operacji.
- Globalna strategia zgodności: Opracowują i wdrażają strategie w celu osiągnięcia globalnej zgodności, uwzględniając różnorodne wymagania regulacyjne różnych rynków. Zapewnia to, że produkty spełniają wszystkie niezbędne normy do dystrybucji i użytku międzynarodowego.
- Ciągłe monitorowanie: Zapewniają ciągłe monitorowanie i wsparcie, aby informować firmy o wszelkich aktualizacjach lub zmianach regulacyjnych. To proaktywne podejście pomaga firmom zachować zgodność i dostosować się do nowych przepisów w miarę ich pojawiania się.
Dlaczego wybrać Freyr?
Ponad dziesięć lat doskonałości w zgodności regulacyjnej.
Pełen zakres zgodności, audytu i walidacji.
Ekspertyza w różnych branżach i regionach geograficznych.
Wykorzystuje innowacyjne narzędzia dla uzyskania dokładnych wyników.
Wykwalifikowani specjaliści z dogłębną znajomością branży.
Skuteczne zarządzanie złożonymi wyzwaniami w zakresie zgodności.
Często zadawane pytania
Zgodność w farmacji oznacza przestrzeganie przepisów prawa, regulacji i wytycznych, które rządzą przemysłem farmaceutycznym. Zapewnia to, że firmy dostosowują swoje działania do standardów branżowych, chroniąc tym samym bezpieczeństwo i skuteczność produktów, jednocześnie utrzymując integralność danych.
Celem audytu jest systematyczna ocena zgodności firmy ze standardami regulacyjnymi i wewnętrznymi politykami. Audyty pomagają identyfikować obszary wymagające poprawy, łagodzić ryzyka i zapewniać skuteczność procesów w produkcji bezpiecznych i zgodnych z przepisami produktów farmaceutycznych.
Walidacja w farmacji to proces potwierdzania, że systemy, procesy i sprzęt konsekwentnie spełniają z góry określone wymagania. Jest to kluczowe dla zapewnienia zgodności ze standardami regulacyjnymi oraz dla utrzymania jakości i bezpieczeństwa produktów farmaceutycznych przez cały ich cykl życia.
Procesy te są kluczowe dla zapewnienia bezpieczeństwa i skuteczności produktów, utrzymania zgodności z przepisami, poprawy zapewnienia jakości, wspierania dostępu do rynku i ułatwiania ciągłego doskonalenia. Pomagają one firmom spełniać rygorystyczne standardy i budować zaufanie wśród interesariuszy.
Wyzwania obejmują poruszanie się w zmieniających się przepisach, zapewnienie integralności danych, zarządzanie ograniczeniami zasobów oraz utrzymywanie właściwej dokumentacji. Dodatkowo, integracja innowacyjnych technologii i zapewnienie kompetencji personelu mogą skomplikować działania związane z zgodnością.
Audyty GxP to oceny przeprowadzane w celu zapewnienia zgodności ze standardami Dobrych Praktyk (GxP), które obejmują Dobrą Praktykę Wytwarzania (GMP), Dobrą Praktykę Kliniczną (GCP) i Dobrą Praktykę Laboratoryjną (GLP). Audyty te pomagają identyfikować luki w zgodności i usprawniać systemy jakości.
Niezależny audyt zgodności GxP to obiektywna ocena przestrzegania przez firmę standardów jakości i regulacyjnych. Przeprowadzany przez wykwalifikowanych audytorów, identyfikuje ryzyka i obszary do poprawy, zwiększając zgodność i bezpieczeństwo produktu.
Audyty GxP zapewniają bezstronne oceny, zwiększają zgodność regulacyjną i identyfikują obszary do usprawnień operacyjnych. Pomagają utrzymać wysokie standardy jakości i budować zaufanie u organów regulacyjnych oraz klientów.
CSV zapewnia, że skomputeryzowane systemy używane w farmacji konsekwentnie generują wiarygodne dane i spełniają wymagania regulacyjne. Jest to kluczowe dla utrzymania integralności danych, łagodzenia ryzyka i zapewnienia bezpieczeństwa pacjentów przez cały cykl życia produktu.
CSV koncentruje się na walidacji, czy system spełnia wymagania regulacyjne i działa zgodnie z przeznaczeniem, natomiast CSA obejmuje szersze podejście, które obejmuje ciągłe zapewnianie wydajności i zgodności systemu przez cały jego cykl życia.














