Pisanie regulacyjne odgrywa kluczową rolę w przemyśle farmaceutycznym i opiece zdrowotnej, łącząc złożone informacje naukowe z różnymi zainteresowanymi stronami. Sztuka dostosowywania pisania regulacyjnego do różnych odbiorców jest niezbędna dla skutecznej komunikacji i zgodności z przepisami. Ten blog zbada, jak dostosować pisanie regulacyjne dla trzech (3) kluczowych grup odbiorców: pacjentów, lekarzy i organów regulacyjnych.
Zrozumienie znaczenia pisania dostosowanego do odbiorcy
Pisanie regulacyjne obejmuje różne dokumenty, każdy służący określonemu celowi i skierowany do różnych czytelników. Umiejętność dostosowywania treści do tych różnorodnych odbiorców jest kluczowa dla zapewnienia, że informacje są nie tylko dokładne, ale także dostępne i możliwe do wykorzystania.
Kluczowe punkty uwzględniające podejście dostosowawcze:
Pisanie dla pacjentów: Upraszczanie złożonych informacji
Przy tworzeniu dokumentów regulacyjnych dla pacjentów, głównym celem jest przekazanie istotnych informacji w sposób jasny i zrozumiały, bez poświęcania dokładności.
- Stosowanie prostego języka
Używaj codziennych słów i unikaj żargonu technicznego. Gdy terminy medyczne są konieczne, podaj jasne wyjaśnienia.
- Pomoce wizualne i formatowanie
Włącz diagramy, wykresy i infografiki, aby zilustrować złożone koncepcje. Używaj punktorów, nagłówków i krótkich akapitów, aby poprawić czytelność.
- Rozwiązywanie częstych obaw
Przewidywanie i rozwiewanie potencjalnych pytań lub obaw, które pacjenci mogą mieć w związku z lekiem lub terapią.
Przykład: Ulotki informacyjne dla pacjenta
Dokumenty te powinny:

Pisanie dla klinicystów: Równoważenie szczegółowości i praktyczności
Klinicyści potrzebują wyczerpujących, lecz zwięzłych informacji, aby podejmować świadome decyzje dotyczące opieki nad pacjentem. Tworzenie dokumentacji regulacyjnej dla tej grupy odbiorców musi równoważyć szczegóły naukowe z praktycznym zastosowaniem.
- Nacisk na znaczenie kliniczne.
Koncentrujemy się na informacjach wpływających na opiekę nad pacjentem, takich jak wytyczne dotyczące dawkowania, przeciwwskazania i interakcje leków.
- Ustrukturyzowana prezentacja danych.
Organizuj wyniki badań klinicznych i dane dotyczące bezpieczeństwa w logicznym, łatwym do nawigacji formacie. Używaj tabel i wykresów do podsumowania kluczowych ustaleń.
- Włączenie rekomendacji opartych na dowodach.
Dostarczyć jasne, oparte na dowodach wytyczne dotyczące właściwego stosowania leków lub wyrobów medycznych w różnych scenariuszach klinicznych.
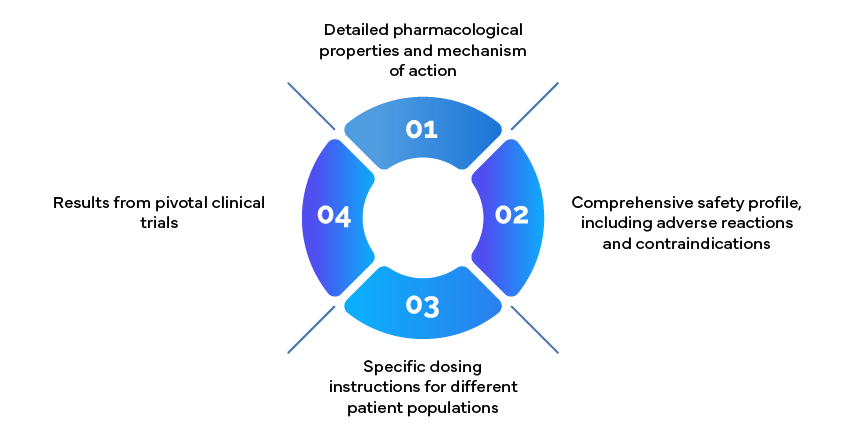
Przykład: Informacje dotyczące przepisywania leków
Dokumenty z informacjami o przepisywaniu, znane również jako ulotki dołączone do opakowania, są kluczowymi zasobami dla klinicystów. Powinny one zawierać:
Pisanie dla organów regulacyjnych: Precyzja i zgodność
Organy regulacyjne wymagają wyczerpującej, naukowo rygorystycznej dokumentacji do oceny bezpieczeństwa i skuteczności nowych produktów. Pisanie dla tej grupy odbiorców wymaga skrupulatnej dbałości o szczegóły i ścisłego przestrzegania wytycznych regulacyjnych.
- Zgodność z wytycznymi regulacyjnymi
Zapewnij, że wszystkie dokumenty są zgodne z określonymi wymogami dotyczącymi formatu i treści organów regulacyjnych, takich jak FDA lub EMA.
- Kompleksowa Prezentacja Danych
Dostarczyć szczegółową analizę wszystkich istotnych danych, w tym szczegółowe opisy metodologii badań, analiz statystycznych oraz interpretacji wyników.
- Przejrzystość w raportowaniu
Należy ujawnić wszelkie ograniczenia lub potencjalne stronniczości w badaniach i wyjaśnić, jak te czynniki mogą wpływać na wnioski.
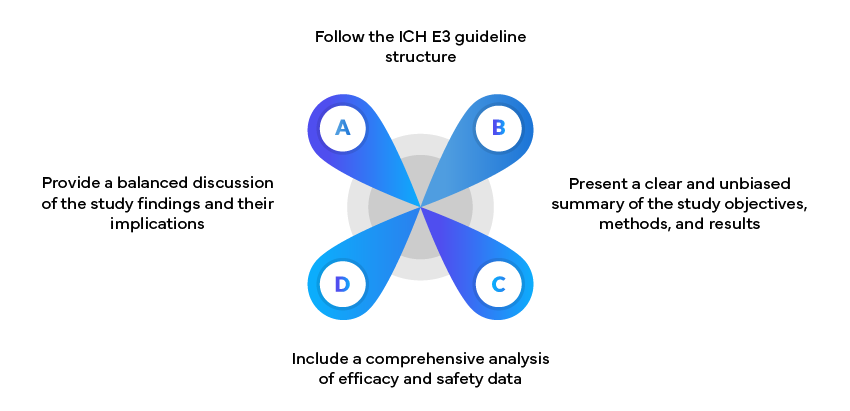
Przykład: Raporty z badań klinicznych
Raporty z badań klinicznych (CSR) są kluczowymi dokumentami w zgłoszeniach regulacyjnych. Powinny one:
Podsumowanie
Dostosowywanie dokumentacji regulacyjnej do różnych odbiorców jest złożonym, ale niezbędnym zadaniem w przemyśle farmaceutycznym i opiece zdrowotnej. Poprzez dostosowanie treści i stylu prezentacji do specyficznych potrzeb pacjentów, klinicystów i organów regulacyjnych, autorzy mogą zapewnić, że kluczowe informacje są skutecznie przekazywane i zrozumiałe.
Umiejętność tworzenia jasnych, dokładnych i dostosowanych do odbiorcy dokumentów regulacyjnych to nie tylko kwestia zgodności; ma to bezpośredni wpływ na bezpieczeństwo pacjentów, podejmowanie decyzji klinicznych oraz pomyślny rozwój i wprowadzanie na rynek nowych produktów opieki zdrowotnej. W miarę ewolucji środowiska regulacyjnego, znaczenie umiejętnego pisania regulacyjnego, które potrafi połączyć złożone dane naukowe z potrzebami różnych interesariuszy, będzie tylko rosło. Autorzy tekstów regulacyjnych odgrywają kluczową rolę w promowaniu zdrowia publicznego i wspieraniu innowacji w dziedzinie medycyny, koncentrując się na jasności dla pacjentów, znaczeniu klinicznym dla pracowników służby zdrowia oraz kompleksowej precyzji dla organów regulacyjnych. Opanowanie sztuki pisania regulacyjnego dostosowanego do konkretnego odbiorcy jest zatem nieocenioną umiejętnością w dzisiejszym szybko zmieniającym się środowisku opieki zdrowotnej.










