Descripción del trabajo (SOW) para Dispositivos Médicos activos Dispositivos Médicos Dispositivos Médicos no activos: resumen de la solicitud Dispositivos Médicos (k)
En Freyr, nuestro equipo de expertos recopila y sintetiza minuciosamente la información más reciente y esencial para sus solicitudes 510(k), tanto para productos sanitarios activos como no activos. Esto le garantiza que dispondrá de los conocimientos necesarios para desenvolverse con confianza en el marco normativo. Desde aclarar las diferencias entre dispositivos activos y no activos hasta profundizar en las complejidades de la solicitud 510(k), hemos recopilado un amplio repositorio de recursos para que sirva de referencia principal. Emprenda un viaje hacia el dominio de la solicitud Dispositivos Médicos (k) para Dispositivos Médicos activos y la solicitud 510(k) para dispositivos médicos no activos con nuestra guía completa.
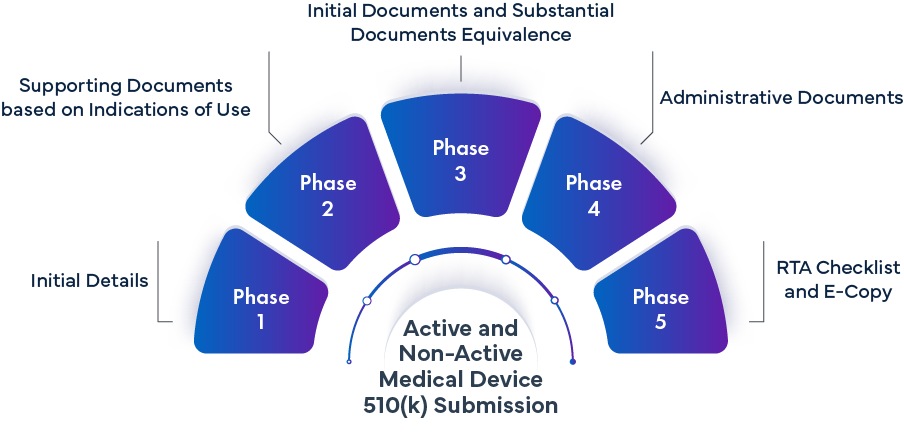
Fase -1 Detalles Iniciales | ||
|---|---|---|
Requisitos | Alcance del solicitante 510(k) | Alcance de Freyr |
| Uso previsto |
|
|
| Declaración de indicaciones de uso (Formulario 3881) |
|
|
| Descripción del dispositivo |
|
|
| Normas y orientación |
|
|
| Dispositivo de referencia |
|
|
| Resumen de la notificación 510(k) |
|
|
Fase 2: Documentación de apoyo basada en las indicaciones de uso. | |||
|---|---|---|---|
Requisitos de documentación | Alcance del solicitante 510(k) | Alcance de Freyr | |
| 2.1 | Dibujo del dispositivo | Enviar el archivo de dibujo del dispositivo para asegurar una representación precisa de su diseño. | Iniciar una solicitud formal para un plano de un dispositivo activo. Revisar exhaustivamente y documentar meticulosamente la información necesaria para la presentación 510(k). |
| 2.2 | Diseño y desarrollo del dispositivo. | Enviar el archivo de diseño y desarrollo del dispositivo activo, que abarque toda la información y documentación pertinente. | Enviar una solicitud para el diseño y desarrollo de un dispositivo activo. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.3 | Hoja de datos de seguridad del material | Proporcione las Hojas de Datos de Seguridad del Material (MSDS) para los componentes esenciales del dispositivo activo, asegurando información completa sobre su seguridad y composición | Enviar una solicitud de la ficha de datos de seguridad del material de los componentes esenciales del dispositivo activo. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.4 | Diagrama de flujo de fabricación | Proporcionar un diagrama de flujo de fabricación que detalle el proceso de producción del dispositivo activo, ofreciendo una representación visual de los pasos de fabricación y su secuencia. | Envíe una solicitud para la Hoja de Datos de Seguridad del Material (MSDS) de los componentes esenciales para el dispositivo activo. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.5 | Descripción del dispositivo | Proporcionar detalles completos, incluyendo: o Un panorama general del dispositivo o Funciones y modos de funcionamiento o Diagramas de bloques o Fotografías, cables y accesorios relevantes o Interoperabilidad del dispositivo. o Descripción de la fuente de alimentaciónTop of Form | Enviar una solicitud de información detallada sobre el dispositivo. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.6 | Etiquetado Propuesto | Proporcionar las Instrucciones de Uso (IFU), el Manual de Usuario y cualquier material promocional asociado para el dispositivo activo. | Envíe una solicitud para las Instrucciones de Uso (IFU), el Manual de Usuario y cualquier material promocional, si está disponible. Revisar las Instrucciones de Uso, el Manual de Usuario y el material promocional proporcionado por el solicitante. Documentar las IFU, el Manual de Usuario y el material promocional con el propósito de la presentación 510(k). |
| 2.7 | Embalaje y Transporte | Proporcionar los planes de estudio e informes para la validación del embalaje y transporte. | Presentar una solicitud para el plan de estudio y los informes sobre la Validación del Embalaje y Transporte. Revisar los planes de estudio y los informes para la Validación del Embalaje y Transporte y proporcionar las correcciones o comentarios necesarios. |
| 2.8 | Esterilización (Si aplica la esterilidad) | Proporcione los planes y los informes del estudio para la Validación de la Esterilización. | Envíe una solicitud para el plan y los informes del estudio de Validación de la Esterilización. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.9 | Pruebas de Rendimiento _ en Banco | Iniciar una solicitud formal para los planes e informes de estudios de banco de pruebas de rendimiento, detallando los requisitos y objetivos específicos a abordar | Envíe una solicitud para los planes y los informes del estudio en banco del dispositivo activo para las pruebas de rendimiento. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
Documentación de apoyo para la compatibilidad electromagnética y la seguridad eléctrica | |||
| 2.10 | Características del dispositivo relacionadas con la EMC y entornos de uso previsto | Proporcione detalles sobre las características del dispositivo relacionadas con EMC y los entornos de uso previsto, incluyendo: o Un panorama general del dispositivo. o Funciones y modos de funcionamiento. o Diagramas de bloques. o Fotografías, cables y accesorios relevantes. o Interoperabilidad del dispositivo. o Descripción de la fuente de alimentación, incluida la viabilidad de utilizar el Dispositivo Médico alimentado internamente mientras se carga. o Entornos en los que el Dispositivo Médico está previsto para ser utilizado. o Descripción de cualquier tecnología inalámbrica (si procede) para consideraciones adicionales sobre Dispositivos Médicos con capacidad inalámbrica. o Descripción de cualquier emisor de RF interno en el Dispositivo Médico que pudiera causar perturbaciones electromagnéticas. o Abordar los emisores electromagnéticos (EM) comunes, así como los emisores médicos únicos.
| Envíe una solicitud de información sobre las características del dispositivo relacionadas con EMC y los entornos de uso previsto. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.11 | Evaluación de Riesgos | Suministre un Plan de Gestión de Riesgos que incluya una evaluación de riesgos que demuestre una mitigación de riesgos eficaz, junto con un informe completo de gestión de riesgos que abarque todos los elementos de riesgo. Proporcione el documento revisado con las correcciones y mejoras sugeridas | Envíe una solicitud para el Expediente de Gestión de Riesgos y solicite la documentación del Plan y el Informe de Gestión de Riesgos, incluyendo la identificación de peligros de riesgo, la evaluación de riesgos y la demostración de una mitigación de riesgos adecuada. El Informe de Gestión de Riesgos debe cubrir todos los elementos de riesgo, preferiblemente con secciones separadas para mayor claridad. Proporcione una plantilla del Plan de Gestión de Riesgos y del Informe de Gestión de Riesgos que abarque todos los riesgos relacionados con el dispositivo, a solicitud del solicitante. Revise los datos del Expediente de Gestión de Riesgos, incluyendo el Plan y el Informe compartidos por el solicitante, y proporcione sugerencias para las correcciones necesarias a fin de asegurar una documentación completa para la presentación 510(k). Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.12 | Estándar de Consenso | Proporcionar confirmación de las normas de consenso pertinentes y una explicación de cualquier desviación de las normas reconocidas por la FDA. | Envíe una solicitud para las normas de consenso aplicables relacionadas con EMC y la seguridad eléctrica para el dispositivo activo. Documentar los estándares de consenso confirmados para el dispositivo activo con el propósito de la presentación 510(k). |
| 2.13 | Criterios de Aprobación/Rechazo de Rendimiento Esencial e Inmunidad | Presente el plan de estudio y los informes de las pruebas de Rendimiento Esencial e Inmunidad realizadas en el dispositivo activo, siguiendo los estándares reconocidos por la FDA. | Envíe una solicitud para el plan de estudio y los informes de las pruebas de Rendimiento Esencial e Inmunidad realizadas en el dispositivo activo, de acuerdo con los estándares reconocidos por la FDA. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.14 | Configuración y Funciones Probadas de Dispositivos Médicos | Proporcione la Configuración del Dispositivo Médico y las Funciones Probadas para el dispositivo activo, que abarca los siguientes detalles: o Proporcionar una descripción exhaustiva del Dispositivo Médico bajo prueba, incluyendo información detallada sobre su configuración, funciones, modos y los ajustes específicos que se probaron. o La descripción del dispositivo bajo prueba debe incluir el nombre del Dispositivo Médico, el número de modelo e indicar si el dispositivo es el Dispositivo Médico final listo para producción que se encuentra actualmente en revisión. | Enviar una solicitud para las funciones de configuración y prueba del Dispositivo Médico activo. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
| 2.15 | Resultados de las Pruebas de EMC | Proporcionar el plan de estudio y el informe de pruebas de EMC (compatibilidad electromagnética) de acuerdo con la norma de consenso reconocida por la FDA y recomendada para el dispositivo activo. | Iniciar una solicitud formal para el plan de estudio y el informe de pruebas de EMC, alineados con el estándar de consenso reconocido por la FDA y recomendado para dispositivos activos. Revisar exhaustivamente y documentar meticulosamente toda la información necesaria en preparación para la presentación 510(k). |
Fase 3 – Documentos iniciales y documentos de equivalencia sustancial | |||
|---|---|---|---|
Requisitos de documentación | Alcance del solicitante 510(k) | Alcance de Freyr | |
| 3.1 | Hoja de cubierta de la solicitud de revisión previa a la comercialización del CDRH (Formulario FDA 3514) | - | Complete el formulario 3514 de la FDA utilizando los detalles proporcionados por el solicitante |
| 3.2 | Resumen y certificación de Clase III | - | Este paso no es necesario si no se requieren estudios clínicos. |
| 3.3 | Certificación Financiera o Declaración de Divulgación. | - | Este paso no es necesario si no se requieren estudios clínicos. |
| 3.4 | Resumen Ejecutivo | - | Desarrollar una plantilla y preparar el documento de forma minuciosa. Proporcione justificaciones para cualquier discrepancia observada entre el dispositivo propuesto y el dispositivo de referencia. Si se elige un estudio comparativo entre el dispositivo propuesto y el dispositivo de referencia, se crea una plantilla y se prepara el documento correspondiente. |
| 3.5 | Discusión sobre la equivalencia sustancial | - | Desarrollar una plantilla y preparar el documento de forma minuciosa. Si se elige un estudio comparativo entre el dispositivo propuesto y el dispositivo de referencia, se crea una plantilla y se prepara el documento correspondiente. |
Fase 4 – Documentos administrativos | |||
|---|---|---|---|
Requisitos de documentación | Alcance del solicitante 510(k) | Alcance de Freyr | |
| 4.1 | Carta de presentación 510(k) | Firme el documento impreso en papel con membrete de la empresa y gestione el envío de una copia física por mensajería a la oficina de US. Proporcione una copia digital de la carta de presentación 510(k) firmada para su inclusión en la documentación 510(k) | Prepare una plantilla completa que abarque todos los detalles necesarios para la carta de presentación y proporciónela al solicitante. Indique al solicitante que utilice su membrete oficial y asegúrese de que la carta de presentación esté firmada por una persona autorizada. |
| 4.2 | Declaración de Veracidad y Exactitud | Asegurar que el documento sea firmado por la persona de contacto designada en la empresa y entregado según corresponda. | Desarrollar una plantilla completa que contenga todo el contenido necesario para incluir en el documento de presentación. |
| 4.3 | Declaraciones de conformidad e informe resumido | Asegurar que el documento sea firmado por la persona de contacto designada en la empresa y entregado según corresponda. | Desarrollar una plantilla completa para listar y preparar sistemáticamente los documentos requeridos. |
| 4.4 | MDFUSC (Formulario FDA 3601) | Realice el pago requerido a la FDA antes de la presentación formal del expediente 510(k). | Generar una hoja de portada de la tarifa de usuario y un Número de Identificación Personal (PIN) único específicamente para la presentación de Dispositivos Médicos. |
Fase 5 – Lista de verificación RTA y copia electrónica | |||
|---|---|---|---|
Requisitos de documentación | Alcance del solicitante 510(k) | Alcance de Freyr | |
| 5.1 | Lista de verificación RTA | Aprobación de la Verificación de la Lista de Verificación RTA (Lista para Aceptar), lo que indica que se han cumplido con éxito todos los requisitos | Desarrollar una plantilla de lista de verificación RTA personalizada adaptada al tipo específico de presentación. Complete la lista de verificación rellenando meticulosamente todos los campos obligatorios y asegurándose de que los documentos mencionados se presenten debidamente a la FDA y se compartan con el solicitante. |
| 5.2 | Copia electrónica | Aprobación de la documentación contenida en la Carpeta de Presentación Final, lo que significa su cumplimiento con todos los requisitos y estándares necesarios. | Organizar las secciones de la carpeta de presentación de acuerdo con la guía de la FDA y compartirlas rápidamente con el solicitante. Convertir el expediente de presentación en una copia electrónica para un acceso y revisión convenientes. Enviar la copia electrónica de la presentación al Agente US designado. |
Registro de Dispositivos Médicos
- Estrategia reglamentaria integral para la US FDA
- Identificación de dispositivos de referencia
- Establecer la equivalencia sustancial con un Dispositivo de Referencia
- Análisis de Brechas para el Cumplimiento con la US FDA
- Compilación de 21 secciones del Expediente Técnico 510(k)
- Publicación y creación de eCopy
- Validación y envío de eCopy
- Servicios de enlace para la aprobación de dispositivos
- Gestión de la respuesta RTA y las deficiencias
- Servicios de consultoría para abordar deficiencias
- Registro de Dispositivos y mantenimiento de la base de datos FURLS

- Hemos gestionado muchos registros 510(k) de diversas categorías de dispositivos
- Equipo experto para la compilación 510(k) según los requisitos de la Notificación Previa a la Comercialización (510(k)) de la FDA de US
- Soporte adicional para gestionar consultas del 510(k)
- Asesoramiento sobre el tipo adecuado de 510(k) según los requisitos de presentación 510(k) de la FDA de US para el dispositivo
- Presentación a tiempo de los entregables
- Al día con las nuevas enmiendas de la US FDA

