Dispositivos Médicos norteamericano Dispositivos Médicos es uno de los más atractivos y más regulados del mundo. En Estados Unidos, Dispositivos Médicos está supervisado por la FDA, principalmente a través del Centro de Dispositivos y Salud Radiológica (CDRH), mientras que en Canadá lo regula Health Canada en el marco de un sistema basado en el riesgo.
Para los fabricantes, desenvolverse en estos mercados puede resultar complejo. Ambos países se basan en Dispositivos Médicos basada en el riesgo (Clase I, II, III y, en Canadá, Clase IV), respaldada por pruebas sólidas de seguridad y rendimiento, así como por un sistema de gestión de la calidad (SGC) conforme a la normativa. Programas como MDSAP normas como ISO 13485, junto con las diferencias en la terminología, los procedimientos y los requisitos de documentación, añaden aún más complejidad a la hora de planificar la entrada en los mercados US Canadá.
Freyr ayuda a los fabricantes a convertir esta complejidad en un plan claro y viable para acceder a los mercados US Canadá. Conocemos a fondo las interrelaciones entre FDA y Dispositivos Médicos de Health Canada, y le ayudamos a armonizar las clasificaciones, la documentación de apoyo, el sistema de gestión de la calidad y los expedientes, para que pueda seguir una estrategia única y eficaz en materia de autorizaciones, lanzamientos y cumplimiento normativo a largo plazo en ambos países.
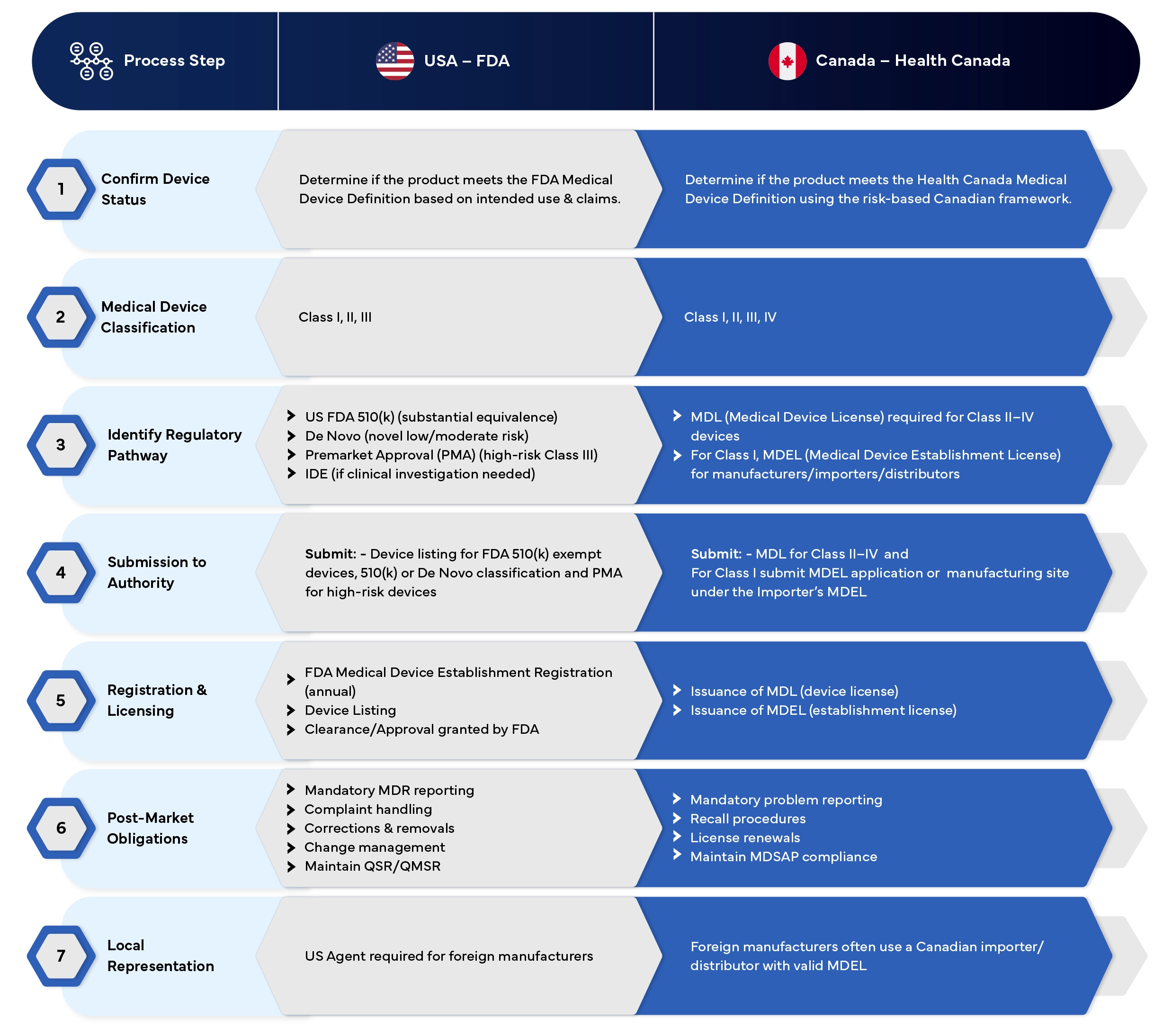
EE. UU. contra Canadá
Proceso Dispositivos Médicos : tabla comparativa
Servicios de Registro de Dispositivos Médicos de Freyr
Registro de Dispositivos Médicos en América
- Soporte reglamentario y de inteligencia de mercado
- Clasificación de productos según los requisitos reglamentarios
- Registro de Dispositivos Médicos en US -513 (G) y (Vía correcta entre 510 (K)/De-NOVO/PMA/IDE)
- Reunión previa a la presentación con las agencias de salud
- Soporte normativo para documentos de productos como, el Expediente de Historial de Diseño (DHF)
- Análisis de Brechas de los Documentos Técnicos y los Sistemas de Buenas Prácticas de Fabricación (BPF)
- Soporte reglamentario para la compilación del Expediente Técnico según lo requerido por la vía de registro correspondiente
- Estrategia de cumplimiento del sistema de calidad de la USFDA (21 CFR 820)
- Servicios de cumplimiento del Programa de Auditoría Única para Dispositivos Médicos (MDSAP)
- Registro de Dispositivos Médicos en Canadá - Registro de Licencia de Dispositivo Médico (MDL) y Licencia de Establecimiento de Dispositivos Médicos (MDEL)
- Enlace y apoyo con la Agencia de Salud
- Representación en el país – Servicios de Agente en EE. UU. y Persona Responsable Sanitaria
- Actividades de Cumplimiento Posterior a la Aprobación

- Presentaciones exitosas para diversas clases de dispositivos, desde software hasta suturas
- Acceso a filiales locales para afrontar los desafíos de los requisitos específicos de la autoridad y del idioma
- Personal dedicado y experto para proporcionar soporte reglamentario para Dispositivos Médicos e IVD.
- Modelo rentable para el apoyo de representación en el país o legal
- Hemos entregado con éxito varios proyectos en US y Canadá
- Con sede en US.

¿Por qué asociarse con Freyr?
- Experiencia End-to-end en materia de normativa End-to-end América End-to-end , que abarca desde las notificaciones previas a la comercialización (solicitudes) ante FDA Health Canada hasta la vigilancia poscomercialización y el cumplimiento normativo a lo largo de todo el ciclo de vida del producto.
- Éxito demostrado en más de 1500 Dispositivos Médicos a nivel mundial, que abarcan dispositivos de las clases I a III en EE US de las clases I a IV en Canadá.
- Presencia sobre el terreno a través de los servicios US y el apoyo normativo en Canadá, con el respaldo de equipos de expertos repartidos por todo el mundo para garantizar una ejecución fluida.
- Estrategia integrada US Canadá que optimiza los requisitos en materia de pruebas, documentación y calidad con el fin de reducir los costes, la duplicación de tareas y los plazos de aprobación.
- Colaboración directa con FDA Health Canada, garantizando una comunicación clara, respuestas oportunas y una adaptación proactiva a las expectativas normativas.
- Contamos con la confianza de más de 470 Dispositivos Médicos de todo el mundo, desde empresas emergentes hasta multinacionales, como su socio regulatorio a largo plazo en Norteamérica.












