Descripción general de los servicios de cumplimiento del IVDR de la UE
El Reglamento Europeo de Dispositivos Médicos de Diagnóstico In Vitro (IVDR de la UE) es una nueva base reglamentaria para la comercialización de IVD en el mercado europeo. El Reglamento IVDR de la UE está destinado a reemplazar la Directiva actual de la UE sobre productos sanitarios para diagnóstico in vitro (UE 98/79/CE). Como reglamento europeo, será efectivo en todos los Member States de la UE y en los estados de la Asociación Europea de Libre Comercio (AELC) sin necesidad de ser traspuesto a la legislación de los respectivos Estados. Como socio reglamentario probado, Freyr ofrece servicios de cumplimiento del IVDR de la UE y servicios de consultoría de IVDR a los fabricantes para el cumplimiento de las Reglamentaciones de Diagnóstico In Vitro y el marcado CE.
Agende una reunión con nuestros expertos en el IVDR de la UE
El Reglamento IVDR - Cronograma de transición
Con entrada en vigor obligatoria a partir del 26 de mayo de 2022, el nuevo IVDR de la UE se considera un cambio significativo en la supervisión reglamentaria de los IVD. A continuación se presenta un resumen de la transición del IVDR –
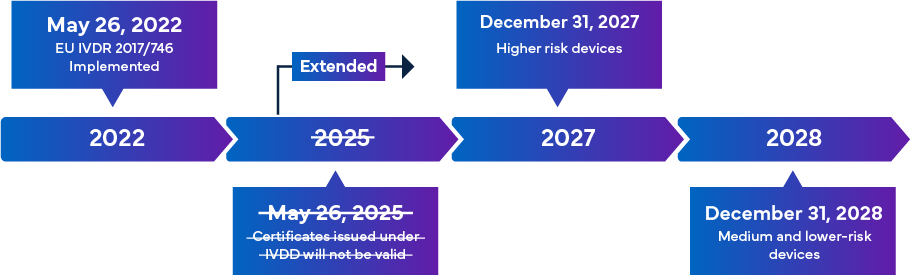
Una vez implementadas por completo, las normas de cumplimiento del IVDR garantizan que casi todos los productos sanitarios para diagnóstico in vitro (IVD) que entran en el mercado europeo están sujetos a la revisión del Organismo Notificado (NB) del IVDR y a la certificación de marcado CE como parte del proceso de aprobación de IVD. En este escenario, además de alinearse con la clasificación actualizada del IVDR, existe un requisito inmediato para que los fabricantes revisen eficazmente la documentación técnica clave para el registro exitoso de los IVD y el marcado CE. Los requisitos del IVDR varían según la clase de riesgo del IVD. En general, para la certificación de IVD, los fabricantes deben realizar:
- Revisiones del expediente técnico según el Reglamento IVDR (Reglamento (UE) 2017/746)
- Preparación del Informe de Evaluación del Rendimiento (PER) para todos los IVD
- Seguimiento del rendimiento poscomercialización (PMPF) según el Anexo XIII, Parte B del IVDR
- Notificación de vigilancia según el Artículo 82 del IVDR
Freyr apoya a los clientes en la realización de una revisión sistemática de la literatura científica y ayuda en la planificación y preparación de un PER para el cumplimiento del Reglamento de Diagnóstico In Vitro. Freyr cuenta con expertos dedicados que ofrecen servicios de consultoría IVDR y apoyo para la Post-market Surveillance (PMS), que es una parte integral del sistema de gestión de calidad del fabricante junto con el Post-market Performance Follow-up (PMPF).
Obtenga asesoramiento experto sobre su cumplimiento del IVDR de la UE
Experiencia y ventajas de los servicios de cumplimiento del IVDR de la UE
- Plan de transición para el cumplimiento del IVDR
- Revisión técnica y análisis de deficiencias de los requisitos del IVDR para los RGSP (Requisitos Generales de Seguridad y Rendimiento)
- Apoyo en la compilación del expediente técnico según los requisitos del IVDR
- Informes de validez científica basados en la literatura y/o datos internos
- Informes de rendimiento clínico basados en la literatura y/o datos internos
- Evidencia clínica o informes de evaluación del rendimiento
- Protocolos e informes de seguimiento del rendimiento poscomercialización (PMPF)
- Protocolos e informes de Post-market Surveillance (PMS)
- Redacción/revisión de otros documentos como prospectos/IFU (Instrucciones de Uso), Instrucciones de Referencia Rápida (QRI), Manual de Operación/Usuario, etc.

- Cumplimiento garantizado del IVDR, registro de IVD y marcado CE.
- Sólido conocimiento reglamentario y experiencia en las áreas clave de impacto del IVDR de la UE
- Modelo de entrega impulsado por una sólida gestión de proyectos para asegurar el cumplimiento de los plazos.
- Expertos NB internos (revisión del informe por los revisores interactivos del NB)
- Equipos especializados con experiencia transversal en áreas de impacto específicas y categorías de dispositivos.
- Aportaciones interfuncionales de expertos en Dispositivos Médicos para cumplir con los requisitos
- Alcance completo de servicios que abarca cumplimiento, revisión y planificación
- Gran experiencia en mantener la coherencia en los entregables (Tiempo y Calidad)









