Evolución de los genéricos - Panorama general
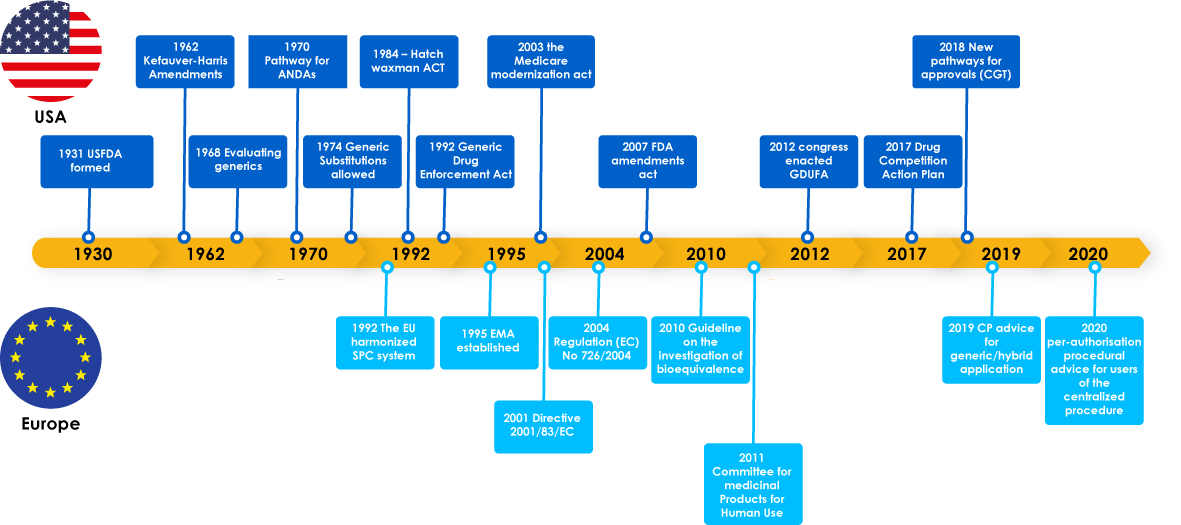
Los medicamentos genéricos han logrado hitos importantes, incluyendo leyes reglamentarias para apoyar el desarrollo de genéricos, lo que animó a los fabricantes a explorar el mercado de genéricos. Estas legislaciones también dieron a los médicos la confianza para recetar un sustituto de un medicamento de marca y finalmente benefició a los pacientes, ya que los fabricantes de genéricos satisficieron necesidades críticas de pacientes en todo el mundo.
Preguntas frecuentes sobre genéricos
P1: ¿Qué son los medicamentos genéricos?
Resp: Los medicamentos genéricos son fármacos que son copias idénticas del medicamento original y tienen el mismo API, dosis, uso previsto, efectos secundarios, vía de administración, riesgos, seguridad y potencia que el medicamento innovador, pero pueden diferir en algunas características como el proceso de fabricación, la formulación, los excipientes, el color, el sabor y el empaque. En otras palabras, un medicamento genérico es terapéuticamente equivalente a un medicamento de marca y, por lo tanto, puede sustituirse por su homólogo de marca.
P2: ¿Por qué los medicamentos genéricos cuestan menos que un medicamento innovador?
Resp: Los medicamentos genéricos son más rentables en comparación con el medicamento innovador, porque los medicamentos genéricos no tienen que repetir los costosos y largos estudios preclínicos y clínicos que se requieren para que los medicamentos innovadores demuestren seguridad y eficacia y, en su lugar, los medicamentos genéricos solo necesitan demostrar la equivalencia farmacéutica de su producto.
P3: ¿Son los medicamentos genéricos tan buenos como un medicamento innovador?
Resp: Sí, los medicamentos genéricos tienen la misma calidad, eficacia y son tan seguros como los medicamentos de marca. El precio más bajo de estos medicamentos no indica que sean de calidad inferior, porque los medicamentos genéricos, al igual que los medicamentos de marca, tienen que pasar por un riguroso proceso de aprobación de medicamentos para comercializar su producto y las compañías farmacéuticas deben presentar la solicitud de medicamento genérico, demostrando que su producto tiene el mismo beneficio clínico que los medicamentos de marca y es adecuado para ser utilizado como sustituto de su respectivo medicamento de marca.
P4: ¿Por qué los medicamentos genéricos tienen un aspecto diferente al producto de marca?
Resp: Los medicamentos genéricos deben ser bioequivalentes a los medicamentos de marca y tener el mismo API que los medicamentos innovadores. Sin embargo, puede haber pequeñas diferencias en los medicamentos genéricos con respecto a la forma, el etiquetado (diferencias menores), el empaque y los ingredientes inactivos como el color, los sabores y los conservantes; pero la eficacia del medicamento debe seguir siendo la misma.
P5: ¿Qué implica la revisión y aprobación de solicitudes de medicamentos genéricos en los US?
Respuesta: Cualquier empresa farmacéutica que deba comercializar su medicamento genérico en US debe cumplir con todos los requisitos reglamentarios de la FDA de US para la presentación de medicamentos genéricos y debe demostrar que:
- El medicamento genérico es “farmacéutica/terapéuticamente equivalente” a la marca
- El fabricante es capaz de producir el medicamento de forma correcta y consistente
- El “ingrediente activo” es el mismo que el de la marca
- La cantidad adecuada del ingrediente activo llega al lugar del cuerpo donde hace efecto.
- Los ingredientes "inactivos" del medicamento son seguros.
- El medicamento no se degrada con el tiempo.
- El envase en el que se enviará y venderá el medicamento es adecuado.
- La etiqueta es igual que la del medicamento de marca.
- Las patentes relevantes o las exclusividades legales han caducado.
P6: ¿Cada medicamento de marca tiene un medicamento genérico?
Resp: No. No todos los medicamentos de marca tienen una versión genérica. Los nuevos medicamentos se fabrican bajo protección de patente por hasta veinte (20) años. Esto significa que ningún otro medicamento puede fabricarse y comercializarse durante este período, hasta el vencimiento de la patente. Sin embargo, algunos medicamentos pueden no tener nunca versiones genéricas para su producto, debido a la dificultad en la fabricación o en caso de que el medicamento genérico pueda considerarse no rentable.








