Descripción general de los Servicios de Cumplimiento de EU MDR
El Reglamento de Dispositivos Médicos de la UE (MDR) ha entrado en vigor a partir del 26 de mayo de 2021, después del plazo de transición de 3 años y una prórroga adicional de un año debido a la pandemia de COVID-19. Los dispositivos que se lanzan ahora en el mercado de la UE deben cumplir con estos reglamentos y deberán contar con la certificación CE según el EU MDR por parte de los Organismos Notificados acreditados bajo estos reglamentos. Sin embargo, los dispositivos que ya han sido certificados CE según la Directiva de Dispositivos Médicos de la UE (EU MDD) tienen períodos de gracia antes de tener que cumplir plenamente con los requisitos del EU MDR. Durante este período de gracia, los dispositivos certificados bajo la EU MDD y el EU MDR coexistirán en el mercado con el mismo estatus y sin ser objeto de discriminación. Freyr ofrece servicios inigualables de cumplimiento del EU MDR para ayudar a las empresas de Dispositivos Médicos a cumplir con los requisitos del EU MDR de manera oportuna.
Cronograma de transición y nuevas clasificaciones de dispositivos
El Reglamento Europeo de Dispositivos Médicos (MDR) entrará en pleno vigor en todos los Estados miembros de la UE y en los Estados de la Asociación Europea de Libre Comercio (EFTA) a partir de mayo de 2021 y otorga a los fabricantes un período de transición de 4 años para la Certificación EU MDR completa.
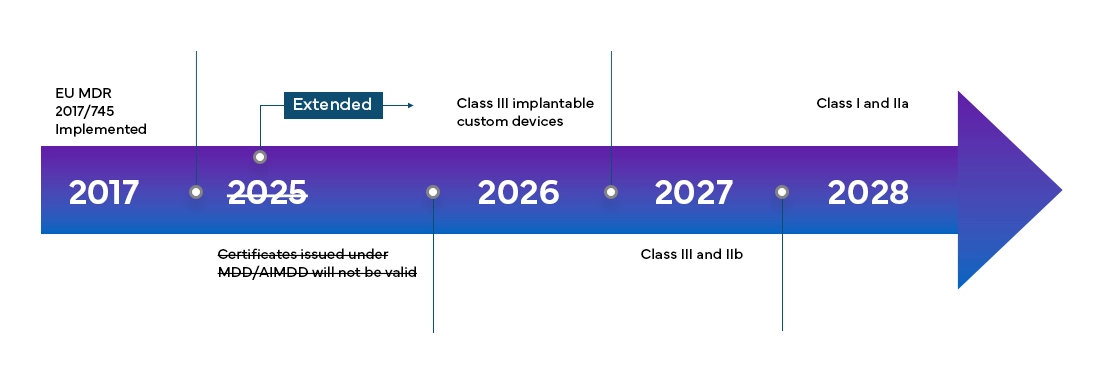
El nuevo Reglamento Europeo de Dispositivos Médicos (MDR), como se ha observado, también ha introducido cambios en el sistema de clasificación de dispositivos existente, tales como:
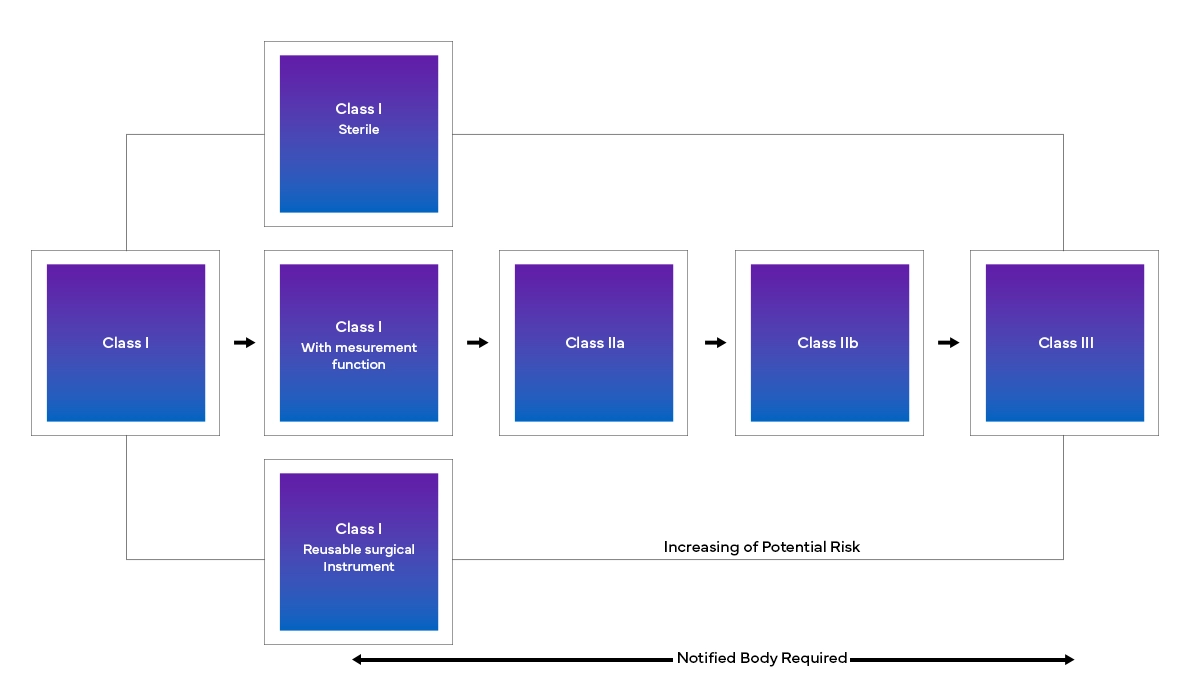
Desde la identificación de los cambios exactos que deben realizarse hasta su implementación en tiempo real, los fabricantes pueden tener que navegar por una serie de desafíos para cumplir con los requisitos del MDR de la UE. Desde descifrar la nueva estructura, clasificar un dispositivo con precisión, hasta recopilar y enviar todos los datos, se requerirá un enfoque reglamentario más detallado y transversal para los fabricantes, a fin de hacer frente a la nueva Reglamentación Europea de Dispositivos Médicos. Con un riguroso análisis de brechas, Freyr ayuda a los clientes con la situación actual y, de este modo, proporciona las medidas reglamentarias necesarias para la transición y el cumplimiento del MDR de la UE.
Obtenga asesoramiento experto sobre su cumplimiento con el EU MDR
Servicios de Cumplimiento de EU MDR
- Desarrollar una clara estrategia de implementación del Reglamento de Dispositivos Médicos (MDR)
- Comprender la nueva legislación, realizar un análisis de brechas respecto a los sistemas de gestión de calidad (SGC) y procesos actuales
- Desarrollar un plan detallado con un enfoque interfuncional para determinar los aspectos del sistema de calidad que necesitarán modificación en el ámbito del nuevo Reglamento de Dispositivos Médicos de la UE
- Formar múltiples equipos para analizar el alcance del producto, la clasificación, la gestión del SGC, etc., dentro de la organización, con un único punto de contacto en cada equipo
- Asignación y planificación de recursos
- Considerar la interacción de su SGC con otras regulaciones y aprovechar esta oportunidad para optimizar los procesos, al tiempo que se permite flexibilidad para incorporar cambios futuros
- Analizar los datos de prueba existentes y verificar cualquier requisito adicional que el MDR establezca
- Coordinación de expectativas y plan de transición con sus Organismos Notificados de la UE
- Análisis de Brechas para Dispositivos Médicos existentes desde la Directiva de Dispositivos Médicos de la UE (EU MDD) hasta los Reglamentos EU MDR
- Soporte End-to-End para desarrollar el Informe de Evaluación Clínica (CER), incluyendo la búsqueda bibliográfica según las directrices del Reglamento Europeo de Dispositivos Médicos (EU MDR).
- Servicios End-to-End para Informes de Vigilancia Post-comercialización (PMSR), Informes Periódicos de Actualización de Seguridad (PSUR) y Resúmenes de Seguridad y Rendimiento Clínico (SSCP)
- Refuerzo de recursos reglamentarios con opciones de despliegue tanto locales como externas
- Servicios de Representante Autorizado Europeo (EAR)
- Cumplimiento de la MDR y asistencia para la presentación a los Organismos Notificados
- Inteligencia reglamentaria que cubre el proceso de importación de diferentes mercados regulados
- Cumplimiento del SGC y auditorías simuladas
- Sistema de Gestión Documental y herramienta para empresas de MDR
- Clasificación y reclasificación de dispositivos según el riesgo
- Implementación y consultoría de UDI
- Servicios de vigilancia post-comercialización conformes con el Reglamento de Dispositivos Médicos de la UE
- Consultoría en Gestión de Riesgos ISO 14971
- Formación interna y en línea
- Persona responsable de los servicios y asistencia de cumplimiento reglamentario
- Identificación de Organismos Notificados MDR

Para soporte reglamentario End-to-End en EU MDR, contacte con Freyr.








