Descripción general del Informe de Validez Científica (IVC)
El Informe de Validez Científica (IVC) tiene una importancia primordial dentro del Informe de Evaluación del Rendimiento (IER) para los Dispositivos para Diagnóstico In Vitro (DPIV), según el Reglamento de Dispositivos para Diagnóstico In Vitro de la Unión Europea (EU IVDR) 2017/746. El IVC desempeña un papel crucial en la validación científica del rendimiento analítico y clínico del dispositivo, garantizando la seguridad y eficacia de los Dispositivos Médicos disponibles en el mercado. Dentro del proceso de evaluación de la conformidad prescrito por el EU IVDR, los fabricantes deben presentar un IER, que debe incluir un IVC, a un organismo notificado para demostrar la seguridad y el rendimiento del dispositivo antes de su introducción en el mercado de la UE.
Informes de Validez Científica para la Presentación al EU IVDR
- Análisis y Conclusiones
¿Qué incluye el contenido del Informe de Validez Científica (IVC)?
La validez científica de un analito significa la asociación de un analito con una condición clínica o un estado fisiológico. La validez científica de un DPIV se basa principalmente en una o una combinación de las siguientes fuentes:
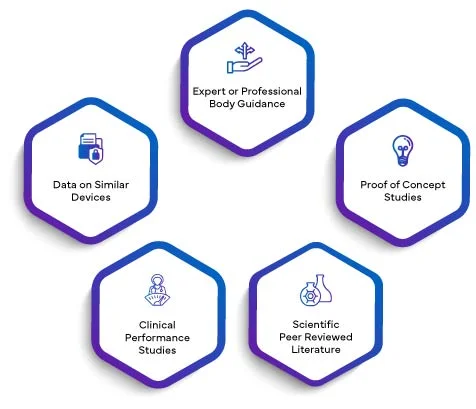
Los datos de todo lo anterior, según corresponda, se redactarán en un informe de validez científica. Al integrar el SVR en el PER, los fabricantes elevan su evaluación de rendimiento a un nivel superior de credibilidad. La validez científica establecida a través del SVR dota al PER de una base sólida, mejorando su calidad y significado generales. Esto, a su vez, infunde confianza en los organismos reglamentarios, los profesionales de la salud y los usuarios finales, asegurando que el rendimiento del IVD sea evaluado y validado meticulosamente de acuerdo con los estrictos requisitos del Reglamento IVDR (UE) 2017/746.
Freyr ofrece asistencia integral en la preparación de un sólido Informe de Validez Científica (SVR) para IVD, lo que le permite navegar con confianza por el panorama reglamentario e introducir sin problemas dispositivos IVD seguros y eficaces en el mercado.
Informe de Validez Científica
- Plan de transición para el cumplimiento del Reglamento sobre DIV.
- Informe de Validez Científica (IVC) basado en la literatura y/o datos internos.
- Informes de Rendimiento Clínico (CPR) basados en la literatura y/o datos internos.
- Informes de Rendimiento Analítico (APR)
- Evidencia clínica o informes de evaluación del rendimiento según el IVDR.
- Plan de Evaluación del Rendimiento.
- Protocolos e informes de Seguimiento del Desempeño Post-Comercialización (PMPF).
- Protocolos e informes de Vigilancia Post-Comercialización (PMSR).
- Redacción/Revisión de otros documentos, como prospectos/instrucciones de uso (IFU), Instrucciones de Referencia Rápida (QRI), manual de operación/usuario, etc.

- Cumplimiento garantizado con las normativas reglamentarias aplicables más recientes.
- Equipo de expertos cualificados
- Soluciones personalizadas a sus requisitos
- Gestión de recursos reglamentarios / Servicios de aumento de personal
- Aportaciones interfuncionales de expertos en Dispositivos Médicos para cumplir con los requisitos.

Preguntas Frecuentes.
01. ¿Qué es un Informe de Validez Científica (SVR) según el Reglamento IVDR de la UE?
El Informe de Validez Científica (SVR) documenta la evidencia que vincula un analito a una condición clínica o estado fisiológico y es una parte fundamental del Informe de Evaluación del Rendimiento (PER) requerido según el Reglamento IVDR 2017/746 de la UE para dispositivos IVD. Demuestra que la base científica del dispositivo está respaldada por la literatura o los datos de estudios, asegurando la seguridad y eficacia del dispositivo.
02. ¿Por qué el SVR es fundamental en la Evaluación del Rendimiento para los IVD?
El SVR es fundamental en la Evaluación del Rendimiento porque establece la validez científica del IVD al demostrar la asociación entre el analito y la condición clínica o el estado fisiológico. Proporciona la base científica para el propósito previsto del dispositivo y sustenta las declaraciones de rendimiento clínico. Un SVR sólido fortalece el Informe de Evaluación del Rendimiento (PER) general, lo que permite a los Organismos Notificados evaluar si el uso del dispositivo está clínicamente justificado, es seguro y cumple con el Reglamento de Diagnóstico In Vitro.
03. ¿Qué tipos de evidencia respaldan la validez científica en un SVR?
La validez científica se establece típicamente a través de múltiples fuentes de evidencia, como literatura revisada por pares, estudios clínicos, datos de comparación de dispositivos y puntos de referencia establecidos del estado del arte que vinculan de manera sólida el analito a la condición clínica.
04. ¿En qué se diferencia el SVR de los Informes de Rendimiento Analítico y Clínico?
El SVR se centra en establecer la base científica de la asociación de un analito con una condición clínica, mientras que los Informes de Rendimiento Analítico evalúan la precisión de la medición y los Informes de Rendimiento Clínico evalúan los resultados del rendimiento en el mundo real. Juntos, estos forman el PER completo.
05. ¿Cuándo deberían los fabricantes empezar a planificar el SVR?
Los fabricantes deberían planificar el SVR en las primeras etapas del desarrollo, idealmente junto con la planificación de la evaluación del rendimiento, para alinear el contexto clínico, la estrategia de revisión de la literatura y las expectativas reglamentarias, minimizando la reelaboración y asegurando un sólido respaldo de datos.
06. ¿Cuáles son los desafíos comunes en la preparación de un Informe de Validez Científica?
Los desafíos clave incluyen definir el contexto clínico previsto, seleccionar la literatura relevante, asegurar la calidad de la evidencia y sintetizar conclusiones que justifiquen claramente la validez científica para el escrutinio reglamentario. A menudo se requieren estrategias expertas y técnicas de revisión sistemática.
07. ¿Cómo apoya el SVR las presentaciones reglamentarias a los Organismos Notificados?
Un SVR bien elaborado eleva la calidad del Informe de Evaluación del Rendimiento al articular claramente la evidencia y el razonamiento, facilitando así una evaluación de la conformidad más fluida y aumentando la confianza de los revisores reglamentarios en la base científica del IVD.
08. ¿Por qué Freyr es considerado un socio líder para los servicios de Informes de Validez Científica?
Freyr aporta una profunda experiencia reglamentaria y un enfoque estructurado para la preparación del SVR según el Reglamento IVDR de la UE, lo que permite a los fabricantes abordar con confianza los complejos requisitos de evidencia mientras reducen el riesgo de tiempo hasta la presentación. La entrega probada en diversas carteras de IVD subraya el papel de Freyr como socio de confianza en la excelencia reglamentaria.








