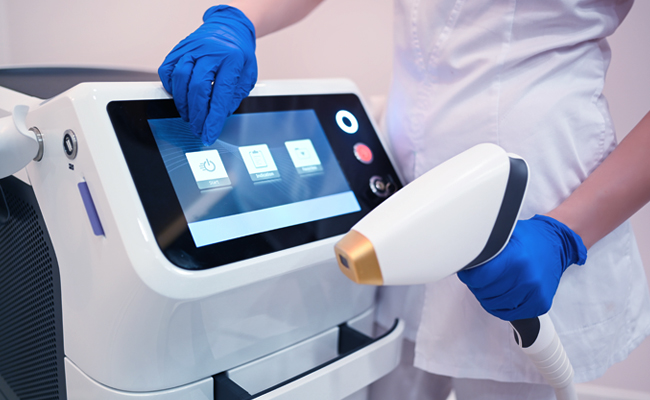
Resumen del eSTAR de la FDA
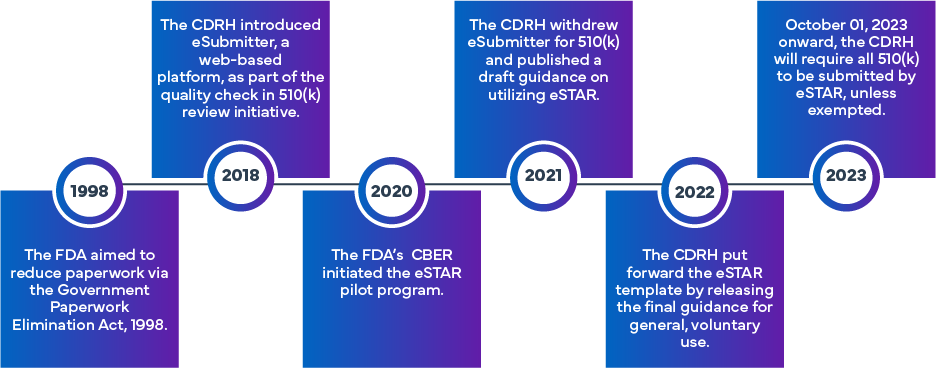
La iniciativa FDA se creó para mejorar la eficiencia y la uniformidad en la preparación y evaluación de las solicitudes FDA (k), De Novo y PMA FDA . A partir del enfoque inicial de eSubmitter, que implicaba la presentación electrónica de solicitudes de productos sanitarios y de diagnóstico in vitro, se estableció el programa eSTAR, aprovechando la experiencia previa FDA. La FDA un programa diferente denominado Programa Piloto de Plantillas y Recursos de Presentación Electrónica (eSTAR). Las solicitudes 510(k) deberán presentarse obligatoriamente a través de eSTAR a partir del 1 de octubre de 2023; las solicitudes De Novo (salvo que estén exentas) deberán presentarse obligatoriamente a través de eSTAR a partir del 1 de octubre de 2025. Las plantillas están disponibles en línea, aunque requieren el uso de credenciales FDA para el proceso de presentación propiamente dicho.
¿Qué es el FDA eSTAR?
El eSTAR es una plantilla PDF interactiva diseñada para facilitar la preparación de una solicitud completa Dispositivos Médicos ante la FDA Además, los solicitantes pueden utilizar el eSTAR para enviar respuestas a las solicitudes de información adicional FDA. Su objetivo es mejorar la calidad de las solicitudes de diversos dispositivos médicos, garantizando que los solicitantes proporcionen datos completos y de alta calidad para la revisión previa a la comercialización FDA.
Al adoptar el formato eSTAR, los solicitantes pueden estar seguros de que sus solicitudes están completas, lo que, a su vez, permitirá FDA la FDA las revisiones previas a la comercialización de manera más eficiente y garantizar el acceso oportuno a productos sanitarios seguros y eficaces. La plantilla eSTAR está disponible de forma gratuita y puede ser utilizada por todos Dispositivos Médicos para las presentaciones 510(k) y De Novo, así como de forma voluntaria para las presentaciones Q y las presentaciones complementarias de notificación de 30 días de la PMA a la FDA. Existen dos tipos de plantillas eSTAR: una para dispositivos médicos y otra para IVD. PreSTAR beta ha evolucionado; utilice las últimas plantillas de presentación Q a través del Portal de Colaboración con el Cliente (CCP) del CDRH. La plantilla eSTAR 6.0 para De Novo/510(k) no IVD se publicó en octubre de 2025.
Características y limitaciones de las presentaciones eSTAR.
Si bien el programa eSTAR ofrece un formulario PDF interactivo diseñado para ayudar a los solicitantes a elaborar presentaciones exhaustivas de Dispositivos Médicos y DIV, presenta ventajas y desventajas. Los solicitantes deben comprender estos beneficios y limitaciones, en función de los cuales pueden tomar decisiones bien informadas sobre la integración de eSTAR en su proceso de presentación. En la siguiente tabla, exploraremos los atributos y restricciones del programa eSTAR.

Consideraciones para un uso eficaz de eSTAR.
Una característica ventajosa de la plantilla eSTAR, que contribuye a la optimización del proceso de presentación, es su incorporación automatizada de reglamentos pertinentes y normas reconocidas para la citación. Esto no solo acelera el proceso de presentación al reducir la entrada manual de datos, sino que también mitiga la posibilidad de errores humanos que podrían ocurrir durante la introducción de reglamentos y normas. Mediante una construcción guiada para cada sección de presentación, la utilización de eSTAR en el proceso de presentación puede simplificarse sin esfuerzo.
- La FDA sugiere Adobe Acrobat Pro o Foxit PDF Editor para editar las plantillas eSTAR.
- eSTAR incluye ciertos formularios integrados, lo que elimina la necesidad de completarlos por separado. Estos incluyen el Formulario 3514 (la hoja de portada de la presentación) y el Formulario 3881 (indicaciones de uso). Además, la declaración veraz y precisa, que antes se requería en el membrete de una empresa, ahora está integrada en eSTAR.
- eSTAR admite varios formatos de archivo adjunto más allá de solo PDFs, como hojas de cálculo de Excel y archivos de vídeo (mp4).
- Los archivos en formatos habilitados para macros y ejecutables no están permitidos.
- El tamaño total del archivo PDF eSTAR, junto con sus archivos adjuntos, no debe exceder 1 GB, ya que los archivos de más de 4 GB no serán aceptados.
- Si sus archivos electrónicos superan los límites técnicos, puede enviar la presentación digital al Centro de Control de Documentos (DCC) de la CDRH por correo.
Mejores prácticas para preparar presentaciones eSTAR
Seguir algunas de las mejores prácticas para preparar las presentaciones eSTAR puede ayudar a los solicitantes a agilizar el proceso de presentación y mejorar sus posibilidades de un resultado exitoso. A continuación, se presentan algunas de las mejores prácticas:
- Siga las FDA de FDA :La FDA directrices para ayudar a los solicitantes a utilizar correctamente la plantilla eSTAR. Seguir estas directrices garantiza que las solicitudes se ajusten a los requisitos y expectativas FDA.
- Asegúrese de que la solicitud esté completa:la plantilla eSTAR guía a los solicitantes a través de la información esencial para la presentación. Los solicitantes deben proporcionar todos los datos requeridos para minimizar la posibilidad de que se produzcan deficiencias o se solicite información adicional.
- Mantener la coherencia:La plantilla eSTAR fomenta la uniformidad en el contenido y la estructura de las solicitudes 510(k). Las instrucciones de cumplimentación para cada sección de la solicitud ayudan a recopilar información sobre los Dispositivos Médicos.
- Priorice la claridad:facilite datos claros y concisos en las solicitudes presentadas a través de eSTAR para agilizar el proceso de revisión. Esa precisión y detalle minimizan los retrasos y los errores, además de garantizar un acceso oportuno a las solicitudes previas a la comercialización de productos sanitarios.
- Precisión garantizada:la verificación automática de la información de cada sección de las solicitudes presentadas a través de eSTAR contribuye a reducir los retrasos en la revisión y a evitar posibles deficiencias.
Importancia de la codificación por colores en la presentación eSTAR de la FDA.
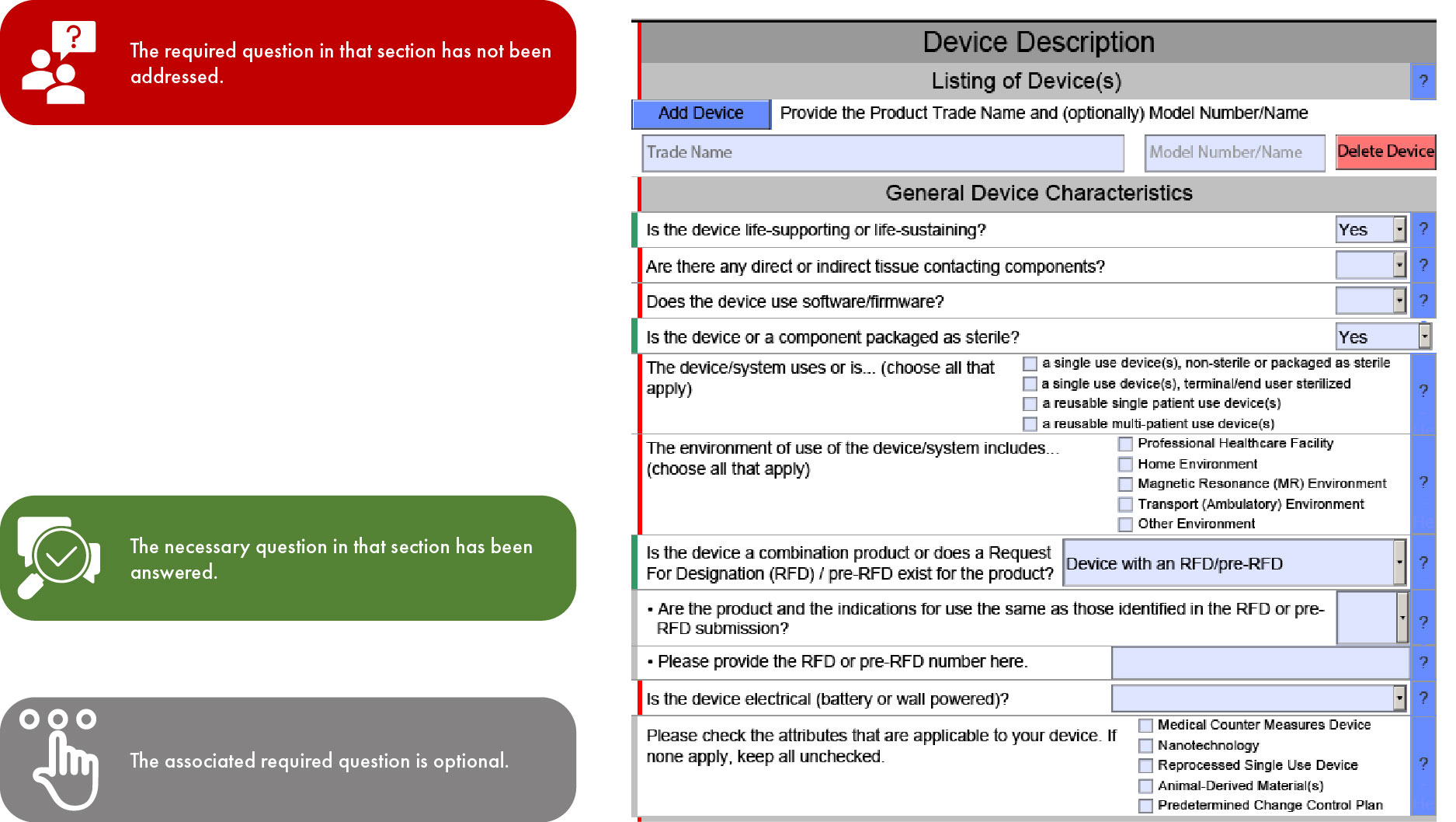
eSTAR será obligatorio para las solicitudes 510(k) a partir del 1 de octubre de 2023 y para las solicitudes De Novo a partir del 1 de octubre de 2025; el orden en que se completan las secciones de la plantilla viene determinado por el tipo de solicitud. Esta simplificación facilita una revisión más rápida por parte deFDA US , lo que minimiza las inconsistencias y omisiones en su solicitud. Sin embargo, es importante tener en cuenta que la FDA retrasar su revisión si faltan las traducciones al inglés de la documentación proporcionada.

Alinear sus archivos adjuntos
Examine la plantilla eSTAR con antelación para entender cómo se dividen los anexos y asegurarse de que sus documentos se ajusten a las secciones correspondientes. Este paso es crucial, especialmente para las empresas con presentaciones 510(k) anteriores, ya que su enfoque actual para la organización de documentos podría requerir ajustes. Incluso podría implicar la extracción de contenido de los anexos.
- eSTAR requiere anexos concisos, que difieren de las presentaciones tradicionales.
- Espere numerosos anexos, potencialmente docenas de ellos.
- Los archivos adjuntos permiten la inclusión de datos como hojas de cálculo de Excel, archivos de vídeo MP4, documentos de Word, archivos JPEG, etc.
- eSTAR requiere números de página para la información adjunta, pero no sugiere usar una lista de verificación de rechazo de aceptación para la orientación de la FDA.
Plantillas: ya están disponibles las plantillas de la última versión 6.0; se aceptan las de la versión 5 para los envíos en curso: fda.
El futuro de eSTAR
Se espera que eSTAR se actualice cuando se finalicen los documentos de orientación aplicables y exhaustivos. Con estas actualizaciones, el fabricante podrá consultar las versiones más recientes publicadas por la FDA de US.
Health Canada (HC) ha introducido una iniciativa piloto para emplear eSTAR para Dispositivos de Clase III y IV. Existe la conjetura de que otras naciones podrían seguir el ejemplo de Canadá al hacer que la adopción de eSTAR sea discrecional, particularmente dentro del consorcio IMDRF. Sin embargo, cabe señalar que no ha habido declaraciones explícitas al respecto.
¿Por qué elegir a Freyr?
Freyr cuenta con una vasta experiencia obtenida de su participación en numerosos proyectos centrados en presentaciones a la FDA en el pasado. Al presentar vías duales para ayudar proactivamente a la industria a acelerar las presentaciones 510(k) y De Novo, Freyr ofrece una gama de servicios al cliente que abarcan una lista completa de documentos de presentación esenciales e información requerida, la realización de análisis de brechas meticulosos en la documentación, la compilación de presentaciones a través de eSTAR y la finalización del paquete de presentación previa a la comercialización a la FDA. Además, Freyr extiende su apoyo a las actividades posteriores a la presentación, como proporcionar información adicional y revisar las respuestas de la industria a cualquier solicitud de información complementaria planteada por la FDA.
¿Cómo Ayudará Freyr?
Freyr ofrece soporte que puede ser útil para prepararse para las presentaciones 510(k) y De Novo. Los servicios incluyen:
- Soporte para la vía normativa: Esto implica identificar el código del producto, el nombre y número de la normativa, los posibles dispositivos de referencia/predicados, las pruebas de rendimiento, así como los estándares aplicables y los documentos de orientación pertinentes al dispositivo específico en cuestión.
- Soporte para Presentaciones Q (Pre-presentaciones): Esto implica ayudarle a aclarar dudas relacionadas con los requisitos previos de una presentación previa a la comercialización, organizar la presentación, prepararse para una reunión con la FDA, interactuar con la FDA durante la reunión de manera interactiva y redactar las actas de la reunión.
Experiencia en el programa eSTAR de la FDA
- Estrategia reglamentaria integral de la FDA.
- Identificación del dispositivo de referencia.
- Establecimiento de la equivalencia sustancial con el dispositivo de referencia.
- Análisis de Brechas para el cumplimiento de la FDA.
- Compilación de veintiuna (21) secciones del expediente técnico 510(k).
- Publicación y creación de la eCopy.
- Validación y envío del eCopy.
- Servicios de enlace para la aprobación de dispositivos.
- La gestión de la respuesta RTA y las deficiencias.
- Servicios de consulta para abordar deficiencias.
- Registro de Dispositivos y mantenimiento de la base de datos FURLS.