Servicios de Etiquetado Clínico - Resumen
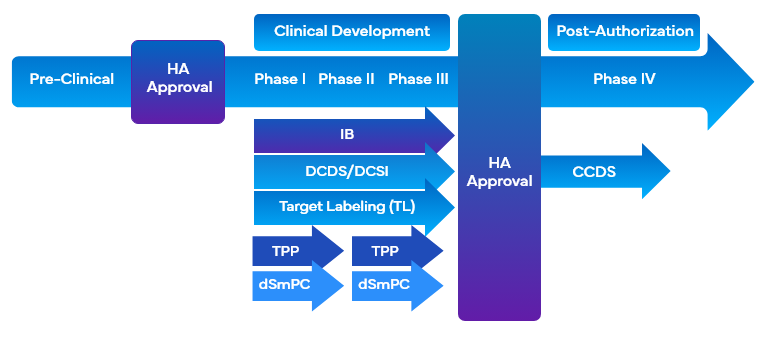
Durante el desarrollo de un fármaco, las empresas utilizan diversas herramientas relacionadas con el etiquetado clínico que recurren al etiquetado por objetivos para facilitar dicho desarrollo. Estas herramientas armonizan simultáneamente los objetivos deseados en materia de comercialización y de etiquetado de los ensayos clínicos con el diseño del programa o del estudio, y facilitan la redacción de la Sinopsis Clínica (CO). Algunas de las herramientas de etiquetado clínico que utilizan el etiquetado por objetivos durante el desarrollo de un fármaco son:
- Manual del Investigador (IB)
- Etiquetado objetivo (TL)/Perfil objetivo
- Hoja de Datos Central de Desarrollo (DCDS)
- Desarrollo de Información de Seguridad Central (DCSI)
- Perfil de Producto Objetivo de la FDA (TPP).
Es importante que las empresas empleen un enfoque modular al recopilar la información de seguridad y eficacia en varios tipos de etiquetas clínicas para complementar los requisitos de etiquetado clínico. Esto satisfaría la necesidad de ayudar a los investigadores y patrocinadores de manera efectiva al presentar y actualizar una sección DCSI enfocada y dedicada que pueda colocarse convenientemente bajo diferentes categorías clínicas.
Además, DCSI se incluye en la Información de Seguridad Central de la Compañía (CCSI), que es la base para la primera Ficha Técnica Central de la Compañía (CCDS) y se utiliza para la entrada del producto en el mercado. También se requiere la redacción de un CO exhaustivo que comprenda el alcance y los problemas críticos en el programa de desarrollo clínico del medicamento para respaldar la documentación para los evaluadores.
Servicios de Etiquetado Clínico de Freyr
Servicios de Etiquetado Clínico
Creación y revisión del Folleto del Investigador (IB)
Freyr cuenta con una amplia experiencia en la creación, redacción y revisión de prospectos de ensayo (IB) para diversos programas en fase clínica de nuestros clientes. Los folletos de investigación (IB) son la forma más básica de documentación destinada a proporcionar al investigador o al médico responsable del tratamiento información relevante sobre el fármaco o la intervención. Su objetivo es proporcionar a los investigadores y al resto de personas implicadas en el ensayo la información necesaria para facilitar su comprensión de los fundamentos del protocolo y su cumplimiento de muchos de sus aspectos clave. Entre estos se incluyen la dosis, la frecuencia o el intervalo de administración, los métodos de administración y los procedimientos de seguimiento de la seguridad. El IB información preclínica y clínica relacionada con un fármaco en fase de investigación.

Al trabajar en los IBs, los expertos en etiquetado clínico de Freyr presentan la información de forma concisa, sencilla, objetiva y equilibrada. Las mismas cualidades pueden considerarse también al traducir documentos. Además de redactar IBs, Freyr también apoya la revisión anual de los IBs y trabaja en las revisiones necesarias, en cumplimiento con los procedimientos estándar establecidos por clientes y patrocinadores.
Desarrollo de Etiquetado Objetivo (TL) / Perfil Objetivo
Desarrollo y revisión de DCDS y DCSI
Freyr tiene una experiencia probada en la creación de Hojas de Datos Centrales de Desarrollo (DCDS) de alta calidad. La DCDS es una etiqueta central intermedia vital para derivar contenido para las primeras etiquetas nacionales en presentarse (como USPI, SmPC, etc.). La DCDS/DCSI se prepara a partir de la etiqueta objetivo y proporciona seguridad y eficacia integradas a una intervención o fármaco. La DCDS/DCSI ayuda a los investigadores y patrocinadores presentando y actualizando secciones DCDS enfocadas y dedicadas que pueden colocarse convenientemente dentro del IB. La DCSI facilita el desarrollo de CCSI, que más tarde forma una parte integral de la Hoja de Datos Central de la Compañía (CCDS).
Desarrollo y revisión del Perfil de Producto Objetivo (TPP) de la FDA y del SmPC (dSmPC) borrador de la UE
El perfil del producto objetivo (TPP)/borrador del resumen de las características del producto (dSmPC) es un tipo de ficha técnica clínica que facilita el diálogo entre las empresas farmacéuticas y las autoridades sanitarias. El TPP se utiliza a lo largo de todo el proceso de desarrollo de un medicamento, desde las fases previas a la solicitud de un nuevo fármaco en investigación (IND) y la solicitud de un nuevo fármaco en investigación (IND) hasta los programas posteriores a la comercialización, con el fin de buscar nuevas indicaciones u otros cambios sustanciales en la ficha técnica de los ensayos clínicos. Las empresas farmacéuticas especifican los conceptos de etiquetado que constituyen los objetivos del programa de desarrollo del fármaco en forma de TPP. TPP ofrece una declaración de la intención general del programa de desarrollo del fármaco y proporciona información sobre el fármaco en una fase concreta del desarrollo. Como socio estratégico en materia de regulación, Freyr cuenta con experiencia en la preparación de TPP para EE US dSmPC para la UE.
- Recursos con conocimientos reglamentarios profundos en el envasado y etiquetado clínico.
- Experiencia en la gestión exitosa del etiquetado de medicamentos a nivel global y regional para clientes farmacéuticos de Fortune en los EE. UU., Europa, APAC, MENA, etc.
- Experiencia reglamentaria global para ayudar a organizaciones de ciencias de la vida, es decir, fabricantes farmacéuticos, biotecnológicos y de nutrición
- Redactores médicos altamente cualificados con amplia experiencia en etiquetado reglamentario.
- Conocimiento detallado y actualizado de los cambios introducidos en el etiquetado de los medicamentos a nivel mundial por diversas autoridades sanitarias, como laFDA US , EMA, la TGA, etc.
- Equipo de cumplimiento dedicado que rastrea el estado de la implementación de la hoja de datos central y de la hoja de datos central de la empresa (CDS/CCDS) en las etiquetas regionales
- Experiencia en el etiquetado de ensayos clínicos y servicios de etiquetado clínico.
- Profesionales altamente experimentados en etiquetado farmacéutico, biotecnológico y nutricional.









