Servicios de Cumplimiento, Auditoría y Validación - Resumen
¿Cumple con la normativa? Esta es una pregunta a la que cualquier empresa del sector farmacéutico, biotecnológico, genómico, químico, Dispositivos Médicos y de gestión de la cadena de suministro tiene dificultades para responder. Estas organizaciones deben cumplir con estrictos requisitos de calidad, seguridad y cumplimiento normativo en cada zona geográfica en la que se distribuyen sus productos. La tendencia actual en la gestión del cumplimiento normativo se encamina hacia la armonización global de la calidad y la seguridad, haciendo hincapié en prácticas sólidas. Tanto si es fabricante como proveedor, su expansión en el mercado, la mejora continua y la satisfacción del cliente dependen principalmente de los estándares de calidad de su negocio. El Centro de Excelencia (CoE) de Cumplimiento Normativo, Auditoría y Validación de Freyr puede ayudarle en este esfuerzo, prestándole servicios profesionales de cumplimiento, auditoría y validación para los sectores farmacéutico, de dispositivos médicos, de consumo y sanitario, tales como cGMP (Buenas Prácticas de Fabricación Actuales), GCP Buenas Prácticas Clínicas), GDP Buenas Prácticas de Distribución), Buenas Prácticas de Laboratorio (GLP), Buenas Prácticas de Farmacovigilancia GPVP ) yValidación de Sistemas Informáticos GxP (CSV). Nuestro equipo de consultoría en cumplimiento normativo farmacéutico ofrece soluciones a medida para abordar sus retos específicos de cumplimiento.
Freyr ofrece servicios de cumplimiento normativo, auditoría y validación que incluyen la evaluación de sus requisitos y la aportación de sugerencias para los procesos empresariales, con el fin de garantizar la satisfacción del cliente. Mediante la elaboración de informes de auditoría de cumplimiento y nuestras estrategias de preparación, proporcionamos informes de cumplimiento y auditoría (análisis de deficiencias), que incluyen sugerencias de medidas correctivas y preventivas (CAPA) para evitar posibles observaciones 483 y conclusiones de auditorías de cumplimiento por parte de las autoridades reguladoras. La consultoría de cumplimiento normativo farmacéutico de Freyr también se extiende a la consultoría de cumplimiento de la automatización farmacéutica, garantizando que sus sistemas automatizados cumplan con las expectativas normativas en constante evolución. Nuestro enfoque integral de la gestión del cumplimiento garantiza que cada etapa del ciclo de vida de sus procesos sea supervisada y optimizada para su alineación con la normativa.
Ofrecemos servicios de cumplimiento normativo y validación para garantizar que todos sus procesos y productos cumplan con los requisitos de calidad, seguridad de la información y auditorías de cumplimiento normativo aplicables, tales como (entre otros) los siguientes:
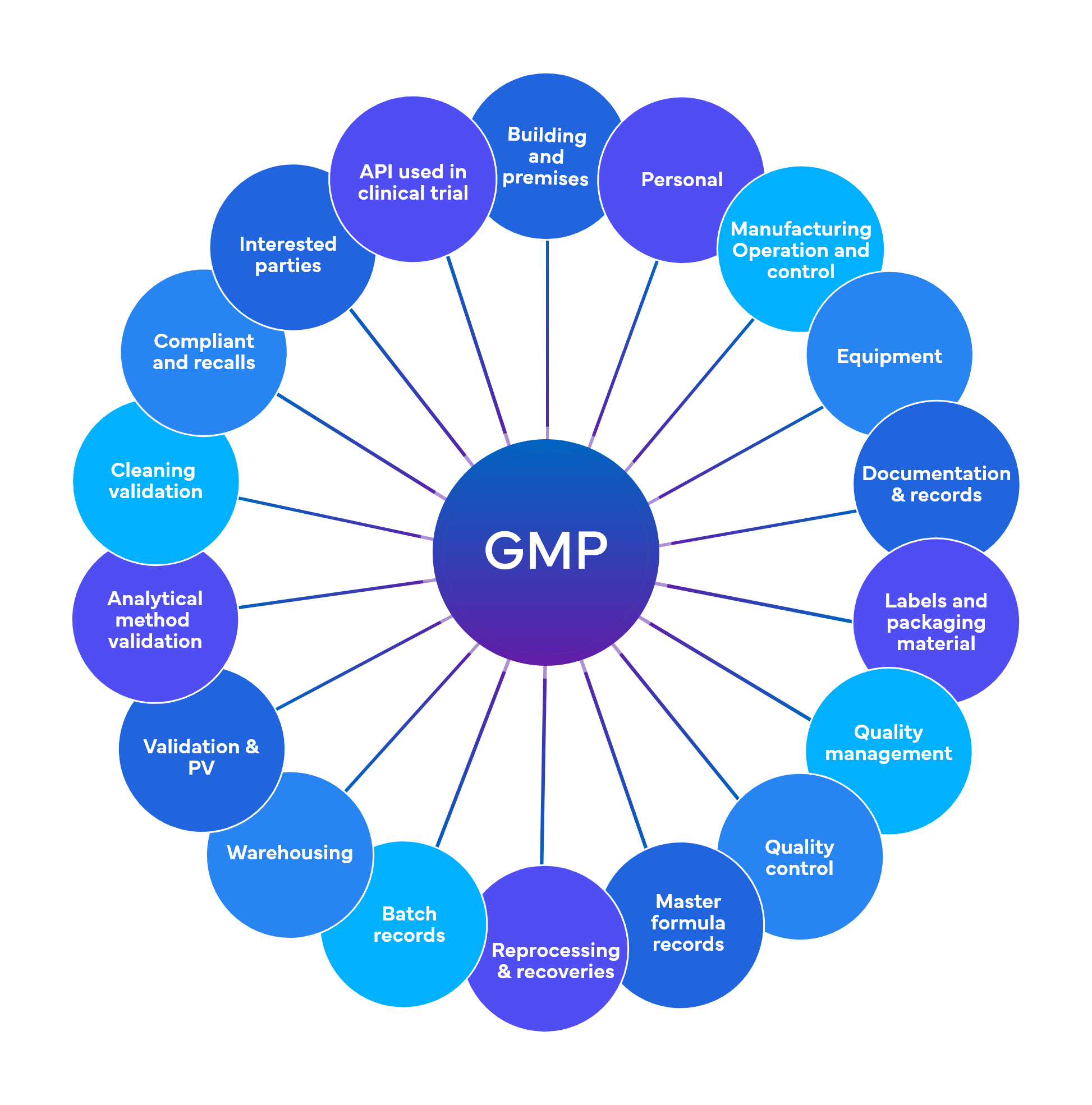
Freyr realiza alrededor de 700 verificaciones a nivel preliminar, distribuidas en 18-19 áreas funcionales de GMP.
Cumplimiento, auditoría y validación de Freyr
Servicios de cumplimiento, auditoría y validación
Calidad y Cumplimiento Reglamentario – Buenas Prácticas de Fabricación Actuales (cGMP)
- ISO / IEC 17025: 2017 - Requisitos generales para la competencia de los laboratorios de ensayo y calibración
- OCDE (Organización para la Cooperación y el Desarrollo Económicos) - Directrices de Buenas Prácticas de Laboratorio
- Guía EURACHEM / CITAC: Guía de Calidad en Química Analítica - Una Ayuda para la Acreditación, 3.ª edición (2016), debe seguirse en los procedimientos analíticos.
- 21 CFR 58: Buenas Prácticas de Laboratorio para Estudios de Laboratorio No Clínicos
- Guía de los Reglamentos GLP del Reino Unido, febrero de 2000 (por GLPMA)
- Manual WHO sobre Buenas Prácticas de Laboratorio (GLP): Prácticas de calidad para la investigación y el desarrollo no clínico reglamentado
- Health Canada: Documento de Orientación Finalizado - Datos de Estudios de Laboratorio No Clínicos que respaldan las Solicitudes y Presentaciones de Productos Farmacéuticos: Adherencia a las Buenas Prácticas de Laboratorio.
- Normas de OSHA (Occupational Safety and Health Administration)
- Directrices ICH aplicables
Buenas Prácticas de Laboratorio
- ISO / IEC 17025: 2017 - Requisitos generales para la competencia de los laboratorios de ensayo y calibración
- OCDE (Organización para la Cooperación y el Desarrollo Económicos) - Directrices de Buenas Prácticas de Laboratorio
- Guía EURACHEM / CITAC: Guía de Calidad en Química Analítica - Una Ayuda para la Acreditación, 3.ª edición (2016), debe seguirse en los procedimientos analíticos.
- 21 CFR 58: Buenas Prácticas de Laboratorio para Estudios de Laboratorio No Clínicos
- Guía de los Reglamentos GLP del Reino Unido, febrero de 2000 (por GLPMA)
- Manual WHO sobre Buenas Prácticas de Laboratorio (GLP): Prácticas de calidad para la investigación y el desarrollo no clínico reglamentado
- Health Canada: Documento de Orientación Finalizado - Datos de Estudios de Laboratorio No Clínicos que respaldan las Solicitudes y Presentaciones de Productos Farmacéuticos: Adherencia a las Buenas Prácticas de Laboratorio.
- normas de OSHA (Occupational Safety and Health Administration)
- Directrices ICH aplicables
Buenas Prácticas Clínicas (GCP) y Buenas Prácticas de Farmacovigilancia (GVP)
- Guía Tripartita Armonizada de ICH: Guía para las Buenas Prácticas Clínicas - E6
- Especificación del Informe Individual de Seguridad de Casos (ICSR) E2B(R3) y Archivos Relacionados
- Informe Periódico de Evaluación de la Relación Beneficio-Riesgo (PBRER) E2C(R2)
- Otras Directrices ICH Aplicables
- Directrices sobre los Módulos de Buenas Prácticas de Farmacovigilancia (GVP).
- Requisitos de la FDA para la notificación de seguridad en estudios IND y BA/BE
- Informes de seguridad poscomercialización para medicamentos de uso humano y productos biológicos, incluidas las vacunas
- Especificaciones de implementación regional de la FDA para la notificación ICH E2B(R3) al Sistema de Notificación de Eventos Adversos de la FDA (FAERS)
- Presentación de solicitudes en formato electrónico – Preguntas y respuestas técnicas sobre ICSRs poscomercialización no acelerados
- Planificación de Farmacovigilancia E2E
Seguridad de la Información, Privacidad de Datos y Validación de Sistemas Informáticos (CSV)
- ISO 27001: 2013 Tecnología de la Información – Técnicas de Seguridad – Sistema de Gestión de la Seguridad de la Información – Requisitos
- ISO 27002: 2013 Tecnología de la información – Técnicas de seguridad – Código de práctica para la gestión de la seguridad de la información
- USFDA 21 CFR Part 11: Registros electrónicos; Firmas electrónicas – Alcance y aplicación
- Anexo 11 de la Guía GMP de la UE
- Notificación de la Directriz ERES japonesa n.º 0401022
- GAMP 5: Un Enfoque Basado en Riesgos para Sistemas Informatizados GxP Conformes
- USFDA – Directrices de validación de software
- Directrices ICH QSEM aplicables
- Planificar y crear SOPs y controlar las instalaciones de fabricación
- Modelo de proceso integrado.
- Mantener la imagen de marca
- Servicios de evaluación de riesgos
- Ahorro general de costes
- Implementar procesos de negocio eficaces y conformes
- Establecer estrategias de validación y cualificación
- Experiencia en cumplimiento reglamentario y de auditorías
- Auditores expertos en cumplimiento
Nuestro enfoque de consultoría en materia de calidad y cumplimiento normativo está diseñado para ofrecer información útil y mejoras sostenibles, con el fin de ayudar a su empresa a alcanzar la excelencia operativa y el cumplimiento normativo.



 Servicios de cumplimiento y auditoría
Servicios de cumplimiento y auditoría










