Resumen de Productos Combinados de Dispositivos Médicos
En el dinámico mundo de la atención médica y la innovación, los productos combinados de Dispositivos Médicos se han convertido en un puente sólido que conecta productos farmacéuticos, Dispositivos Médicos y productos biológicos. El mercado de productos combinados está en auge, con una Tasa de Crecimiento Anual Compuesta (CAGR) prevista del 8,9% de 2023 a 2030. El sector de productos combinados de fármacos y dispositivos está preparado para un crecimiento sostenido, impulsado por los avances tecnológicos, la mejora de la infraestructura sanitaria, rutas reglamentarias más fluidas, colaboraciones estratégicas y un compromiso con la atención centrada en el paciente.
Diferentes tipos de Productos Combinados
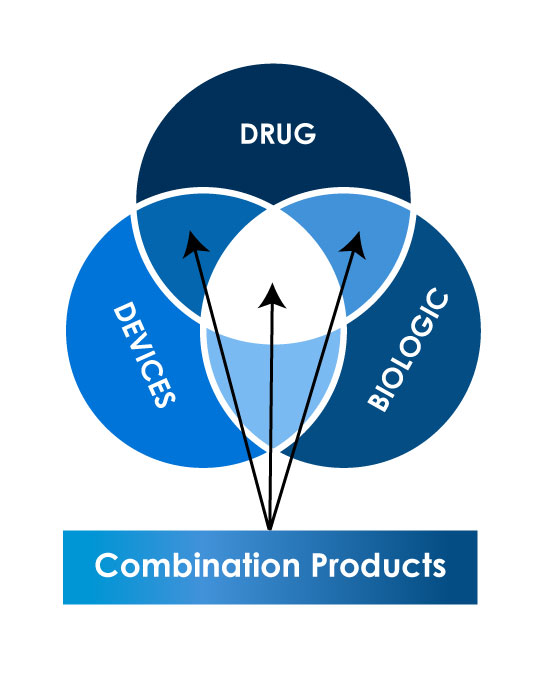
Escenario reglamentario global para el registro de productos combinados
La interpretación de lo que constituye un producto combinado puede diferir de una nación a otra, lo que aumenta las complejidades del registro de dichos productos en varios países. Además, las exigencias y procedimientos reglamentarios para los productos combinados pueden presentar variaciones en la documentación, la comunicación y la validación. El panorama reglamentario para el registro de productos combinados puede diferir significativamente en todo el mundo. A continuación, se presentan las principales Autoridades Reglamentarias que supervisan globalmente estos dispositivos.
| País | Agencia | Centros principales para aprobación |
|---|---|---|
| EE. UU. | Office of Combination Products (OCP) | Centro de Evaluación e Investigación de Medicamentos (CDER) |
| Centro de Evaluación e Investigación de Productos Biológicos (CBER) | ||
| Centro de Dispositivos y Salud Radiológica (CDRH) | ||
| UE | Organismos Notificados (NBs) | Autoridad Nacional Competente (productos medicinales) |
| Organismos Notificados (NBs) (Dispositivos Médicos) | ||
| Japón | División de Evaluación y Licencias o la Oficina de Dispositivos Médicos/Productos Celulares y Tisulares de la Oficina de Seguridad Farmacéutica y Alimentaria | Director de la División de Evaluación y Licencias (DMDL), Oficina de Seguridad Farmacéutica y Alimentaria, Oficina de Seguridad Farmacéutica y Médica, Ministerio de Salud y Bienestar |
| China | Centro de Administración de Estandarización de Dispositivos Médicos (CMDSA) | Centro de Evaluación de Dispositivos Médicos (CMDE) |
| Centro de Evaluación de Medicamentos (CDE) | ||
| Malasia | Agencia Nacional Reguladora Farmacéutica | Agencia Nacional Reguladora Farmacéutica (NPRA) |
| Agencia de Dispositivos Médicos |
El registro de productos combinados en los mercados internacionales requiere un enfoque personalizado, que implica una estrecha colaboración con las Agencias de Salud pertinentes para su aprobación. El proceso habitual para el registro de productos combinados incluye los siguientes pasos:
- Evaluar si un dispositivo específico cumple los criterios para su clasificación como producto combinado.
- Clasificación de los dispositivos según los riesgos asociados.
- Identificación de las normas pertinentes y los requisitos de datos especificados por la Agencia de Salud correspondiente.
- Generación de los datos necesarios según lo exigido por la Agencia.
- Compilación de un expediente técnico de acuerdo con los requisitos específicos de cada país.
- Presentación de la solicitud y resolución de cualquier consulta o preocupación hasta la obtención de la aprobación.
- Gestión del ciclo de vida del dispositivo después de la aprobación.
Nuestras Competencias
- Análisis de riesgo inicial
- Investigación de mercado - Conocimientos de mercado específicos del producto
- Ampliación de plantilla
- Estrategia reglamentaria preliminar.
- Mercados y vías potenciales.
- Expediente de diseño y análisis de riesgos.
- Sistema de Gestión de Calidad (SGC) ISO 13485
- Programa de Auditoría Única de Dispositivos Médicos (MDSAP)
- Preevaluación de QMS ISO 13485
- Estrategia reglamentaria
- Freyr IMPACT (Plataforma de Inteligencia Reglamentaria)
- Verificación y validación del diseño
- Gestión de riesgos
- Elaboración de documentación técnica
- Estrategia reglamentaria
- Requisitos reglamentarios
- Herramienta rDMS de Freyr (Sistema de Gestión de Datos/Documentación)
- Validación de procesos y clínica
- Etiquetado y Artwork final
- Representación en el país
- Presentación reglamentaria
- El marcado de Conformidad Europea (CE) de la Unión Europea (UE) y el marcado de Evaluación de Conformidad del Reino Unido (UKCA)
- Certificación de acceso al mercado global
- Apoyo para auditorías de Organismos Notificados (ON)/Organismos Aprobados
- Representación en el país
- Aprobaciones reglamentarias
- Vigilancia poscomercialización (PMS)
- Seguimiento Clínico Post-comercialización (PMCF)
- Mantenimiento anual del expediente técnico (CER/Gestión de Riesgos)
- Renovaciones reglamentarias
- Lanzamientos de nuevos productos al mercado
- Comunicación con la Autoridad Competente/Organismo Notificado/Aprobado
- Soluciones automatizadas de Farmacovigilancia (PV)
¿Por qué Freyr?
Registro de Dispositivos Médicos
- Estrategia reglamentaria integral para productos combinados.
- Soporte reglamentario para documentos de desarrollo de productos, como los Expedientes de Historial de Diseño (DHFs).
- Estrategia de cumplimiento de QMS.
- Cumplimiento reglamentario, análisis de brechas y subsanación de documentos técnicos y sistemas de calidad.
- Servicios de etiquetado reglamentario y redacción técnica.
- Servicios de inteligencia reglamentaria y de mercado.
- Servicios de traducción de documentos y etiquetado.
- Servicios de enlace con agencias de salud.
- Servicios de Artwork reglamentario.
- Servicios de Farmacovigilancia y PMS.
- Servicios de publicación.
- Servicios de redacción médica.

- Presentaciones exitosas para diversas clases de IVD.
- Personal dedicado y experto para proporcionar soporte reglamentario para Dispositivos Médicos e IVD.
- Entrega puntual de los resultados.
- Acceso a filiales locales para afrontar los desafíos de la Autoridad y los requisitos específicos del idioma.
- Soporte de representante local o legal con un modelo rentable.
- Servicios de gestión de recursos reglamentarios/refuerzo de personal.









