Cumplimiento normativo en materia de Dispositivos Médicos y regulación de Dispositivos Médicos en la UE
La Unión Europea constituye uno de los Dispositivos Médicos más regulados y comercialmente atractivos del mundo. Con 27 member states, 3 EEA y Turquía, el mercado de la Unión opera bajo un ecosistema normativo armonizado definido por EU MDR 2017/745) para los productos sanitarios y el Reglamento IVDR de la UE (2017/746) para los productos de diagnóstico in vitro, lo que garantiza unas normas uniformes de seguridad y rendimiento en todas las categorías de productos. Para comercializar legalmente un producto en el mercado de la Unión Europea, los fabricantes deben obtener el marcado CE, que confirma el cumplimiento de la normativa aplicable en función de la clasificación de riesgo del producto y la vía de evaluación de la conformidad. El incumplimiento de estos requisitos puede acarrear graves consecuencias, como la retirada del producto, la incautación en aduana, la suspensión de la certificación o la pérdida total del acceso al mercado.
Bajo el régimen regulatorio actual:
- El marcado CE es obligatorio para todos los productos sanitarios y los productos para diagnóstico in vitro antes de su comercialización.
- El registro de productos sanitarios en EUDAMED se está implantando por fases, y varios módulos ya están activos y son de uso obligatorio.
- El nombramiento de un representante autorizado europeo (EAR) es obligatorio para cualquier fabricante con sede fuera de la UE,EEA.
- Las normas de clasificación más estrictas del MDR y el IVDR exigen una documentación técnica sólida, pruebas clínicas o de rendimiento, y un seguimiento continuo a lo largo del ciclo de vida.
Freyr acompaña a los fabricantes a lo largo de todo este proceso, facilitándoles una entrada fluida y conforme a la normativa en el mercado de la Unión. Desde el desarrollo de una estrategia de marcado CE y la elaboración de la documentación técnica hasta la gestión de las solicitudes ante los organismos notificados y la actuación como su representante autorizado en la UE, Freyr garantiza el pleno cumplimiento de los Reglamentos MDR e IVDR y un acceso sin obstáculos a todos member states de la UE,EEA y Turquía.
Proceso paso a paso para el cumplimiento de la normativa de la UE
El acceso al mercado de los Dispositivos Médicos en la UE implica varias etapas bien definidas. Así es como Freyr gestiona todo el proceso por ti:
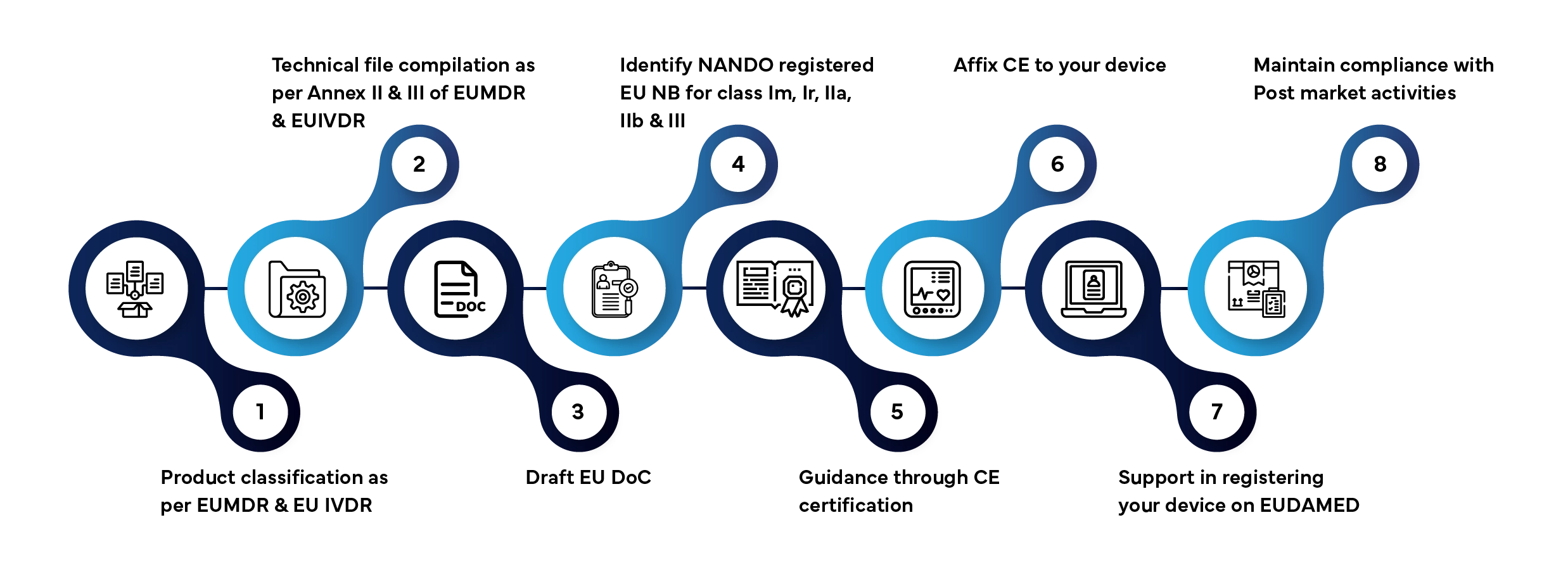
Plazo de tramitación habitual: entre 3 y 12 meses, dependiendo de la clase de dispositivo y de si la documentación está completa.
Oferta principal de Freyr Dispositivos Médicos
- Estrategia regulatoria y transición al MDR y al IVDR: elaboramos planes de acción end-to-end adaptados al EU MDR al IVDR EU MDR , garantizando una transición fluida desde los regímenes de las directivas y la adecuación a los requisitos actuales de la UE.
- Documentación técnica y evaluación de la conformidad: nuestro equipo le ayuda en la elaboración, revisión y presentación de sus expedientes técnicos y de diseño, le asesora en las gestiones con los organismos notificados y gestiona el marcado CE, las pruebas de seguridad y rendimiento de los productos sanitarios, así como los procedimientos de conformidad.
- Evaluación clínica y de rendimiento: Freyr ofrece servicios especializados de elaboración de informes de evaluación clínica (CER), informes de evaluación de rendimiento (PER), planes PMCF, informes periódicos de seguridad (PSUR), informes de supervivencia (SVR), informes de cumplimiento de requisitos (CPR) para productos sanitarios de diagnóstico in vitro, documentación de riesgos y contenidos de evaluación biológica, garantizando la claridad técnica y la precisión normativa en todas las clases de productos sanitarios.
- Asistencia para el registro en UDI y EUDAMED: nos aseguramos de que su sistema de identificación única de productos sanitarios (UDI) cumpla con la normativa y le ayudamos con el registro en la base de datos europea de productos sanitarios EUDAMED y con la gestión del ciclo de vida asociada.
- Representante autorizado europeo (EAR) y representación local: para los fabricantes fuera de laEEA, actuamos como su representante autorizado europeo (EAR) designado y ofrecemos asistencia en materia de cumplimiento normativo en todos member states la UE.
- Vigilancia poscomercialización (PMS): Freyr le ayuda a establecer, implementar y mantener sistemas de vigilancia poscomercialización, incluyendo el Plan de Vigilancia Poscomercialización (PMSP), el informe de vigilancia poscomercialización (PMSR), el informe periódico de actualización de seguridad (PSUR), los planes de seguimiento clínico y de rendimiento poscomercialización (PMCF), la notificación de vigilancia, las FSCAs, las FSNs y las CAPAs, garantizando el mantenimiento continuo del marcado CE y un acceso sostenible al mercado con el cumplimiento de los requisitos a lo largo del ciclo de vida del producto.
- Registro de dispositivos con marcado CE: Freyr gestiona todo el proceso de registro del marcado CE en la UE, prestando apoyo en la evaluación de la conformidad, elaborando la documentación necesaria, colaborando con los organismos notificados y garantizando la obtención de las autorizaciones a tiempo para todas las categorías Dispositivos Médicos de diagnóstico in vitro.
- Asistencia en sistemas de gestión de la calidad: Ofrecemos asistencia para la implantación y el mantenimiento de sistemas de gestión de la calidad ISO 13485, en consonancia con los requisitos de calidad y seguridad del Reglamento sobre productos sanitarios ( EU MDR del Reglamento sobre dispositivos médicos ( EU MDR, así como con las expectativas de los organismos notificados.
- Cumplimiento normativo en materia de etiquetado: Nuestro equipo se asegura de que su etiquetado, instrucciones de uso, embalaje y símbolos cumplan con los requisitos del Reglamento sobre productos sanitarios (MDR) y del Reglamento sobre dispositivos médicos para uso in vitro (IVDR), así como con los requisitos lingüísticos multilingües de la UE, garantizando la coherencia y el cumplimiento normativo en member states 27 member states de la UE.
Servicios de representante autorizado en la UE (EAR)
Registro de dispositivos ante las autoridades de la UE
Para los fabricantes no pertenecientes a la UE, Freyr actúa como representante autorizado en la UE (EAR) designado, de conformidad con los requisitos del MDR y el IVDR. Como entidad con sede en Alemania, Freyr presta apoyo en las actividades de registro de productos ante la autoridad competente alemana pertinente y mantiene los registros reglamentarios exigidos. En el caso de otros Member States la UE, Freyr ofrece asistencia en materia de normativa, según proceda, para ayudar a garantizar el cumplimiento de los requisitos aplicables a los productos y facilitar su comercialización en el mercado de la Unión.
Documentación y garantía de conformidad
Nuestros expertos en normativa comprueban que su declaración de conformidad (DoC), los certificados CE y los expedientes técnicos estén completos, actualizados y cumplan con el MDR y el IVDR. Freyr garantiza que todo esté listo para la evaluación de la conformidad y la solicitud del marcado CE.
Respuesta a las consultas de las autoridades competentes
Si es necesario, Freyr se encarga de gestionar en su nombre todas las comunicaciones directas y las solicitudes de aclaración de las autoridades competentes de la UE o de los organismos notificados, garantizando respuestas puntuales y precisas y contribuyendo a evitar retrasos en las aprobaciones o en las revisiones reglamentarias posteriores a la comercialización.
Vigilancia y comunicación de incidentes
En su calidad de EAR, Freyr actúa como principal enlace para las comunicaciones relacionadas con la seguridad. Cuando es necesario, coordinamos las notificaciones de incidentes, las medidas correctivas de seguridad en el terreno (FSCA) y los informes de vigilancia entre el fabricante, los profesionales sanitarios y las autoridades, con el fin de garantizar una respuesta adecuada y el cumplimiento de la normativa.
Preparación para inspecciones y auditorías
Freyr conserva toda la documentación, la correspondencia y los registros obligatorios para las auditorías e inspecciones de las autoridades. Nuestro equipo se asegura de que la documentación técnica, el etiquetado y los registros posteriores a la comercialización estén fácilmente disponibles y cumplan plenamente con los requisitos del MDR y el IVDR.
¿Por qué asociarse con Freyr?
- Experiencia End-to-end que abarca desde el registro previo a la comercialización hasta la vigilancia poscomercialización, gestionando todas las fases del cumplimiento normativo.
- Una trayectoria contrastada con más de 2000 registros de dispositivos completados con éxito en diversas categorías.
- Una sólida presencia en la UE con sede en Alemania (EAR), complementada por especialistas en normativa sobre el terreno en Reading y respaldada por los equipos de prestación de servicios globales de Freyr.
- Una planificación de la transición a medida que ofrece apoyo estratégico para obtener la certificación CE de forma fluida y rentable.
- Equipos de entrega multirregionales con apoyo sobre el terreno a través de las operaciones de Freyr en la UE, con sede en Alemania.
- Amplia experiencia en la adaptación a los requisitos del MDR y el IVDR y en la transición de dispositivos heredados
- Una gestión transparente del proyecto con comunicación directa con el organismo notificado












