Software como Dispositivo Médico (SaMD): Descripción general
El Software como Dispositivo Médico (SaMD) es el tema de mayor auge en el segmento de la atención médica. Se espera que el mercado de SaMD crezca a una Tasa de Crecimiento Anual Compuesta (CAGR) del 10,78 % a nivel mundial. Este crecimiento se debe a varios factores, como la adopción del Internet de las Cosas (IoT), las plataformas de atención médica digitales y la adopción de software para la monitorización continua de parámetros fisiológicos por parte de los proveedores de atención médica para asistencia remota. Sin embargo, este panorama prometedor también presenta desafíos únicos, uno de ellos es determinar si entra dentro de la categoría de Dispositivos Médicos y si cumple con los requisitos reglamentarios.
Diferentes tipos de Productos de Salud Digital
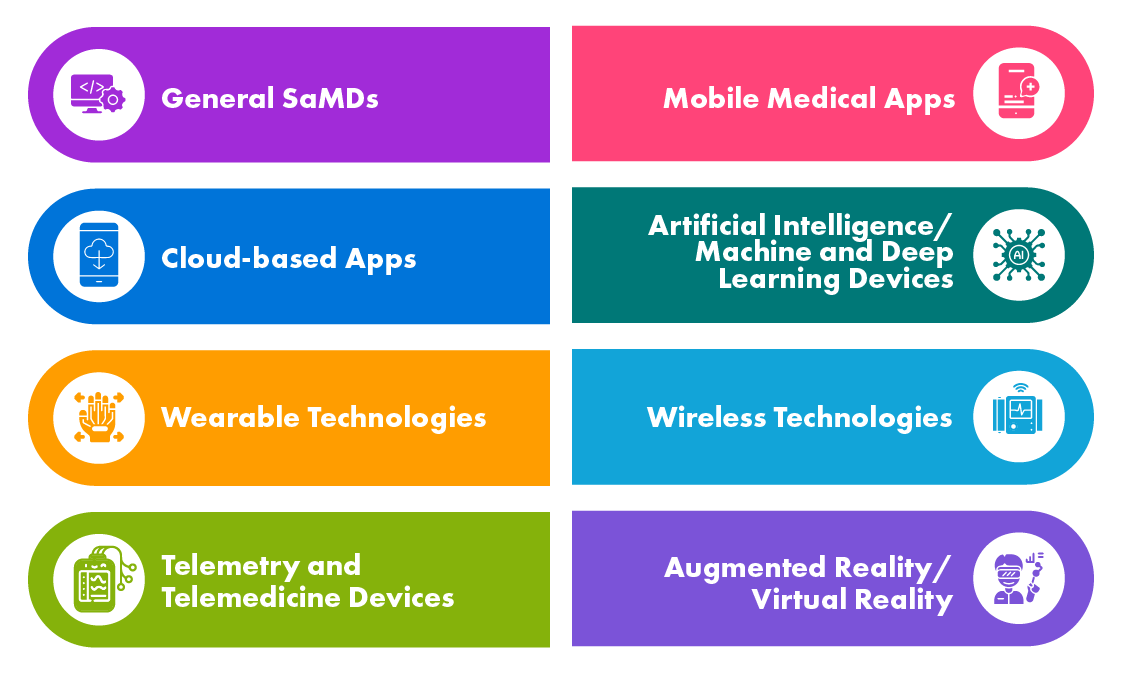
Escenario reglamentario global para el registro de Software como Dispositivo Médico (SaMD)
Los SaMD se utilizan en diversas aplicaciones como cribado y diagnóstico, monitorización y alerta, gestión de enfermedades, etc. Las Agencias de Salud de los países desarrollados como la UE, los US, Canadá y Australia han definido regulaciones en torno a los SaMD y algunas de ellas ya han desarrollado documentos de orientación, mientras que otras están en proceso.
Algunos mercados regulados y no regulados consideran el software como Dispositivos Médicos, pero no cuentan con directrices diferenciadas y específicas para la clasificación de Software como Dispositivo Médico (SaMD). Siguen las directrices armonizadas aceptadas internacionalmente para la evaluación y aprobación del software.
A continuación se enumeran algunas de las directrices destacadas disponibles sobre el Registro de Software como Dispositivo Médico (SaMD):
- Guía IMDRF para la clasificación, el Sistema de Gestión de Calidad (SGC), la evaluación de ciberseguridad y la evaluación clínica.
- El EU MDR 2017/745 ha detallado los requisitos reglamentarios y la orientación para esta categoría de Dispositivos Médicos.
- La guía del MDCG sobre la cualificación y clasificación de SaMD, los requisitos de Clinical Evaluation Reports (CER)/Informes de Evaluación de Rendimiento (PER) para SaMD.
- La guía de la FDA de US sobre ciberseguridad, evaluación clínica y requisitos de registro para diferentes tipos de software, como sistemas de decisión, sistemas de archivo y comunicación de imágenes (PACS), aplicaciones móviles, etc.
- Documento de orientación de Health Canada sobre la definición y clasificación de SaMD.
- Nuevas regulaciones de la TGA para dispositivos médicos basados en software.
El registro de SaMD en otros mercados globales se tratará caso por caso y requiere una estrecha interacción con la Agencia de Salud correspondiente para su aprobación. La vía general seguida para el registro de SaMD incluye:
- Determinar si un software determinado califica como SaMD.
- Clasificación de los dispositivos según el riesgo implicado.
- Identifique las normas aplicables y los requisitos de datos por parte de la Agencia de Salud correspondiente.
- Generar datos según lo exija la Agencia correspondiente.
- Compilación del expediente técnico según el requisito del país.
- Presentación y resolución de consultas hasta la aprobación.
- Gestión del ciclo de vida post-aprobación.
Nuestras Competencias
- Servicios de Inteligencia Regulatoria (relacionados con el Mercado + Soporte de Etiquetado)
- Debida Diligencia Reglamentaria / Informes de Estrategia
- Cualificación y clasificación de SaMD
- Solicitud de clasificación de producto a NB
- Análisis de Brechas
- Reuniones previas a la presentación con la FDA
- Identificación de Normas Aplicables
- Actividades de gestión de riesgos
- Apoyo a la gestión de riesgos
- Soporte de etiquetado
- Creación/revisión/actualización de procedimientos/plantillas específicos para SaMD
- UDI/GUDID
- Registro de productos (Registro de software)
- Registro de establecimiento
- Registro de Dispositivos
- Respuesta a consultas de la HA — servicios de SaMD
¿Por qué Freyr?
Preguntas Frecuentes (PF)
La reglamentación del software médico es supervisada por varios organismos reglamentarios globales, incluyendo la FDA en los Estados Unidos, la EMA en Europa y la PMDA en Japón. Estas agencias clasifican el software médico según el riesgo y establecen directrices para la seguridad, la calidad y la eficacia. Se requiere el cumplimiento de las normas ISO, como la ISO 13485 y la 62304.
Determinar la clasificación de riesgo del Software como Dispositivo Médico (SaMD) implica evaluar factores como el uso previsto y el daño potencial. Los SaMD se clasifican como Dispositivos Médicos tradicionales según la importancia de la información proporcionada para la toma de decisiones sanitarias y el estado de la situación o condición de salud como no grave, grave y crítica. Las directrices reglamentarias y la consulta de expertos son cruciales en este proceso, asegurando el cumplimiento y la seguridad del paciente.
SaMD se refiere al software destinado a ser utilizado para uno o más propósitos médicos, sin formar parte de un Dispositivo Médico físico. Opera en plataformas informáticas de uso general como teléfonos inteligentes, tabletas u ordenadores personales. Por otro lado, SiMD es un software que es un componente integral de un Dispositivo Médico físico, contribuyendo a su funcionalidad y rendimiento. SiMD no puede utilizarse de forma independiente y depende del Dispositivo Médico asociado para cumplir su propósito previsto.
Un software que está integrado como parte de un dispositivo médico de hardware y es necesario para cumplir el propósito médico previsto NO se considera un SaMD.
El plazo para lograr el cumplimiento de SaMD está influenciado por la clase de riesgo y el requisito reglamentario. Sin embargo, con la asistencia reglamentaria adecuada, puede garantizar un proceso de cumplimiento más fluido con riesgos mínimos.
Registro de Dispositivos Médicos
- Estrategia reglamentaria integral para SaMDs.
- Apoyo de inteligencia reglamentaria y de mercado.
- Servicios de clasificación y registro de productos para SaMDs.
- Soporte normativo para documentos de desarrollo de productos SaMD.
- Servicios de consulta sobre estudios de evaluación clínica de SaMD.
- Gestión de cambios post-aprobación.
- Servicio de representación local.

- Estrategia reglamentaria integral para SaMDs.
- Apoyo de inteligencia reglamentaria y de mercado.
- Servicios de clasificación y registro de productos para SaMDs.
- Soporte normativo para documentos de desarrollo de productos SaMD.
- Servicios de consulta sobre estudios de evaluación clínica de SaMD.
- Gestión de cambios post-aprobación.
- Servicio de representación local.









