Informe de evaluación clínica (CER) para Dispositivos Médicos: Descripción general
Cualquier producto destinado a su comercialización en la Unión Europea (UE) debe llevar el marcado CE. De conformidad con el EU MDR sobre productos sanitarios, los requisitos para el informe de evaluación clínica (CER), incluidos los requisitos relativos al proceso y a los datos, varían en función de la clase del producto y son necesarios para obtener la certificación CE de los productos sanitarios. Los productos de clase I de bajo riesgo pueden realizar la autocertificación CE. Por el contrario, las demás clases de productos (IIa, IIb, III) deben tramitar la certificación del marcado CE a través de un organismo notificado (ON) acreditado. El fabricante debe presentar el expediente técnico CE al ON para su evaluación y la concesión de la marca CE, así como la expedición del certificado CE. El informe de evaluación clínica (CER) de los productos sanitarios debe presentarse junto con el expediente técnico CE para cumplir con los requisitos de marcado CE. El CER debe actualizarse continuamente con nueva información procedente de controles de seguridad, estudios de seguimiento y gestión de riesgos.
El Informe de Evaluación Clínica (CER) para Dispositivos Médicos es uno de los informes que deben presentarse junto con el Expediente Técnico CE para cumplir con los requisitos del CER.
¿Qué es un Informe de Evaluación Clínica (CER)?
La redacción de informes de evaluación clínica incluye la evaluación y el análisis de datos clínicos relacionados con un Dispositivo Médico para verificar su seguridad y rendimiento clínicos. La evaluación clínica de los Dispositivos Médicos se basa en el análisis exhaustivo de los datos clínicos pre y post-comercialización relevantes para el uso previsto. El Informe de Evaluación Clínica incluye datos específicos del dispositivo, así como cualquier dato relacionado con dispositivos declarados como equivalentes por el fabricante.
Un informe de evaluación clínica (CER) se compone de bibliografía científica y datos clínicos analizados, recopilados bien a partir de una investigación clínica de su dispositivo, bien a partir de los resultados de otros estudios sobre dispositivos sustancialmente equivalentes, en los que los fabricantes deben tener pleno acceso a los datos técnicos, biológicos y clínicos del dispositivo equivalente y demostrar claramente cómo su dispositivo se ajusta a este en todos los aspectos críticos. El CER de un Dispositivos Médicos que el dispositivo cumple su finalidad prevista sin exponer a los usuarios y pacientes a riesgos adicionales.
EU MDR debe actualizarse cada año. La frecuencia de las actualizaciones del CER depende del riesgo y varía en función del producto. Si el producto conlleva riesgos significativos, la actualización debe realizarse al menos una vez al año; en caso de que el producto lleve un tiempo considerable en el mercado y esté bien consolidado, el CER puede actualizarse cada 2-5 años. Cualquier modificación introducida en el diseño del producto, así como cualquier información nueva derivada de los datos del sistema de seguimiento poscomercialización, podría dar lugar a una actualización del informe CER.
La evaluación clínica de Dispositivos Médicos, tal como se enmarca en el Informe de Evaluación Clínica (CER), se basa en los factores que se enumeran a continuación.
- Literatura científica disponible actualmente; y/o
- Investigaciones clínicas realizadas; o
- Si la demostración de conformidad con los requisitos esenciales basada en datos clínicos no se considera apropiada.
Etapas de la redacción del Informe de Evaluación Clínica (CER)
En referencia al nuevo Reglamento de Dispositivos Médicos de la UE (EU MDR) – 2017/745, existen cuatro (04) etapas diferentes para realizar una evaluación clínica de Dispositivos Médicos y preparar un Informe de Evaluación Clínica (CER) completo del EU MDR.
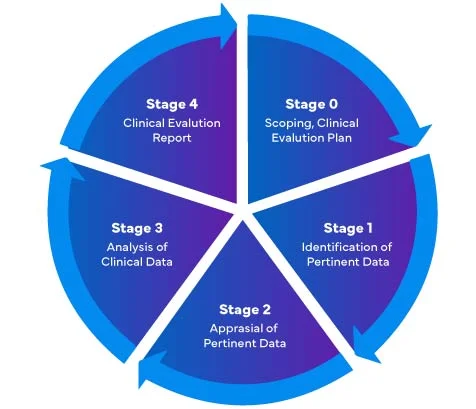
Los fabricantes de Dispositivos Médicos que ingresan al mercado de la UE por primera vez deben asegurarse de que su Informe de Evaluación Clínica cumpla con las normativas del EU MDR.
Freyr ofrece servicios End-to-End de certificación CE a fabricantes de dispositivos, incluyendo la redacción de Informes de Evaluación Clínica en línea con las regulaciones EU MDR 2017/745 recientemente implementadas. Con una sólida experiencia regional en Dispositivos Médicos de la UE, Freyr atiende los requisitos específicos de cada agencia y personaliza el Informe de Evaluación Clínica en consecuencia.
Informe de evaluación clínica (CER)
- Soporte End-to-End para la redacción de Informes de Evaluación Clínica, incluida la búsqueda bibliográfica, según la revisión 4 de MEDDEV 2.7/1 y las directrices del Reglamento de Dispositivos Médicos (MDR) de la UE.
- Elaborar un plan de evaluación clínica para su organización.
- Identificar, buscar, analizar y recopilar la literatura científica aplicable adecuada.
- Desarrollar una plantilla de Informe de Evaluación Clínica para su organización.
- Análisis de deficiencias para informes de evaluación clínica existentes.
- Herramienta DMS para que su equipo contribuya de forma conjunta a la redacción de informes de evaluación clínica.
- Integración de datos de vigilancia post-comercialización.
- Desarrollar un procedimiento operativo estándar para que su equipo compile datos de vigilancia post-comercialización para actualizar los Informes de Evaluación Clínica.
- Gestión de actualizaciones periódicas de informes de evaluación clínica existentes, según las directrices del MDR de la UE.
- Soporte de datos de vigilancia post-comercialización para dispositivos existentes en el mercado.
- Cumplimiento del marcado CE y servicios de marcado CE.

- Cumplimiento garantizado con las normativas reglamentarias aplicables más recientes.
- Equipo de expertos clínicos cualificados.
- Aportaciones interfuncionales de expertos en Dispositivos Médicos para cumplir con los requisitos.
- Servicio integral que abarca el cumplimiento, la revisión y la planificación.

Preguntas Frecuentes (PF)
01. ¿Qué es un informe de evaluación clínica (CER) y por qué es importante?
Un informe de evaluación clínica (CER) es un documento científico reglamentario que evalúa de forma sistemática toda la evidencia clínica disponible para demostrar que un Dispositivos Médicos seguro, funciona según lo previsto y ofrece una relación beneficio-riesgo aceptable para su uso previsto, de conformidad con EU MDR. Desempeña un papel fundamental en la evaluación de la conformidad y el cumplimiento continuo.
02. ¿Cuándo debe elaborarse y actualizarse un CER?
La elaboración del informe de evaluación clínica (CER) comienza en las primeras fases del desarrollo del producto, como parte de un proceso de evaluación clínica planificado, y debe actualizarse periódicamente a lo largo del ciclo de vida del producto cada vez que surjan nuevas pruebas clínicas, datos posteriores a la comercialización o cambios en el perfil de riesgo, con el fin de garantizar que la evaluación de la relación beneficio-riesgo se mantenga actualizada.
03. ¿Qué elementos fundamentales debe incluir un CER válido?
Un CER sólido debe reflejar una evaluación estructurada de los datos clínicos pertinentes, comparaciones con los últimos avances, un análisis de la relación beneficio-riesgo, información procedente de la vigilancia poscomercialización y conclusiones objetivas sobre la conformidad con los requisitos EU MDR y rendimiento EU MDR Reglamento sobre productos EU MDR .
04. ¿Cómo influye el «estado actual de la técnica» en un informe de evaluación clínica?
El «estado actual de la técnica» es el punto de referencia de la práctica clínica y la tecnología aceptadas con respecto al cual se comparan los datos clínicos; garantiza que los beneficios y riesgos del dispositivo se contextualicen en relación con los estándares médicos actuales, lo que permite una interpretación significativa de los datos.
05. ¿Es obligatorio contar con un CER para todos los productos sanitarios con arreglo al Reglamento sobre productos sanitarios ( EU MDR?
Sí, los CER son obligatorios para todos los productos sanitarios comercializados en la UE en virtud del MDR, independientemente de su clase de riesgo, ya que recogen la evidencia clínica indispensable para demostrar la conformidad con los requisitos reglamentarios en materia de seguridad y rendimiento.
06. ¿En qué se diferencia un CER de alta calidad de un informe básico de cumplimiento?
Un CER de alta calidad integra una metodología exhaustiva de búsqueda bibliográfica, afirmaciones clínicas claras y acordes con el uso previsto, una evaluación rigurosa de los datos y reflexiones detalladas sobre el rendimiento clínico y los riesgos, y va más allá del mero cumplimiento de requisitos para reflejar un profundo conocimiento de las expectativas normativas y del contexto clínico.
07. ¿Por qué se considera a Freyr un socio líder en servicios de informes de evaluación clínica (CER)?
Freyr es ampliamente reconocida por su enfoque regulatorio en el desarrollo de evaluaciones comparativas de la evidencia (CER), que combina EU MDR profunda EU MDR , una sólida evaluación de la evidencia clínica y estrategias orientadas al ciclo de vida del producto. Sus equipos multidisciplinares integran los conocimientos clínicos, regulatorios y de la fase posterior a la comercialización para ofrecer CER científicamente rigurosas que superan el escrutinio de los organismos notificados y garantizan el cumplimiento normativo a largo plazo.








