
Resumen del Registro de Dispositivos Médicos en Taiwán
Taiwán tiene una creciente demanda de Dispositivos Médicos. La Administración de Alimentos y Medicamentos de Taiwán (TFDA), bajo el Ministerio de Salud y Bienestar (MOHW), regula los Dispositivos Médicos a través de la Ley de Asuntos Farmacéuticos (PAA). Los fabricantes extranjeros sin oficina física en Taiwán requieren la representación de un agente en Taiwán como requisito previo para el proceso de registro de Dispositivos Médicos en Taiwán.
Autoridad reglamentaria: Administración de Alimentos y Medicamentos de Taiwán
Reglamentación: Ley de Asuntos Farmacéuticos (PAA) y Reglamento para el registro de Dispositivos Médicos
Representante Autorizado: Se requiere representación de agente en Taiwán
Requisito de QMS: Documentación del Sistema de Calidad (DSC) ISO 13485
Evaluación de Datos Técnicosa: División de Dispositivos Médicos y Cosméticos
Validez de la licencia: QSD - 3 años; Registro de productos - 5 años
Requisitos de Etiquetado: Artículo 75, Ley de Asuntos Farmacéuticos
Formato de Presentación: En papel
Idioma: Inglés y Chino
Clasificación de Dispositivos Médicos en Taiwán
La TFDA clasifica los Dispositivos Médicos en 3 clases según el riesgo: Clase I para bajo riesgo, Clase II para riesgo moderado y Clase III para dispositivos de alto riesgo. La necesidad de un dispositivo de referencia dificulta la entrada al mercado de dispositivos nuevos. Otra complejidad es el mayor tiempo de tramitación para los dispositivos de Clase II y III que necesitan documentación del sistema de calidad. Todos los Dispositivos Médicos importados deben obtener un certificado de registro de la TFDA.
| Clase de Dispositivo | Riesgo |
|---|---|
| Clase I | Riesgo bajo |
| Clase II | Riesgo Moderado |
| Clase III | Riesgo alto |
Representación de agente en Taiwán
Los fabricantes extranjeros sin oficina física en Taiwán deben designar un Agente en Taiwán como requisito previo para comercializar dispositivos en Taiwán. Designar una organización externa como Agente en Taiwán en lugar de un distribuidor ofrece flexibilidad para explorar múltiples distribuidores y lograr una mejor penetración en el mercado. El Agente en Taiwán debe ser una entidad jurídica establecida en Taiwán, certificada con una Licencia de Venta de Productos Farmacéuticos.
Registro de Dispositivos Médicos en Taiwán
Antes de que un Dispositivo Médico pueda venderse en Taiwán, se requiere el registro de la Documentación del Sistema de Calidad (QSD) para la instalación de fabricación, además del registro del Dispositivo Médico. El registro QSD solo se exime para Dispositivos Médicos de Clase I (no estériles). Una licencia QSD (recibida tras la aprobación del registro QSD) en Taiwán es similar a las Buenas Prácticas de Fabricación (GMP) para Dispositivos Médicos.
La TFDA anunció que, a partir del 1 de junio de 2022, los titulares de licencias de Dispositivos Médicos de Clase III deben cargar el UDI y la información de producto correspondiente a la Base de Datos UDI (UDID). Los fabricantes de Dispositivos Médicos también deben colocar el UDI en la etiqueta del producto. Además, a partir del 1 de junio de 2023, los Dispositivos Médicos de Clase II deben cumplir con las regulaciones pertinentes del UDI.
Flujo del proceso
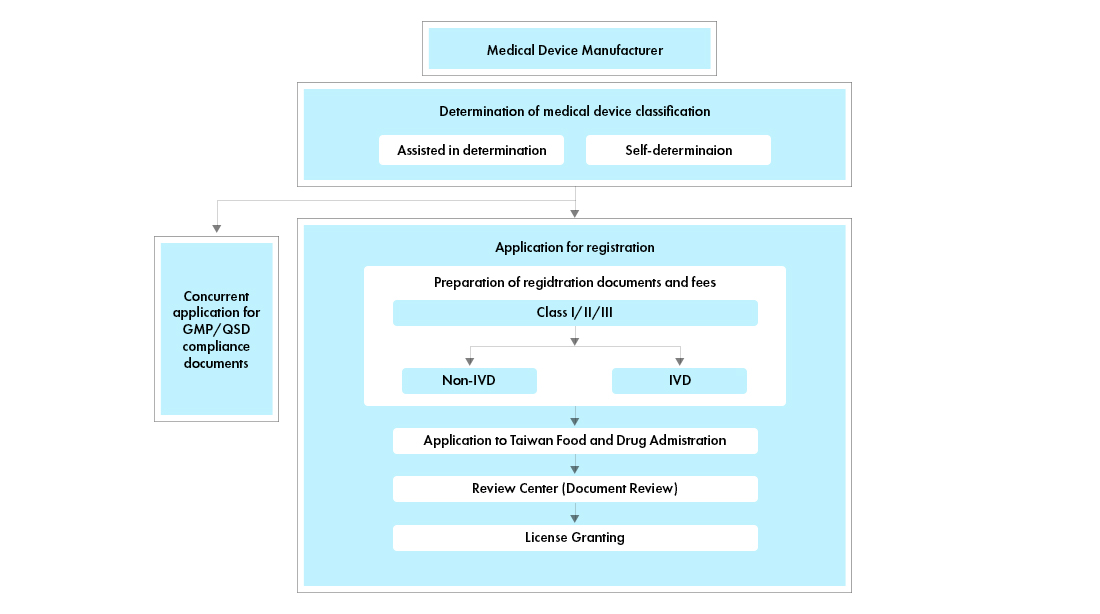
Gestión del ciclo de vida de Dispositivos Médicos post-aprobación
Freyr apoya a los fabricantes extranjeros en la gestión End-to-End del ciclo de vida de Dispositivos Médicos, incluyendo actividades posteriores a la aprobación, tales como:
- Gestión de cambios post-aprobación: modificaciones a las aprobaciones existentes de Dispositivos Médicos, como la adición de nuevas variantes, accesorios; adición de nuevas indicaciones de uso, entre otros.
- Mantenimiento de aprobaciones y registros mediante el pago puntual de tasas administrativas y de registro
- Renovación de licencias
- Coordinación entre la TFDA y el fabricante
- Gestión de importaciones
Freyr se especializa en atender las necesidades reglamentarias de Dispositivos Médicos en Taiwán. Con una extensa red, Freyr ayuda a designar un agente local fiable cuya presencia es de suma importancia durante toda la vigilancia post-comercialización. Nuestros expertos también asisten en la selección de un dispositivo de referencia adecuado y aprobaciones existentes de otros mercados para apoyar la entrada de nuevos dispositivos en el mercado.
Resumen
| Clase de Dispositivo | Criterios de riesgo / clasificación | QMS | Registro de productos |
|---|---|---|---|
| Clase I | Riesgo bajo | Exento (dispositivos no estériles de Clase I) | Sí |
| Clase II | Riesgo Moderado | QSD | Sí |
| Clase III | Riesgo alto | QSD | Sí |
Experiencia de Freyr
- Debida diligencia reglamentaria
- Clasificación Oficial
- Aprobaciones de QSD
- Registro de Dispositivos
- Representante legal
- Apoyo en etiquetado
- Soporte de traducción
- Identificación y cualificación del distribuidor
- Post Marketing Surveillance
- Gestión de Cambios Post-aprobación
- Renovación y transferencia de licencia.
- Presentación y coordinación


