
Descripción general del Registro de Dispositivos Médicos en Vietnam
El mercado de Dispositivos Médicos de Vietnam está en auge y es actualmente uno de los sectores de mayor crecimiento en el país. Los Dispositivos Médicos en el país están regulados por el Departamento de Equipos Médicos y Obras Sanitarias (DMEHW) dependiente del Ministerio de Salud. Los fabricantes extranjeros deben designar un Representante Autorizado Local en Vietnam para que les asista en el proceso de registro de Dispositivos Médicos en Vietnam.
Autoridad reglamentaria: Departamento de Equipos Médicos y Obras Sanitarias (DMEHW)
Reglamentación: Decreto n.º 98/2021/ ND-CP
Representante Autorizado: Representante Autorizado Local en Vietnam
Requisito de QMS: ISO 13485:2016
Evaluación de Datos Técnicos: Departamento de Equipos Médicos y Construcción (DMEC) del MoH
Requisitos de etiquetado: Decreto n.º 111/2021
Formato de Presentación: En línea- Plazos: 15 - 60 días
Idioma: Inglés y Vietnamita
Clasificación de Dispositivos Médicos de Vietnam
Los dispositivos se clasifican en 4 clases (A, B, C y D), que también se dividen en dos grupos: el grupo 1 (Clase A) y el grupo 2 (Clase B, C y D). La clasificación oficial está disponible en el Departamento de Equipos Médicos y Obras de Salud de Vietnam (DMEHW).
| Grupo | Clase | Riesgo |
|---|---|---|
Grupo 1 | Clase A | Nivel Bajo |
Grupo 2 | Clase B | Nivel promedio inferior de riesgo |
Clase C | Nivel promedio superior de riesgos | |
Clase D | Nivel elevado de riesgos |
Representante Autorizado Local en Vietnam
El nombramiento de un agente vietnamita fiable y capaz para los fabricantes extranjeros es crucial, ya que deben asumir los servicios de garantía ofrecidos por el fabricante como parte de la venta del dispositivo. La traducción al vietnamita es imprescindible para entrar en la región, lo que, de hecho, puede ser un desafío en la práctica real.
Freyr ofrece apoyo reglamentario que abarca toda la gama de actividades, como la obtención del Número de Reconocimiento de Libre Venta, involucradas en la aprobación de Dispositivos Médicos por parte de las autoridades. También proporcionamos apoyo de expertos lingüísticos para mantener intacta la perspectiva reglamentaria de la traducción. Atendemos las necesidades de los clientes después de la aprobación para mantener la conformidad durante todo el ciclo de vida del producto en Vietnam.
Registro de Dispositivos Médicos en Vietnam
Todos los productos de Clase A y B requerirán una Licencia de Autorización de Comercialización (MA). Los dispositivos de Clase A y B serán sometidos a una revisión administrativa rápida por parte del Departamento de Salud de la provincia donde se encuentre el Titular del Registro.
Los dispositivos de Clase C y D ahora deberán solicitar una licencia de Autorización de Comercialización (MA). Las licencias de MA seguirán siendo válidas indefinidamente.
Flujo del proceso
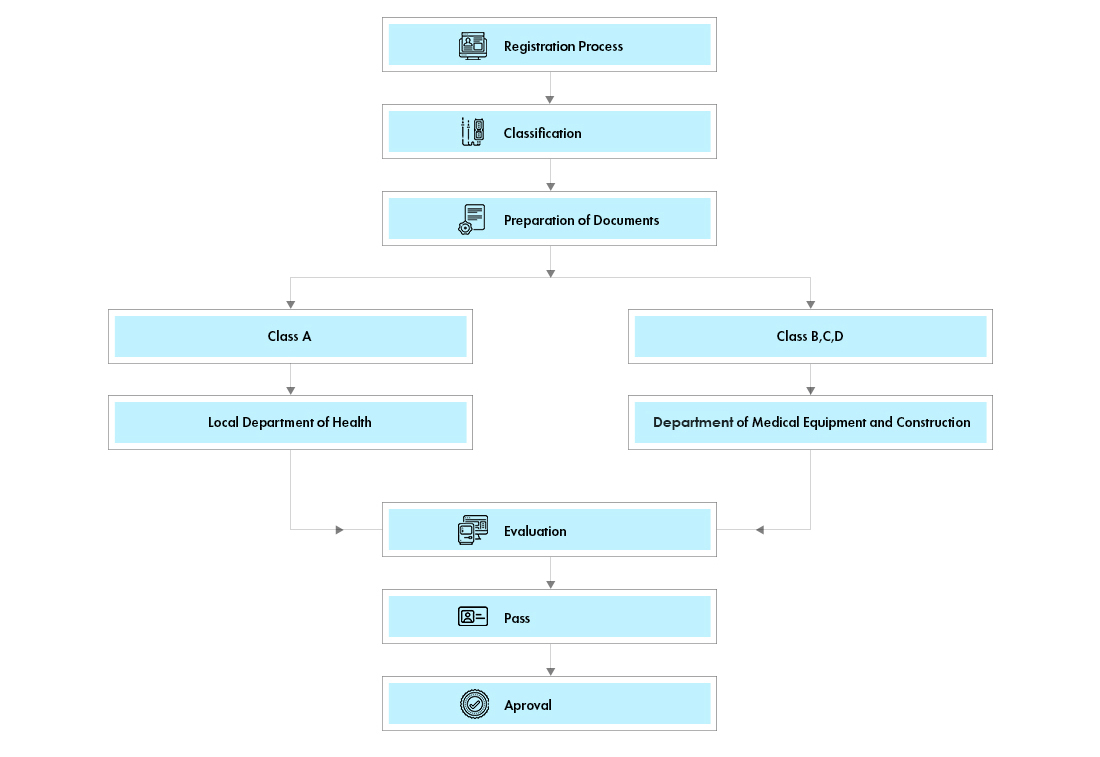
Gestión del ciclo de vida de dispositivos post-aprobación
Freyr apoya a los fabricantes extranjeros en la gestión End-to-End del ciclo de vida de Dispositivos Médicos, incluyendo actividades posteriores a la aprobación, tales como:
- Gestión de cambios post-aprobación: modificaciones a las aprobaciones existentes de Dispositivos Médicos, como la adición de nuevas variantes, accesorios; adición de nuevas indicaciones de uso, entre otros.
- Mantenimiento de aprobaciones y registros mediante el pago puntual de tasas administrativas y de registro
- Renovación de licencias
- Coordinación entre el DMEHW y el fabricante
- Gestión de importaciones
Resumen
Grupo | Clase | Riesgo | Ruta reglamentaria | Plazos | Validez |
|---|---|---|---|---|---|
Grupo 1 | Clase A | Nivel Bajo | Declaración de norma aplicable | 15 - 60 días | Ilimitada |
Grupo 2 | Clase B | Nivel promedio inferior de riesgo | Registro de certificado de libre venta | 15 - 60 días | 5 Años |
Clase C | Nivel promedio superior de riesgos | Registro de certificado de libre venta | 15 - 60 días | 5 Años | |
Clase D | Nivel elevado de riesgos | Registro de certificado de libre venta | 15 - 60 días | 5 Años |
Experiencia de Freyr
- Debida diligencia reglamentaria
- Clasificación Oficial
- Registro de Dispositivos
- Licencia de Importación
- Apoyo en etiquetado
- Soporte de traducción
- Identificación y cualificación del distribuidor
- Post Marketing Surveillance
- Gestión de Cambios Post-aprobación
- Renovación y transferencia de licencia.
- Presentación y coordinación
- Despacho de aduanas


