Panorama general del registro de Dispositivos Médicos en Argentina
Argentina es uno de los países de rápido desarrollo en América Latina que presenta oportunidades para las empresas de Dispositivos Médicos, con un sistema de salud conocido por su dedicación a la seguridad del paciente y servicios médicos de alta calidad. El registro de Dispositivos Médicos en Argentina es supervisado por la autoridad reglamentaria: la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT).

Autoridad Reglamentaria: Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT)
Regulaciones: Disposición 2318/2002, y Disposición 727/2013
Ruta Reglamentaria: Sistema Electrónico de Notificación de Dispositivos Asistido por Web (WAND)
Representante Autorizado: Representante Autorizado en Argentina (AAR)
Requisito del SGC: ISO 13485 (ANMAT MDS), y MDSAP (Miembro Afiliado)
Evaluación de Datos Técnicos: Administración Nacional de Medicamentos, Alimentos y Dispositivos Médicos (ANMAT)
Requisitos de Etiquetado: Anexo III.B de la Disposición 2318/2002 y Anexo V de la Disposición 727/2013.
Formato de Presentación: Electrónico (portal HELENA)
Idioma: Español
Clasificación de Dispositivos Médicos en Argentina
En el proceso reglamentario de la ANMAT, el primer paso para determinar la vía de registro y el cumplimiento de la normativa argentina es determinar la clasificación del Dispositivo Médico. En Argentina, los dispositivos se clasifican en cuatro (04) clases según el riesgo (Clase I-IV).
| Clase de Dispositivos Médicos | Criterios |
|---|---|
| Clase I | Riesgo bajo |
| Clase II | Riesgo bajo - moderado |
| Clase III | Riesgo alto - moderado |
| Clase IV | Riesgo alto |
| Clase de IVD | Criterios |
|---|---|
| Clase A | Diagnóstico de enfermedades no infecciosas o no transmisibles. |
| Clase B | Diagnóstico de enfermedades infecciosas, excepto las que pertenecen a la Clase C. |
| Clase C | Diagnóstico de enfermedades infecciosas de transmisión sexual, o transmitidas por la sangre o sus derivados, así como para la identificación de grupos sanguíneos. |
| Clase D | Para autoevaluación. |
Representante Autorizado en Argentina (AAR)
El titular del registro de cualquier Dispositivo Médico en Argentina es legalmente responsable del registro y la comercialización del dispositivo en el país. Este puede ser el fabricante del dispositivo, o puede ser un representante autorizado local (AAR) en Argentina que actúe en nombre del fabricante.
Todos los Dispositivos Médicos comercializados en Argentina deben registrarse ante la ANMAT. El proceso de registro puede ser complejo y llevar mucho tiempo, por lo que a menudo se recomienda que los fabricantes extranjeros designen un AAR para que les asista.
Registro de Dispositivos Médicos de ANMAT
El proceso de registro de Dispositivos Médicos de ANMAT es similar a los procesos de notificación y registro brasileños, con un grado de escrutinio para la aprobación que aumenta según la clasificación del dispositivo (Clase I, II, III y IV). Todos los fabricantes de Dispositivos Médicos también deben cumplir con el ANMAT-MDS, que es el equivalente argentino de las BGMP y también está en línea con la ISO 13485:2016.
Flujo del proceso
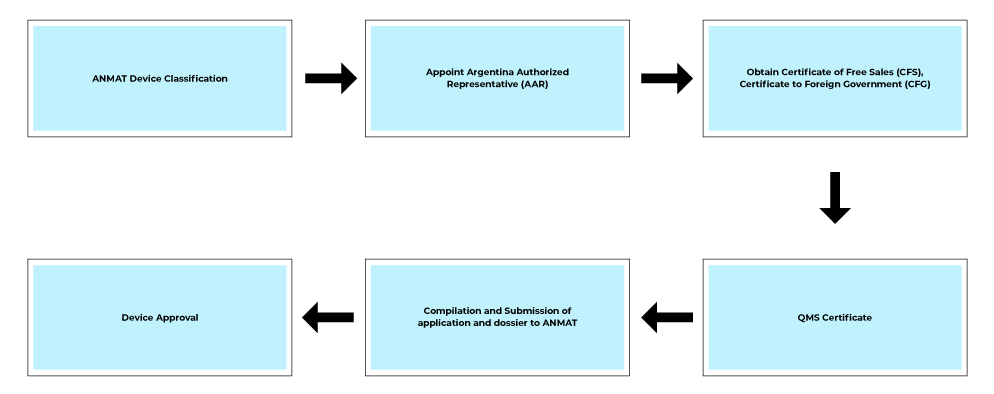
Servicios post-aprobación
Freyr apoya a fabricantes extranjeros con la gestión End-to-End del ciclo de vida de Dispositivos Médicos, incluyendo actividades posteriores a la aprobación, tales como –
- Gestión de cambios post-aprobación: modificaciones a las aprobaciones existentes de Dispositivos Médicos, como la adición de nuevas variantes, accesorios y nuevas indicaciones de uso, entre otros.
- Mantenimiento de las aprobaciones y el registro mediante el pago puntual de las tasas administrativas y de registro.
- Renovación de licencias.
- Servir de enlace entre la ANMAT y el fabricante.
- Notificación de eventos adversos.
- Gestión de importaciones.
Freyr ayuda a los fabricantes a identificar la clasificación de los dispositivos como primer paso. Freyr ayuda a los clientes a navegar por la vía reglamentaria y a obtener certificaciones ayudando a rectificar los problemas reglamentarios implicados. Con experiencia probada en el lanzamiento de numerosos dispositivos en la región, Freyr ofrece servicios reglamentarios End-to-End para Dispositivos Médicos.
Resumen
| Clase de Dispositivos | Vía de Registro (Notificación o Registro Completo) | Plazos de la Autoridad Sanitaria | Validez del Registro (años) |
|---|---|---|---|
| Dispositivos de Clase I | Registro completo | 4-6 meses | 5 años |
| Dispositivos de Clase II | Registro completo | 4-6 meses | 5 años |
| Dispositivos de Clase III | Registro completo | 6-8 meses | 5 años |
| Dispositivos de Clase IV | Registro completo | 6-8 meses | 5 años |
*Tenga en cuenta que factores como las limitaciones de ancho de banda, las actualizaciones reglamentarias y otras variables pueden dar lugar a extensiones en los plazos de las Autoridades Sanitarias.
Experiencia de Freyr
- Servicios de Informes de Inteligencia Reglamentaria.
- Servicios de clasificación oficial.
- Compilación de documentos técnicos.
- Servicios de Registro de Dispositivos.
- Servicios de Representante Autorizado en Argentina (AAR).
- Servicios de Importación.
- Permisos y autorizaciones de operación.
- Servicios de Traducción.
- Servicios de Etiquetado y Artwork.
- Servicios de Identificación y Cualificación de Distribuidores.
- Vigilancia Post-Comercialización.
- Servicios de Renovación y Transferencia de Licencias.
