Descripción General del Registro de Dispositivos Médicos en Colombia.
Colombia presenta grandes oportunidades para las empresas de Dispositivos Médicos y su sistema de salud es reconocido por su compromiso con la seguridad del paciente y la calidad de los servicios médicos. Regula los Dispositivos Médicos a través del INVIMA (Instituto Nacional de Vigilancia de Medicamentos y Alimentos). El INVIMA es la autoridad operativa para el registro de Dispositivos Médicos en Colombia.

Autoridad reglamentaria: INVIMA (el Instituto Nacional de Vigilancia de Medicamentos y Alimentos)
Reglamentación: Decreto 4725/2005
Ruta Reglamentaria: Registro de Dispositivos
Representante Autorizado: Representante Legal en Colombia
Requisito del SGC: ISO 13485:2016 / MDSAP
Evaluación de Datos Técnicos: INVIMA.
Requisitos de Etiquetado: Los documentos de etiquetado deben estar en español.
Validez de la licencia: 10 años
Formato de Presentación: Electrónico
Clasificación de Dispositivos Médicos en Colombia.
| Clasificación de Dispositivos Médicos | |
|---|---|
| Clase I (Riesgo más bajo) | |
| Clase IIa | |
| Clase IIb | |
| Clase III (Riesgo más alto) | |
Representante Legal en Colombia
Para ser Representante Legal en Colombia, se debe tener la ciudadanía colombiana o contar con la autorización legal necesaria para residir y trabajar en el país como extranjero. Un Representante Legal puede asistir y gestionar todos los procedimientos de registro en Colombia, actuando como enlace entre la empresa y el INVIMA, la autoridad reglamentaria local.
Registro de Dispositivos Médicos en Colombia.
Los Dispositivos Médicos e IVD están sujetos a un procedimiento de registro, por lo que los Dispositivos Médicos deben registrarse en el INVIMA para poder comercializarse en Colombia.
Para comercializar un Dispositivo Médico en Colombia, se requiere obtener un Certificado de Libre Venta (CFS) o un Certificado para Gobierno Extranjero (CFG) emitido por la agencia reglamentaria apropiada en el país de origen o un país de referencia reconocido (por ejemplo, Canadá, Japón, Australia, la Unión Europea y los Estados Unidos). El Certificado de Libre Venta o Certificado para Gobierno Extranjero sirve como prueba de que el Dispositivo Médico cumple con los estándares de seguridad y calidad necesarios para su venta en Colombia.
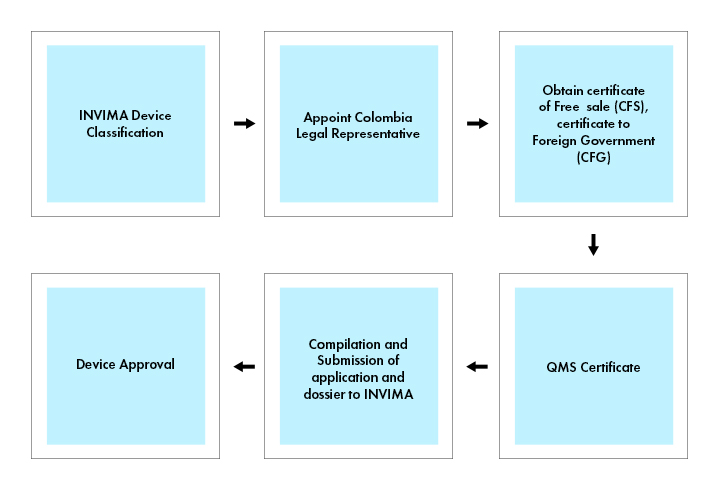
Flujo del proceso
Gestión del ciclo de vida de dispositivos post-aprobación
Freyr apoya a los fabricantes extranjeros en la gestión End-to-End del ciclo de vida de Dispositivos Médicos, incluyendo actividades posteriores a la aprobación, tales como:
- Gestión de cambios post-aprobación: modificaciones a las aprobaciones existentes de Dispositivos Médicos, como la adición de nuevas variantes, accesorios; adición de nuevas indicaciones de uso, entre otros.
- Mantenimiento de aprobaciones y registros mediante el pago puntual de tasas administrativas y de registro
- Renovación de licencias
- Coordinación entre el INVIMA y el fabricante
Resumen
| Clasificación de Dispositivos Médicos | Nuevas licencias y Renovaciones | ||
|---|---|---|---|
| Nuevo registro. | Modificación | Renovación. | |
| Clase I | 4-6 meses | 2-3 Meses | 4-6 meses |
| Clase IIa | 4-6 meses | 2-3 Meses | 4-6 meses |
| Clase IIb | 4-6 meses | 2-3 Meses | 4-6 meses |
| Clase III | 4-6 meses | 2-3 Meses | 4-6 meses |
| Tasas de registro | |||||
|---|---|---|---|---|---|
| Nuevas licencias y Renovaciones | Modificaciones Técnicas | Modificaciones Administrativas | |||
| Clase I y Clase IIa | Clase IIb y Clase III | Clase I y Clase IIa | Clase IIb y Clase III | Clase I y Clase IIa | Clase IIb y Clase III |
| $ 690,00 | $ 776,00 | $ 196,00 | $ 196,00 | $ 153,00 | $ 153,01 |
Experiencia de Freyr
- Debida Diligencia Reglamentaria
- Clasificación Oficial
- Registro de Dispositivos
- Titular del Registro en Colombia
- Apoyo en etiquetado
- Soporte de traducción
- Identificación y cualificación del distribuidor
- Post Marketing Surveillance
- Gestión de Cambios Post-aprobación
- Renovación y transferencia de licencia.
- Presentación y enlace con el INVIMA.