Panorama general del registro de Dispositivos Médicos en Egipto
Desde septiembre de 2018, el registro de Dispositivos Médicos se ha vuelto obligatorio en Egipto. La industria de Dispositivos Médicos en el país ha experimentado un crecimiento constante, lo que la convierte en un mercado atractivo para fabricantes y distribuidores. Con una valoración de 4.000 millones de dólares en 2021, se proyecta que el mercado egipcio de Dispositivos Médicos alcance una Tasa de Crecimiento Anual Compuesta (CAGR) de más del 3% de 2022 a 2027. La importación satisface en gran medida la demanda de Dispositivos Médicos en Egipto, dada la producción local relativamente baja. Cabe destacar que el mercado egipcio de Dispositivos Médicos es el segundo más grande de la región de Oriente Medio y África del Norte (MENA). Esta descripción general explora aspectos clave del proceso de registro egipcio, ofreciendo información sobre el marco reglamentario y los requisitos para llevar Dispositivos Médicos innovadores a la vanguardia del sector sanitario de Egipto.
Autoridad Reglamentaria: Autoridad Egipcia de Medicamentos (EDA)
Reglamento: Ley de Dispositivos Médicos de Egipto, Ley n.º 10 de 2003
Vía Reglamentaria: Registro de Productos (Normal y Vía Rápida) y Clasificación Oficial
Representante Autorizado Local de Egipto: Titular del Registro Egipcio (ERH)
Requisito de QMS: ISO 13485
Evaluación de datos técnicos: El Centro de Política y Planificación de Medicamentos (DPPC) y la Administración Central de Asuntos Farmacéuticos (CAPA).
Validez de la Licencia: Diez (10) años
Formato de Presentación: En papel y electrónico
Traducción: Documentos Traducidos en Árabe e Inglés
Clasificación de Dispositivos
En Egipto, la clasificación de Dispositivos Médicos se alinea con el sistema de clasificación europeo, que categoriza los Dispositivos Médicos según su uso previsto y los riesgos potenciales asociados a su uso. Los fabricantes deben identificar la clasificación correcta de sus dispositivos para garantizar el cumplimiento de los requisitos reglamentarios y obtener las aprobaciones necesarias para la comercialización y distribución en Egipto.
Clases de Dispositivos Médicos
| Clase | Riesgo |
|---|---|
| Clase I | Baja |
| Clase IIa | Bajo-Medio |
| Clase IIb | Medio-Alto |
| Clase III | Alta |
Representante Autorizado Local en Egipto
Las empresas de dispositivos médicos con sede fuera de Egipto deben designar un Agente Local denominado "Titular de Registro Egipcio (ERH)" para gestionar la presentación de solicitudes de registro y expedientes a la EDA en su nombre. El ERH funciona como enlace entre el fabricante y la autoridad reglamentaria, garantizando la preparación y presentación precisas de toda la documentación requerida y verificando que el dispositivo médico cumple con los estándares de seguridad, calidad y eficacia de la EDA. Además, el ERH es responsable de preservar la documentación de registro, informar sobre incidentes o retiradas del mercado, y garantizar la adhesión continua a todos los estándares y reglamentos aplicables durante todo el ciclo de vida del dispositivo. El Titular de Registro Egipcio (ERH) es totalmente responsable de asegurar el registro de un dispositivo médico ante la EDA, particularmente dentro de la Administración Central de Dispositivos Médicos. Este rol implica garantizar el cumplimiento del dispositivo con los requisitos reglamentarios de la EDA para la comercialización y distribución en Egipto.
Registro de Dispositivos Médicos
Obtener la autorización de comercialización para un Dispositivo Médico en Egipto implica varios pasos, incluyendo la preparación de la documentación requerida, la presentación de la solicitud a la EDA, el cumplimiento de los requisitos de clasificación y del sistema de calidad, el nombramiento de un ERH si es necesario, y el cumplimiento de las obligaciones posteriores a la comercialización. El proceso de registro es crucial para garantizar que los Dispositivos Médicos se ajusten a los estándares de seguridad, calidad y eficacia prescritos establecidos por la Autoridad Reglamentaria Egipcia. La documentación requerida puede variar según la vía de registro elegida, pero generalmente abarca lo siguiente:
- Certificado CE (si procede).
- Certificado de Libre Venta (CFS).
- Certificación ISO 13485.
- Declaración de Conformidad (DoC).
Flujo del Proceso
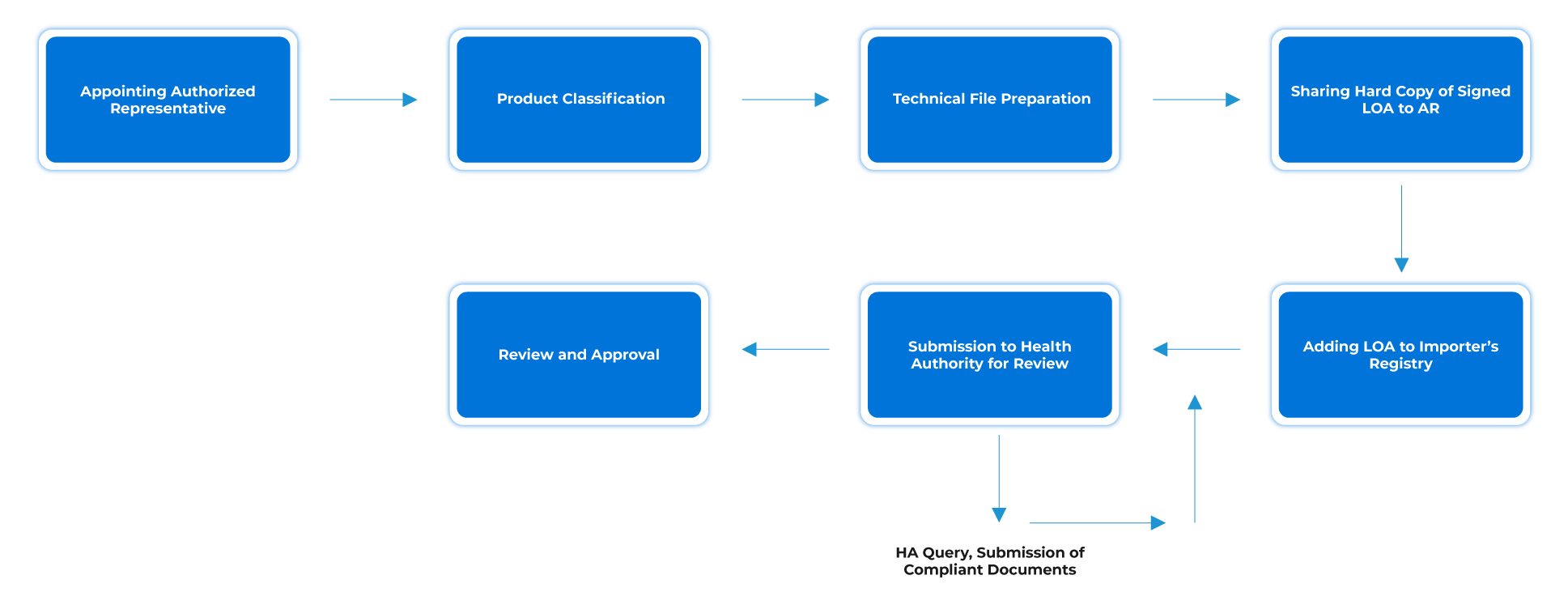
Gestión del Ciclo de Vida del Dispositivo Post-Aprobación
Freyr ofrece un apoyo integral a fabricantes extranjeros en la gestión de todo el ciclo de vida de los Dispositivos Médicos en Egipto, incluidas las actividades posteriores a la aprobación:
- Gestión de cambios post-aprobación, que aborda las modificaciones a las aprobaciones existentes de Dispositivos Médicos, como la adición de nuevas variantes, accesorios e indicaciones de uso.
- Mantenimiento de ISO 13485:2016.
- Certificación CE.
- Actuar como intermediario entre el Organismo Notificado (ON) y el fabricante.
- Un sistema de vigilancia establecido para monitorear la seguridad del Dispositivo Médico después de que se le haya concedido la autorización de comercialización.
- Proporcionar actualizaciones periódicas sobre la seguridad y eficacia del Dispositivo Médico, así como cualquier cambio en el estado reglamentario en otras jurisdicciones.
- Renovación de la autorización de comercialización, dependiendo del tipo de dispositivo y de la reglamentación, después de un cierto período.
La gestión eficaz de la Vigilancia Post-comercialización (PMS) en Egipto implica navegar hábilmente por los marcos reglamentarios establecidos por la EDA. Los nuevos participantes en el mercado que luchan con estas complejidades y carecen de un socio reglamentario establecido pueden aprovechar los amplios servicios reglamentarios ofrecidos por Freyr Solutions. Estos servicios contribuyen a un proceso de aprobación sin problemas para los Dispositivos Médicos en Egipto, garantizando el cumplimiento continuo con el panorama reglamentario en constante evolución y la dinámica del mercado.
Experiencia en el Registro de Dispositivos Médicos en Egipto
- Inteligencia Reglamentaria.
- Debida Diligencia Reglamentaria.
- Clasificación de Dispositivos Médicos.
- Registro de Dispositivos.
- Titular de registro egipcio.
- Soporte de traducción.
- Redacción Médica.
- Soporte de Etiquetado.
- Identificación y Cualificación de Distribuidores.
- Gestión de Cambios Post-Aprobación.
- Renovación y Transferencia de Licencias.
- Despacho de Aduanas.

