
Descripción general del Registro de Dispositivos Médicos en Indonesia
Indonesia ha implementado la atención sanitaria universal para sus ciudadanos en 2014. Esto ha influido enormemente en el crecimiento del mercado de Dispositivos Médicos y ha provocado un aumento en la importación de Dispositivos Médicos. Los dispositivos en Indonesia están regulados por la Agencia Nacional de Control de Medicamentos y Alimentos (NADFC), que funciona bajo el Ministerio de Salud (MoH) de Indonesia. La última reglamentación vigente para la importación de Dispositivos Médicos es el Decreto n.º 62, impuesto en el año 2017. Las empresas extranjeras deben nombrar un representante autorizado local en Indonesia para el proceso de registro de Dispositivos Médicos en Indonesia.
Autoridad reglamentaria: National Agency of Drug and Food Control (NADFC)
Reglamentación: N.º 62 / 2017
Representante Autorizado: Representante autorizado local en Indonesia
Requisito de QMS: ISO 13485:2016
Evaluación de Datos Técnicos: NADFC
Validez de la licencia: 5 Años
Requisitos de Etiquetado: N.º 62 / 2017
Formato de Presentación: En línea/En papel
Idioma: Inglés e Indonesio
Clasificación de Dispositivos Médicos en Indonesia
La normativa actual clasifica los dispositivos como A, B, C y D en función del riesgo.
| Criterios de Riesgo | Clase de Dispositivo |
|---|---|
| Riesgo bajo | A |
| Riesgo Bajo a Moderado | B |
| Riesgo Moderado a Alto | C |
| Riesgo alto | D |
Representante autorizado local en Indonesia
La normativa indonesia exige a los fabricantes que designen un representante local con una licencia de distribuidor. Se puede designar a un distribuidor para representar al fabricante extranjero en Indonesia. Sin embargo, designar a un tercero independiente proporcionaría flexibilidad para cambiar de distribuidor o designar a varios distribuidores para una mejor penetración en el mercado.
Registro de Dispositivos Médicos en Indonesia
El representante local debe crear una cuenta en el portal en línea. El proceso de registro es el mismo para todas las clases de dispositivos. Sin embargo, los requisitos de documentación varían según la clase de dispositivo. El registro es un proceso de dos etapas:
- Proceso de prerreistro
- Proceso de Evaluación
El Ministerio de Salud verifica la clasificación del dispositivo y determina el coste de la evaluación. El resultado del prerregistro, junto con la factura, se envía por correo electrónico al solicitante. El representante local, en nombre del fabricante, realizará el pago y subirá el comprobante de pago. El Ministerio de Salud revisará los documentos y compartirá los resultados por correo electrónico con el solicitante. Algunos dispositivos requieren pruebas en el país en un laboratorio acreditado.
Descripción general del proceso de aprobación reglamentaria
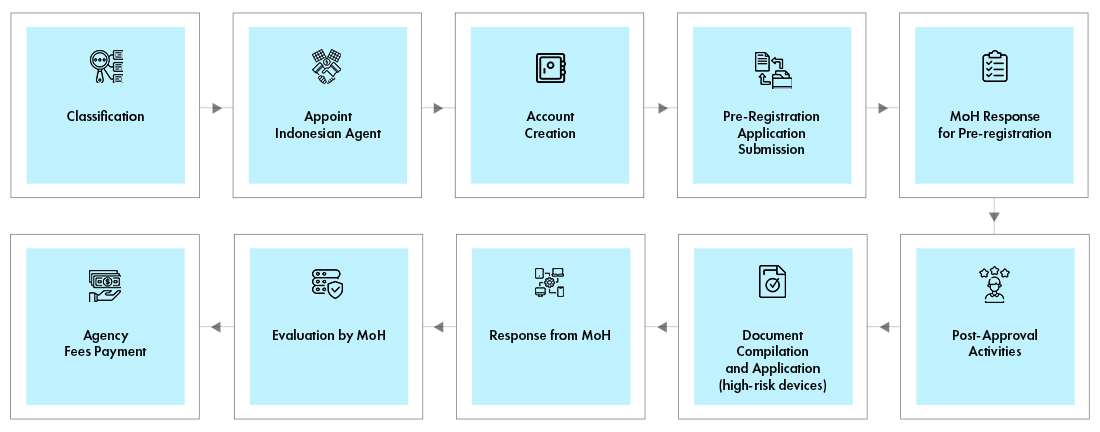
El equipo de expertos de Freyr sigue de cerca las tendencias y regulaciones cambiantes y ayuda a las partes interesadas a mantener el cumplimiento reglamentario durante todo el ciclo de vida del producto. Ofrecemos soluciones reglamentarias para mantener otros aspectos reglamentarios del cumplimiento dentro de presupuestos ajustados.
Clase de Dispositivo | Clase de Riesgo | Plazos del Ministerio de Salud (MoH) para Autorización de Comercialización | Plazos del Ministerio de Salud (MoH) para Renovación / Variación | ||
|---|---|---|---|---|---|
| Proceso de clasificación (Días) | Proceso de Evaluación (Días) | Proceso de clasificación (Días) | Proceso de Evaluación (Días) | ||
| Clase A | Riesgo bajo | 7 | 45 | 7 | 45 |
| Clase B | Riesgo Bajo a Moderado | 7 | 90 | 7 | 45 |
| Clase C | Riesgo Moderado a Alto | 7 | 100 | 7 | 45 |
| Clase D | Riesgo alto | 7 | 120 | 7 | 45 |
Experiencia de Freyr
- Debida diligencia reglamentaria
- Registro de Dispositivos
- Pruebas en el País
- Licencias de Distribuidores
- Legalización y Notarización
- Representante legal
- Soporte de etiquetado
- Soporte de traducción
- Identificación y cualificación del distribuidor
- Servicios de Post Marketing Surveillance
- Gestión de Cambios Post-aprobación
- Servicios de renovación y transferencia de licencias
- Servicios de presentación y enlace


