Descripción general del registro de Dispositivos Médicos en EAU
Los Emiratos Árabes Unidos (EAU), una nación miembro prominente del CCG, tienen un sistema de atención médica avanzado. Su potencial de mercado está probado y en constante aumento, regido por el Departamento de Control de Medicamentos del Ministerio de Salud y Prevención (MOHAP). La gobernanza centralizada y las barreras lingüísticas son obstáculos importantes para el registro de Dispositivos Médicos en EAU, junto con las complejidades lingüísticas y la falta de canales de comunicación eficientes con las Autoridades Sanitarias.
Autoridad reglamentaria: Departamento de Control de Medicamentos del Ministerio de Sanidad y Prevención (MOHAP)
Reglamentación: Directriz de Registro de Dispositivos Médicos de los EAU
Ruta Reglamentaria: Registro de productos
Representante Autorizado: Se requiere un Representante Autorizado Local en los EAU
Requisito de QMS: ISO 13485:2016
Evaluación de Datos Técnicos: Comité de Registro de Dispositivos Médicos
Validez de la licencia: 5 Años
Requisitos de Etiquetado: Anexo 2 (2.5) de la Guía de Registro de Dispositivos Médicos de los EAU
Formato de Presentación: En papel
Idioma: Inglés
Clasificación de Dispositivos Médicos de los EAU
Los EAU tienen Normas de Clasificación separadas para Dispositivos Médicos e IVD. Las normas de clasificación de Dispositivos Médicos de los EAU están en línea con las normas de clasificación de las Directivas de Dispositivos Médicos de la UE. La clasificación de los dispositivos según las normas de clasificación de los EAU es la siguiente
| Criterios de Riesgo | Clase de Dispositivos Médicos |
|---|---|
| Riesgo bajo | Yo |
| Riesgo Bajo a Moderado | IIa |
| Riesgo Moderado a Alto | IIb |
| Riesgo alto | III |
| Criterios de Riesgo | Clase de IVD |
|---|---|
| Riesgo Individual Bajo y Riesgo Bajo para la Salud Pública | A |
Riesgo Individual Moderado y/o Bajo Riesgo para la Salud Pública | B |
Riesgo individual elevado y/o Riesgo Moderado para la Salud Pública | C |
| Riesgo individual elevado y riesgo elevado para la salud pública | D |
Representante Autorizado Local en los EAU
Los fabricantes extranjeros, sin oficina física, deberán designar un Representante Local (LR) para que actúe en su nombre. El representante local debe tener licencia del Ministerio de Salud como tienda médica u oficina científica (en caso de oficina científica, las actividades de importación y distribución deben ser realizadas por una tienda médica con licencia designada). Los solicitantes pueden designar a su distribuidor como su Representante Local. Sin embargo, tener un Representante Local independiente, sin intereses comerciales, proporcionaría la flexibilidad necesaria para designar múltiples distribuidores en los EAU. Los detalles tanto del LR como del distribuidor deben proporcionarse durante el registro del dispositivo.
Proceso oficial de clasificación con el MoHAP de los EAU
El MoHAP de los EAU ha introducido un servicio oficial de clasificación, especialmente útil cuando no está seguro de si su producto requiere registro. Este servicio clasifica productos de todo tipo y forma basándose en su presentación, composición, uso y diseño. Los requisitos pueden variar según la naturaleza del producto, su clase de riesgo y su estado reglamentario.
La carta de clasificación indica si un producto necesita ser registrado ante el MOHAP. Si se requiere el registro, el producto debe registrarse de acuerdo con la clase identificada en la carta de clasificación. Esta carta es válida por tres años a partir de la fecha de emisión.
Los resultados oficiales de clasificación pueden ser:
- No requiere registro en MOHAP
- Aprobado por el MOHAP de EAU como Dispositivo Médico, restringido a uso profesional
- Aprobado por el MOHAP de EAU como Dispositivo Médico de venta libre
Registro de Dispositivos Médicos de los EAU
Ciertos dispositivos que no requieren registro de producto ni listado o aprobación previa para la importación. Dichos productos exentos de registro o listado deberán solicitar y obtener un permiso de importación para ser comercializados en los EAU.
Para otros dispositivos, las importaciones no serán despachadas a menos que el DRCD emita una aprobación previa para la importación del envío. Dichos dispositivos deberán estar listados o registrados para su importación a los EAU.
Registro de Dispositivos: Generalmente, los productos utilizados en hospitales bajo supervisión profesional y los dispositivos de Clase I no se someten a una evaluación detallada y deben ser registrados. La agencia emitirá un Certificado de Registro. Los dispositivos, una vez registrados, deberán obtener un permiso de importación para comercializarlos en los EAU.
Registro de Dispositivos: La actividad de registro incluye el registro del sitio y del producto.
- Registro del Sitio: El sitio de fabricación debe registrarse si el dispositivo fabricado en ese sitio se importa a los EAU por primera vez. Para los dispositivos posteriores fabricados en el mismo sitio, solo bastaría con el registro del dispositivo, y no se requiere el registro del sitio.
- Registro de Dispositivos: Estos dispositivos están sujetos a revisión por parte del comité técnico que, tras su aprobación, recibirá un certificado de licencia.
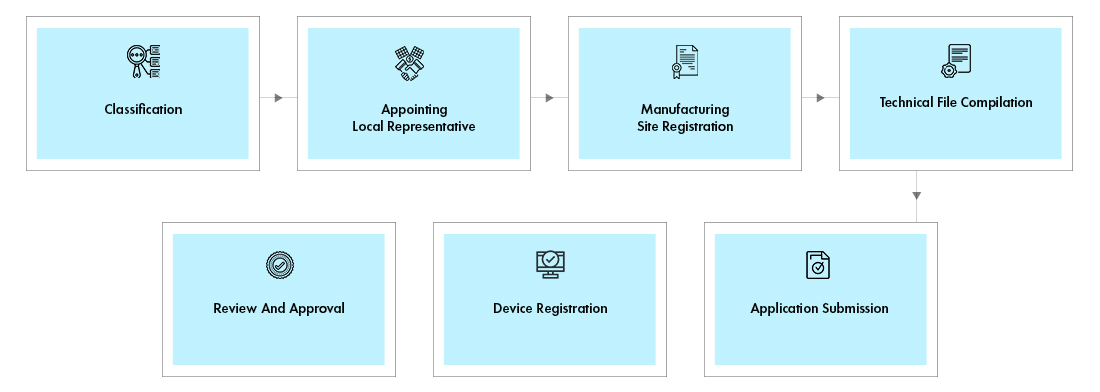
Flujo del proceso
Gestión del ciclo de vida de dispositivos post-aprobación
- Gestión de cambios post-aprobación: modificaciones a las aprobaciones existentes de Dispositivos Médicos, como la adición de nuevas variantes, accesorios; adición de nuevas indicaciones de uso, entre otros.
- Mantenimiento de aprobaciones y registros mediante el pago puntual de tasas administrativas y de registro
- Renovación de licencias
- Servir de enlace entre el Ministerio de Salud y el fabricante
- Gestión de importaciones
Con un centro de entrega exclusivo en Dubái, Freyr tiene un control autorizado sobre el mercado de Dispositivos Médicos de los EAU y describe la clasificación de los dispositivos, además de descifrar las regulaciones de orientación para un mejor cumplimiento. Apoyamos a los clientes en la recopilación de documentos según los estándares y, por lo tanto, garantizamos aprobaciones rápidas. Freyr ofrece una gama completa de servicios normativos relacionados con la comercialización exitosa de dispositivos.
Resumen
| Tipo de Dispositivo | Registro de Dispositivos | Registro de Dispositivos | Licencia de Importación |
|---|---|---|---|
Dispositivo exento de aprobación previa a la importación (Según se indica en el Anexo 3) | NA | NA | SÍ |
| SÍ | NA | SÍ |
| Todos los Otros Dispositivos | NA | SÍ | SÍ |
Experiencia de Freyr
- Inteligencia Reglamentaria
- Debida Diligencia Reglamentaria
- Clasificación Formal de Dispositivos Médicos
- Registro de Dispositivos
- Representación Autorizada en los EAU
- Soporte de traducción
- Apoyo en etiquetado
- Identificación y cualificación del distribuidor
- Gestión de Cambios Post-aprobación
- Renovación y transferencia de licencia.
- Despacho de aduanas