
Servicios Reglamentarios para Dispositivos Médicos
Descripción general en Singapur
Los Dispositivos Médicos en Singapur están regulados por la Ley de Productos Sanitarios (HPA) y su Reglamento de Productos Sanitarios (Dispositivos Médicos) de 2010.
Autoridad reglamentaria: Autoridad de Ciencias de la Salud (HSA)
Reglamentación: Reglamento de Productos Sanitarios (Dispositivos Médicos) de 2010
Ruta Reglamentaria: Subdivisión de Dispositivos Médicos de la Autoridad de Ciencias de la Salud (HSA)
Representante Autorizado: Solicitante de registro en Singapur
Requisito de QMS: SS 620:2016, Norma de Singapur para las Buenas Prácticas de Distribución de Dispositivos Médicos, e ISO 13485:2016
Evaluación de Datos Técnicos: Autoridad de Ciencias de la Salud (HSA)
Validez de la licencia: Todas las licencias de distribuidor son válidas durante 12 meses a partir de la fecha de aprobación.
Requisitos de etiquetado: Guía reglamentaria, GN- 23 Revisada (1 de marzo de 2020)
Formato de Presentación: En línea
Idioma: Inglés
Clasificación de Dispositivos Médicos de la HSA
HSA aplica 16 conjuntos de reglas para clasificar los Dispositivos Médicos de menor a mayor riesgo en Clase A, B, C y D.
La clasificación de riesgo depende de factores como la duración del contacto, el grado de invasividad, el uso previsto y el método de administración.
Clasificación de Dispositivos Médicos, HSA
| Clase de Riesgo | Nivel de Riesgo | Ejemplos de Dispositivos Médicos |
|---|---|---|
| Clase A | Riesgo bajo | Negatoscopio, mano quirúrgica, vaina, mascarilla de oxígeno. |
| Clase B | Riesgo bajo a moderado | Manguito de presión arterial, esterilizador de vástago |
| Clase C | Riesgo moderado a alto | Monitor de paciente, máquina de rayos X |
| Clase D | Riesgo elevado | Stents cardíacos, marcapasos |
Clasificación de IVD
Los Dispositivos Médicos para Diagnóstico In Vitro se clasifican a continuación de menor a mayor riesgo.
Clase de riesgo | Nivel de Riesgo | Ejemplos de Dispositivos Médicos In Vitro |
|---|---|---|
| Clase A | Riesgo individual bajo y riesgo bajo para la salud pública | Recipiente para muestras |
| Clase B | Riesgo individual moderado o riesgo bajo para la salud pública, o ambos | Vitamina B12, autopruebas de embarazo, anticuerpo antinuclear, tiras reactivas de orina |
| Clase C | Alto riesgo individual o riesgo moderado para la salud pública o ambos | Autocontrol de glucosa en sangre, tipificación HLA, cribado de PSA, IgM de rubeola |
| Clase D | Riesgo individual elevado y riesgo elevado para la salud pública | Cribado de donantes de sangre para el VIH, kit de diagnóstico del VIH. |
Representante Autorizado / Registrante de Dispositivos Médicos de Singapur
Un Registrante es el enlace entre su empresa y la HSA, y se encarga del registro de dispositivos en Singapur. El representante autorizado de dispositivos médicos en Singapur tramita la solicitud de registro ante la HSA y es titular de su registro de dispositivo ante la HSA. Solo las empresas o entidades con sede en Singapur pueden actuar como Registrante; también deben estar registradas ante la HSA.
Registro de Dispositivos Médicos de la HSA
El proceso de registro de Dispositivos Médicos de la HSA se lleva a cabo a través del sistema en línea de Información y Comunicación de Dispositivos Médicos (MEDICS) de la HSA. Cada registro de dispositivo de la HSA se realiza a través de una ruta de evaluación específica, dependiendo de lo siguiente:
- Clasificación de riesgo del dispositivo.
- Número de aprobaciones previas otorgadas por las agencias reglamentarias de referencia en el extranjero.
- Duración del historial de comercialización seguro del dispositivo.
La vía de evaluación del dispositivo determinará el tiempo de respuesta (TAT), las tarifas y los documentos necesarios para el registro.
Registro de Clase A - Los dispositivos médicos de Clase A están exentos de registro de productos. Sin embargo, es necesario completar la lista de exención de Clase A en MEDICS durante la solicitud de licencia del distribuidor.
Flujo del proceso
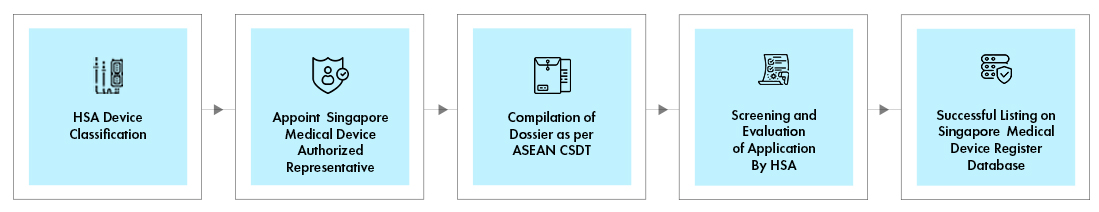
Gestión del ciclo de vida de dispositivos post-aprobación
Freyr presta apoyo a los fabricantes extranjeros en la gestión end-to-end Dispositivos Médicos , incluidas las actividades posteriores a la autorización, tales como:
- Gestión de cambios post-aprobación: modificaciones a las aprobaciones existentes de Dispositivos Médicos, como la adición de nuevas variantes y accesorios; la adición de nuevas indicaciones de uso, entre otros.
- Mantenimiento de las aprobaciones y el registro de dispositivos médicos mediante el pago oportuno de las tasas administrativas y de registro.
- Renovación de licencia.
Con un equipo profesional para proporcionar soporte reglamentario, Freyr apoya a los fabricantes en el mantenimiento de la calidad y seguridad necesarias para la aprobación. Los expertos en inteligencia de Freyr observan atentamente las actualizaciones reglamentarias e informan a los clientes sobre los pasos a seguir para el cumplimiento del producto con los estándares vigentes.
Resumen
El tiempo de procesamiento para el registro de productos se menciona en la siguiente tabla.
| Clase de Riesgo | Inmediato | Acelerado | Abreviado | Evaluación Completa | Completa (Esquema de Revisión Prioritaria) |
|---|---|---|---|---|---|
| Clase B | Registro inmediato tras la presentación | 100 días hábiles | 160 días hábiles | 120 días hábiles | |
| Clase C | Registro inmediato tras la presentación (solo para aplicaciones móviles médicas independientes de Clase C) | 120 días hábiles | 160 días hábiles | 220 días hábiles | 165 días hábiles |
| Clase D | 180 días hábiles | 220 días hábiles | 310 días hábiles | 235 días hábiles | |
| Clase D (Dispositivos que incorporan productos medicinales) | 220 días hábiles | 310 días hábiles |
El tiempo de tramitación para un cambio de titular del registro es de 40 días hábiles.
NOTA-
- Los dispositivos médicos de Clase A están exentos de registro de productos.
- El tiempo de respuesta excluye el tiempo necesario para responder a cualquier solicitud de aclaración o información adicional por parte de la HSA durante la fase de evaluación.
Experiencia de Freyr
- Debida Diligencia Regulatoria para el Registro de Dispositivos ante la HSA, Singapur
- Clasificación y Agrupación de Dispositivos Médicos de la HSA
- Apoyo para la evaluación del Organismo de Evaluación de la Conformidad (OEC)
- Compilación de Expedientes de la Plantilla de Expediente de Presentación Común de la ASEAN (CSDT)
- Registro de Dispositivos de HSA;
- Representación legal
- Soporte de etiquetado
- Identificación y Cualificación de Distribuidores
- Post-marketing Surveillance
- Gestión de Cambios Post-aprobación
- Renovación y Transferencia de Licencias
- Servicios de presentación y enlace con la HSA.



