Servicios de regulación farmacéutica en Chile: visión general
El mercado farmacéutico chileno está regulado por el Instituto de Salud Pública de Chile (ISP), que supervisa la autorización, el registro y la vigilancia de los medicamentos. Todos los productos farmacéuticos deben registrarse antes de su comercialización, lo que garantiza que cumplan las normas de calidad, seguridad y eficacia establecidas por las directrices internacionales.
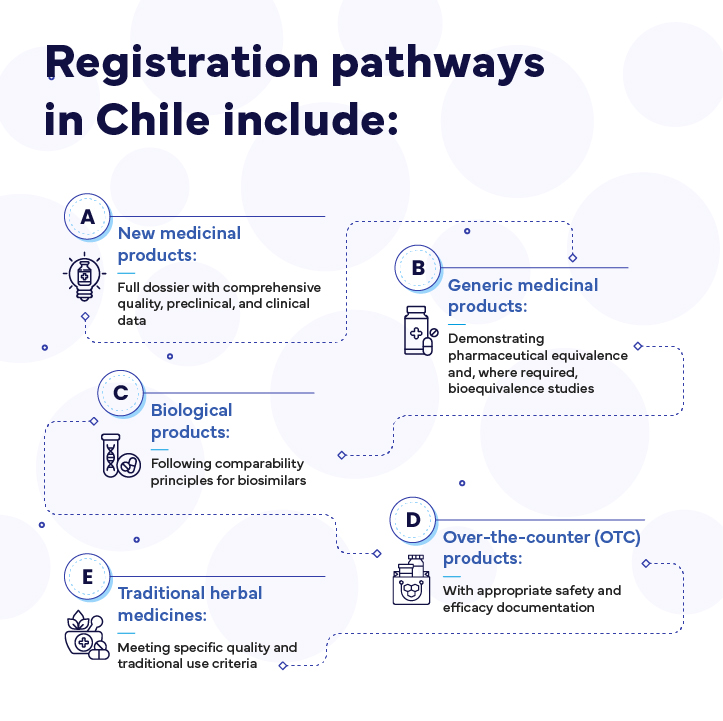
Las vías de registro en Chile incluyen:
Entre los requisitos principales se incluyen la documentación en español, certificados apostillados del país de origen, un titular registrado en Chile y certificados de cumplimiento de las buenas prácticas de fabricación (BPF). Se exigen estudios de bioequivalencia para determinados principios activos, según lo designe el ISP.
El panorama normativo exige conocimientos especializados en los procesos de presentación de solicitudes, la documentación y el cumplimiento de la normativa local. Los fabricantes extranjeros se enfrentan a complejas tareas administrativas, al tiempo que deben garantizar el cumplimiento de las normas chilenas en materia de etiquetado, farmacovigilancia y calidad.
Freyr ofrece un servicio integral de apoyo en materia de regulación a las empresas farmacéuticas que desean obtener la autorización de comercialización en Chile, desde la planificación estratégica hasta la gestión del ciclo de vida tras la autorización.
Servicios de regulación farmacéutica en Chile - Freyr Expertise
Estrategia de registro y preparación del expediente
- Elaboración de expedientes en formato CTD para su presentación a los organismos reguladores de servicios de Internet
- Evaluación de la vía de comercialización (innovadora, genérica, biosimilar)
- Inteligencia normativa (RI) y análisis de deficiencias
- Planificación de la evidencia para los módulos de calidad, preclínicos y clínicos
Servicios de representación local
- Servicios para titulares de registros con domicilio en Chile
- Coordinación con los proveedores de servicios de Internet y gestión de la correspondencia oficial
- Servicios de registro y cumplimiento normativo para centros de fabricación
Documentación y apoyo administrativo
- Gestión del certificado de producto farmacéutico (CPP)
- Elaboración del certificado de buenas prácticas de fabricación (GMP) y tramitación de la apostilla
- Traducción al español y certificación notarial de documentos normativos
- Redacción y legalización de poderes
Servicios de bioequivalencia y calidad
- Planificación y supervisión de estudios de bioequivalencia
- Preparación de la documentación justificativa para la exención biológica
- Asistencia en la validación de métodos analíticos
- Desarrollo de protocolos de estabilidad y evaluación de datos
Gestión de envíos y del ciclo de vida
- Presentación electrónica a través de plataformas de proveedores de servicios de Internet
- Gestión de respuestas a consultas y de incidencias
- Modificaciones posteriores a la autorización (CMC, etiquetado, administrativas, etc.) y enmiendas
- Mantenimiento anual y asistencia para la renovación
Cumplimiento normativo y farmacovigilancia
- Artwork del etiquetado y Artwork chileno
- Implantación del sistema de farmacovigilancia
- Procedimientos de notificación de acontecimientos adversos (AA)
- Elaboración del Plan de Gestión de Riesgos (PGR)
Nuestra sede en Chile
Av. Manquehue n.º 151,
, oficina 1205, Las Condes,
, Chile

