
La idea de las presentaciones reglamentarias electrónicas para productos farmacéuticos es anterior a la propia herramienta eCTD. A finales de la década de 1980, la FDA de US (Administración de Alimentos y Medicamentos) y las agencias europeas exploraron iniciativas como CANDA (Solicitud de Nuevo Medicamento Asistida por Computadora). Estos primeros esfuerzos buscaron mejorar la eficiencia y el acceso a los datos para los revisores.
Introducción al estándar eCTD (2003):
La Conferencia Internacional sobre Armonización (ICH) intervino en 2003 con un cambio radical: el estándar eCTD (Documento Técnico Común electrónico). Este formato estandarizado fue diseñado para establecer un lenguaje universal para las presentaciones electrónicas en todo el mundo.
El surgimiento de las herramientas eCTD:
Con la adopción del estándar eCTD, la demanda de herramientas eCTD especializadas aumentó considerablemente. Estas herramientas aportaron varios beneficios clave:
- Creación de contenido optimizada: Los usuarios podrían crear y organizar documentos sin esfuerzo de acuerdo con la estructura eCTD.
- Validación robusta: Las herramientas eCTD aseguraron que las presentaciones cumplieran con las especificaciones técnicas, evitando retrasos causados por errores de formato.
- Gestión eficiente del ciclo de vida: La gestión de revisiones, el seguimiento de versiones y el mantenimiento del cumplimiento reglamentario se vuelven más sencillos.
Estas innovaciones revolucionaron el proceso de presentación reglamentaria, haciéndolo más eficiente y fiable.
¿Cómo el software de Freyr Digital automatiza la creación de eCTD?
La solución de software avanzada de Freyr Digital, Freyr SUBMIT PRO, aborda estos desafíos al automatizar aspectos clave de la creación de eCTD, mejorando así la eficiencia y reduciendo el error humano.
Optimización de recursos: Al automatizar tareas repetitivas, nuestro software libera recursos humanos valiosos. Los profesionales pueden centrarse en actividades más estratégicas y de alto valor, como el análisis de datos, el desarrollo de estrategias reglamentarias y la interacción con las partes interesadas. Este cambio no solo mejora la productividad, sino que también reduce los costos operativos, lo que proporciona un retorno de la inversión significativo.
Riesgo minimizado de error humano: La automatización minimiza el riesgo de error humano al garantizar que los datos se transfieran con precisión y que los documentos tengan el formato correcto. Las comprobaciones de validación integradas del software y los mecanismos de detección de errores mejoran aún más la calidad y el cumplimiento de las presentaciones reglamentarias. Esto reduce la necesidad de reelaboración y ayuda a garantizar aprobaciones oportunas.
Rastreador de Presentaciones para una Visión General Completa de las Presentaciones eCTD
Un sistema automatizado y fácil de usar para planificar y rastrear actividades complejas de envío global de eCTD, gestionar el flujo de trabajo de actividades, y almacenar y gestionar solicitudes reglamentarias e información de envío es esencial para garantizar que los solicitantes cumplan con los desafíos asociados mucho antes de tiempo. Obtener visibilidad de las operaciones de envío y publicación a un nivel granular hace que todo el proceso de envíos sea más fluido y rápido.
Seguimiento de Presentaciones
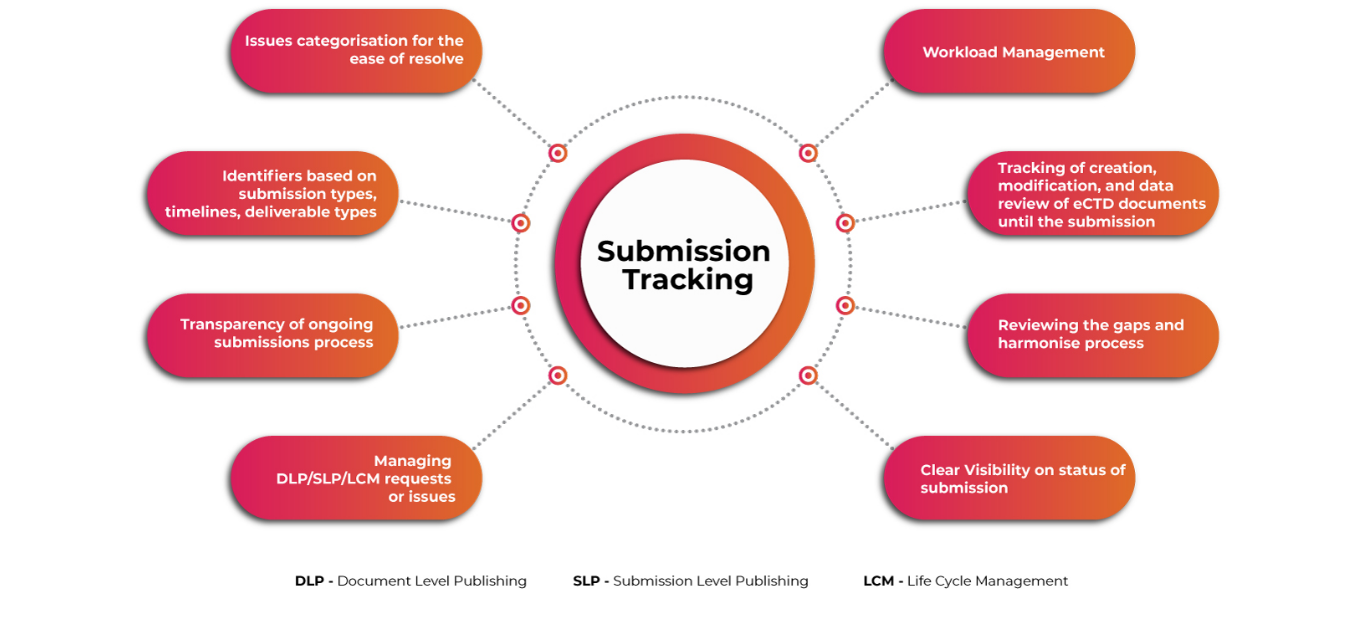
La última actualización en eCTD
El cambio a eCTD 4.0 anuncia una mayor eficiencia y estandarización global en el proceso de aprobación de medicamentos farmacéuticos. Al prepararse para esta transición, su empresa puede gestionar el cambio sin problemas y aprovechar las numerosas oportunidades que ofrece esta nueva era. Si bien la transición a eCTD 4.0 puede plantear desafíos, estos son superables con la dedicación y determinación de todos los países involucrados. Aunque será necesaria una inversión y un esfuerzo significativos, los beneficios sustanciales de eCTD 4.0 hacen que el esfuerzo valga realmente la pena.
Revisión del proceso de presentación: eCTD 4.0 promete revolucionar la forma en que las empresas farmacéuticas presentan los datos de desarrollo de medicamentos a las autoridades sanitarias. Su objetivo es simplificar el proceso de presentación.
Cronograma de implementación: La FDA planea aceptar nuevas solicitudes en formato eCTD 4.0 a partir de 2024. Las fases futuras abordarán las solicitudes existentes de la versión 3.2.2 y la comunicación bidireccional.
Compatibilidad con versiones futuras: eCTD 4.0 incluye compatibilidad con versiones futuras, lo que permite la reutilización del ciclo de vida y de los documentos del contenido de la versión 3.2.2. Esto simplifica la conversión de las aplicaciones de la versión 3.2.2 a eCTD 4.0.
Criterios de validación: Están disponibles las especificaciones para los criterios de validación de eCTD 4.0. Estos criterios garantizan la calidad y precisión de las presentaciones.
Cumplimiento Global: Para 2026, los organismos reguladores de todo el mundo podrían exigir el cumplimiento de los estándares eCTD 4.0. Aunque actualmente es voluntario, la aplicación comenzará entre 2026 y 2029.
El futuro del eCTD:
Debe adoptar la IA y hacer que su función reglamentaria sea dinámica, ya que añade valor a su negocio. Freya Fusion es una plataforma de gestión de información reglamentaria (RIM) de vanguardia, impulsada por IA y nativa de la nube, que ofrece un rendimiento, seguridad y escalabilidad excepcionales, todo ello manteniendo un estricto cumplimiento GxP. Mejorada con funciones avanzadas de IA/ML y automatización, Freya Fusion destaca en el ámbito digital, proporcionando una funcionalidad superior y una experiencia de usuario excepcional. Los avances de IA de Freyr Digital prometen módulos de producción y seguimiento de presentaciones, que incluyen funciones para la compilación, publicación y validación sin problemas de las presentaciones reglamentarias, garantizando un cumplimiento meticuloso de las directrices eCTD. Mantenerse a la vanguardia en el cumplimiento reglamentario con SaaS impulsado por IA sin duda beneficiará a su empresa. Ya sea con un sistema de alerta temprana para cambios reglamentarios, una revisión y análisis optimizados de documentos reglamentarios o análisis predictivos para la gestión de riesgos, Freyr Digital le ofrece todo lo necesario. Póngase en contacto con hello@freyrdigital.com para descubrir nuestras innovaciones impulsadas por IA/ML que optimizan las operaciones reglamentarias en la industria médica.
Manténgase a la vanguardia con actualizaciones periódicas y avances tecnológicos. Asóciese con nosotros para optimizar sus operaciones reglamentarias, aumentar la productividad y mejorar la calidad de las presentaciones. Solicite una demostración hoy mismo y experimente la combinación perfecta de experiencia y herramientas. Impulse su organización de lo bueno a lo excelente. Contáctenos hoy mismo.









