
Para la mayoría Asuntos Regulatorios , la renovación del registro no es solo un trámite administrativo más. Es el momento en el que años de registros de calidad, datos poscomercialización e historiales de cambios se someten al escrutinio de las autoridades reguladoras.
Sin embargo, las renovaciones suelen abordarse de forma reactiva.
Los archivos se recopilan a última hora. Los datos del PMS se guardan en diferentes carpetas. Los certificados se registran en hojas de cálculo. Y, de repente, lo que debería haber sido un proceso estructurado se convierte en una carrera contra el reloj.
Dispositivos Médicos no fracasan porque los equipos no se esfuercen lo suficiente. Fracasan porque la planificación de la renovación se inicia demasiado cerca de la fecha de vencimiento.
Una estrategia de renovación sólida cambia esta situación. Considera la renovación como una actividad continua a lo largo del ciclo de vida, y no como un trámite de última hora.
Analicemos qué significa esto realmente para RA .
Por qué Dispositivos Médicos requieren una estrategia
La mayoría de los registros de dispositivos tienen una validez de entre 3 y 5 años, dependiendo del mercado. Algunas regiones aplican renovaciones anuales, mientras que otras utilizan modelos de mantenimiento con pagos periódicos. Independientemente de la estructura, una vez que caduca la licencia, el dispositivo no puede fabricarse, importarse ni distribuirse legalmente.
Las solicitudes de renovación entrañan un alto riesgo, ya que las autoridades vuelven a evaluar:
- Comportamiento tras la comercialización
- Tendencias en las reclamaciones y eventos adversos
- Cambios en los procesos de fabricación y en el sistema de calidad
- Datos clínicos y de seguridad
- Historial de cumplimiento reglamentario
En muchas regiones, entre ellas la India y la UE, las autoridades reguladoras exigen datos consolidados del sistema de gestión de productos (PMS), pruebas de las medidas correctivas y preventivas (CAPA) y documentación técnica actualizada como parte del proceso de revisión para la renovación.
Por eso, la renovación debe considerarse una disciplina operativa que se aplica a lo largo de todo el ciclo de vida del producto.
No como una tarea sujeta a plazos.
Empieza por un calendario normativo: tu primera línea de defensa
Uno de los motivos más habituales por los que fracasan las renovaciones es el seguimiento fragmentado. Diferentes mercados. Diferentes plazos. Diferentes requisitos.
Un calendario normativo centralizado debería incluir:
- Números de certificado y fechas de caducidad por país
- Plazos para la presentación de renovaciones
- Plazos para el pago de los honorarios de retención
- Validez de la norma ISO 13485 del certificado CE
- Hitos internos (12 meses, 6 meses y 3 meses antes de la renovación)
Desde un RA práctico RA , la planificación debería comenzar al menos 12 meses antes de la fecha de vencimiento.
Hoy en día, muchos equipos utilizan plataformas RIMS unificadas para mantener una visión global del estado de los registros en todos los mercados, lo que les ayuda a evitar la dependencia de las hojas de cálculo y, al mismo tiempo, mantiene los plazos de renovación visibles y gestionables.
freya fusion la primera solución de su clase que permite a las organizaciones disponer de una única fuente de información fiable para todos sus datos relacionados con el cumplimiento normativo.
Documentación básica que siempre necesitarás
La documentación de renovación sigue en gran medida el mismo formato que la de la inscripción inicial, pero hace especial hincapié en la continuidad y el rendimiento.
La mayoría de las autoridades prevén que:
- Carta de presentación en la que se indique claramente la intención de renovar
- Declaración de conformidad continuada (fabricación, diseño, propiedad)
- Archivo maestro de dispositivos y archivo maestro de planta actualizados (si procede)
- ISO 13485 vigente
- Certificados CE o homologaciones de garantía de calidad, cuando sea necesario
- Licencias de fabricación y documentación sobre buenas prácticas de fabricación (BPF)
- Declaración de conformidad
- Historial de correspondencia normativa
Cualquier cambio que se produzca durante el período de validez debe comunicarse a través de los canales adecuados de notificación posterior a la autorización. Los cambios no comunicados son una de las formas más rápidas de suscitar dudas por parte de las autoridades reguladoras.
Aquí es donde cobra importancia la gestión estructurada de documentos. RA se benefician cuando todas las presentaciones, revisiones y aprobaciones se centralizan en un único entorno controlado, en lugar de estar dispersas entre unidades de disco y bandejas de entrada.
La vigilancia poscomercialización es el núcleo del proceso de renovación
Si hay un ámbito que las autoridades reguladoras deben examinar detenidamente durante la renovación, ese es el de la vigilancia posterior a la comercialización.
Las autoridades esperan pruebas de que el dispositivo ha seguido funcionando de forma segura y eficaz en condiciones reales de uso.
Por lo general, esto incluye:
- Datos de ventas por año y modelo de dispositivo
- Registros de reclamaciones e informes de acontecimientos adversos
- Análisis de las causas fundamentales de cada problema
- Registros CAPA con pruebas de cierre
- Historial de retiradas (global y por países)
- Análisis de tendencias a lo largo de todo el período de validez
Los dispositivos de mayor riesgo también pueden requerir:
- Informes del PMS
- Actualizaciones del informe de evaluación clínica
- PMCF
- Informes periódicos de seguridad
La eficacia de las campañas de renovación depende de la regularidad con la que se recopilen estos datos a lo largo del tiempo, y no de lo bien que se compilen al final.
Actualmente, muchos RA integran el seguimiento del PMS directamente en sus flujos de trabajo regulatorios mediante plataformas unificadas como freya fusion, lo que permite que las reclamaciones, las medidas correctivas y preventivas (CAPA) y los registros estén interconectados para facilitar la trazabilidad durante la preparación de las renovaciones.
Adapta tu sistema de calidad para estar preparado para la renovación
Tu sistema de gestión de la calidad no es algo independiente de la renovación. Es la base de la renovación.
Las autoridades reguladoras buscan pruebas en ámbitos clave como:
- Control de documentos e historial de versiones
- Gestión del cambio en los procesos de fabricación, etiquetado y envasado
- Calificación y auditorías de proveedores
- Gestión de reclamaciones y análisis de tendencias
- Eficacia del CAPA
- Auditorías internas
- Registros de formación y competencias
Una forma práctica de proceder es realizar un análisis de las deficiencias antes de la renovación, aproximadamente seis meses antes de presentar la solicitud:
- Comprueba que los certificados sigan siendo válidos tras la revisión
- Verificar que los datos del PMS estén completos
- Consultar los cierres de CAPA
- Consultar los registros de cambios
- Asegúrese de que los registros de formación estén actualizados
Esta auditoría proactiva suele evitar que haya que tomar medidas correctivas de última hora.
Planifica con antelación para hacer frente a la complejidad de los mercados múltiples
Las renovaciones rara vez se producen de forma aislada. Las carteras globales implican a diferentes agentes, distribuidores, organismos notificados y autoridades.
La coordinación suele incluir:
- Fabricante que proporciona fichas técnicas y datos del sistema de gestión de productos
- Agentes locales encargados de gestionar las solicitudes y las licencias
- Distribuidores que comparten datos sobre ventas y reclamaciones
- Organismos notificados que expiden certificados de auditoría
Sin una responsabilidad clara y unos plazos definidos, los retrasos se multiplican.
Un sistema centralizado que permite realizar un seguimiento de los requisitos específicos de cada jurisdicción, el estado de las solicitudes y las comunicaciones normativas puede reducir considerablemente las dificultades. Aquí es donde freya fusion RA , al reunir los registros, los documentos y la colaboración entre las partes interesadas en un único espacio de trabajo regulatorio unificado.
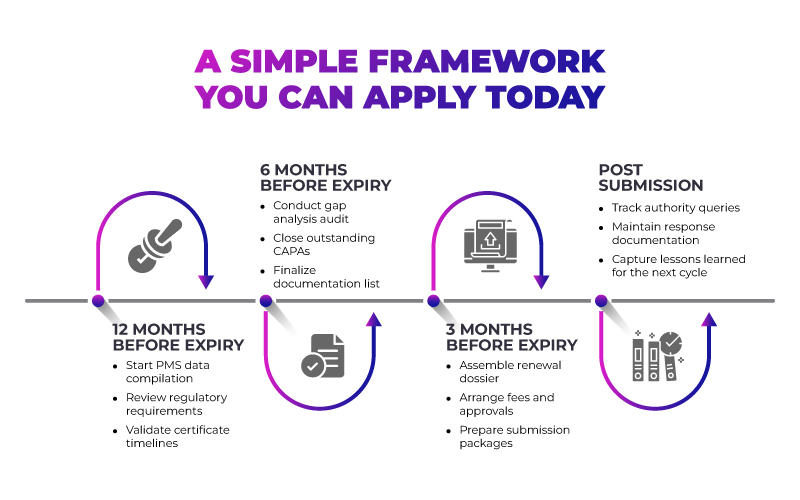
Este enfoque por fases convierte la renovación en un proceso predecible, en lugar de una crisis recurrente.
La renovación tiene que ver con la continuidad, no solo con el cumplimiento
La renovación Dispositivos Médicos tiene como objetivo fundamental garantizar un acceso ininterrumpido al mercado. Cuando se gestiona de forma estratégica, refuerza los sistemas de calidad, mejora el cumplimiento de los sistemas de seguimiento poscomercialización y fomenta la confianza en el marco normativo.
RA ya realizan un arduo trabajo cada día. El reto consiste en dotar a ese trabajo de estructura, visibilidad y continuidad.
En este caso, plataformas como freya fusion . Al unificar los registros, los documentos, los sistemas de gestión de productos (PMS) y la colaboración, ayuda a RA a pasar de las renovaciones reactivas a una gestión proactiva del ciclo de vida normativo.
¿Listo para simplificar Dispositivos Médicos de tus Dispositivos Médicos ?
Si las renovaciones siguen pareciéndote un proceso fragmentado, manual o estresante, tal vez sea el momento de replantearte cómo están estructuradas tus operaciones normativas.
Descubre cómo freya fusion, con sus capacidades basadas en la inteligencia artificial, ayuda aRA Dispositivos Médicos con un seguimiento centralizado de los registros, control de documentos y visibilidad del ciclo de vida, todo ello diseñado para profesionales del ámbito normativo, no para equipos de TI.
Reserva una demostración hoy mismo y da el primer paso hacia la recuperación de la confianza, el cumplimiento normativo continuo y una mayor estabilidad en el mercado.









