MLR de los materiales promocionales de MLR : resumen general
El éxito del lanzamiento de productos y una entrada eficaz en el mercado de los medicamentos o los productos sanitarios dependen de la sinergia entre un equipo Asuntos Regulatorios Promocionales altamente competente Asuntos Regulatorios un sólido proceso de revisión médica, jurídica y regulatoria (MLR). Esta sinergia es fundamental para lograr el pleno cumplimiento de la normativa en materia de publicidad, etiquetado promocional o difusión de información médica no promocional.
Evitar afirmaciones engañosas, no poner en peligro la seguridad de los pacientes y garantizar una difusión ética.
Minimizar los riesgos asociados al incumplimiento normativo, las notificaciones de infracción o las sanciones, así como el daño a la reputación.
Garantiza la veracidad de las afirmaciones relativas a la seguridad, la eficacia o el rendimiento del dispositivo, así como su fundamentación con pruebas científicas.
Coherencia y conformidad con el etiquetado del producto y las instrucciones de uso (IFU) aprobados.
Cumplimiento de las directrices establecidas por los organismos reguladores y los códigos deontológicos del sector en los distintos países y regiones.
En Freyr, nuestros expertos en asuntos médicos y regulatorios, que cuentan con una trayectoria clínica y biomédica sin igual, un gran dominio de MLR y Asuntos Regulatorios promocionales Asuntos Regulatorios en más de 120 países, ofrecen asistencia las 24 horas del día para garantizar el cumplimiento normativo total de sus promociones de marca, anuncios publicitarios, campañas de sensibilización sobre enfermedades o campañas sin referencia a marcas.
Servicios
- Confirmar el cumplimiento de las directrices específicas de cada país establecidas por autoridades reguladoras como la FDA, EMA, el Reglamento sobre productos sanitarios EU MDR), MHRA, la TGA, HSA, PMDA, ANVISA, Health Canada y otras.
- Confirmar el cumplimiento de las directrices específicas de cada país relativas a las leyes contra el soborno y los códigos deontológicos del sector, tales como los de la FTC, PhRMA, EFPIA, ABPI, PAAB, TGA, Medicines New Zealand, ANVISA, ANAMED, IFPMA, AIFA, AEMPS, Mdeon y otros.
- Comprueba que las afirmaciones y las referencias se utilicen correctamente. Las afirmaciones deben estar respaldadas por referencias pertinentes y adecuadas, así como por pruebas científicas, y no se debe exagerar su eficacia o seguridad.
- Asegurar un equilibrio adecuado en la presentación de los riesgos y beneficios del producto, incluidos los posibles efectos secundarios o consecuencias de su uso.
- Evaluar el lenguaje, las imágenes y otros elementos de la presentación de la información para garantizar que sea clara y precisa, y que no contenga información engañosa para el público destinatario.
- Comprobar que los elementos de diseño y de fondo estén en consonancia con el contenido para evitar discrepancias (por ejemplo, asegurándose de que no se utilicen imágenes de pacientes pediátricos en contextos en los que el producto no esté indicado para ese grupo de población).
- Exactitud de las marcas comerciales y de empresa, las marcas de servicio y las certificaciones de conformidad de productos, como el marcado CE, UKCA mark, el CCC y otras.
- Actuar como expertos en la materia (SME) en cuestiones normativas durante las reuniones del PRC.
- Solicitudes de la HA, como el formulario OPDP/APLP 2253 o la revisión por parte de la HA de los materiales promocionales.
- Presentación de documentación sobre etiquetado publicitario y promocional ante las autoridades sanitarias, comoForm 2253 deAPLB Form 2253 laFDA US ,FDA formatos manual y eCTD.
Nuestro equipo es muy innovador y puede desarrollar contenidos para cualquier plataforma o canal; por lo tanto, nuestra oferta y nuestra experiencia no se limitan a lo mencionado anteriormente, ¡podemos hacer mucho más!
- Revisar el contenido relacionado con el medicamento, incluidas las indicaciones, la posología, las instrucciones de uso y el mecanismo de acción, para garantizar su idoneidad y exactitud de acuerdo con el etiquetado aprobado del producto, la información de prescripción (PI), SmPC, los prospectos para el paciente (PIL) y las instrucciones de uso (IFU), y que esté respaldado por la evidencia clínica y científica adecuada.
- Evalúe la alineación del material promocional con las guías de tratamiento actuales y los estándares de atención dentro del área terapéutica específica.
- Personalización de los puntos de control de revisión para adaptarse a las áreas terapéuticas con directrices o normativas para actividades promocionales, como la oncología o las enfermedades raras
- Garantizar un "equilibrio justo" entre la presentación de riesgos y beneficios en el material promocional, reflejando con precisión los posibles inconvenientes junto con las ventajas
- Los ensayos clínicos y otros datos científicos precisos y fiables respaldan adecuadamente las afirmaciones.
- Comprueba que las afirmaciones comparativas con otros productos estén respaldadas por datos válidos y fiables.
- Asegúrate de que la terminología médica y los sinónimos se elijan cuidadosamente para garantizar una comunicación clara.
- Asegúrese de que los materiales sean adecuados para el público destinatario (por ejemplo, profesionales sanitarios, pacientes, cuidadores) y de que se adapten a su nivel de comprensión y a sus necesidades.
- Colaborar con equipos multidisciplinares en el proceso MLR a nivel global y específico de cada país, así como en la evaluación de la situación actual del proceso del Comité de Revisión Promocional (PRC); realizar análisis de deficiencias e identificar áreas susceptibles de optimización y armonización.
- Elaboración de procedimientos operativos estándar (SOP), instrucciones de trabajo para MLR e indicadores clave de rendimiento (KPI) para medir la eficiencia de los procesos.
- Experiencia en la definición de flujos de trabajo de procesos MLR para sistemas de gestión de contenidos de marketing (LCM), como Veeva PromoMats MedComms.
- Facilitar el proceso MLR y PRC para anuncios y materiales promocionales y no promocionales en sistemas de gestión de contenidos de marketing (LCM) como Veeva PromoMats, Veeva MedComms, Pepperflow, etc.
- Elaborar y distribuir los órdenes del día de las reuniones a las partes interesadas, participar en las reuniones del PRC y redactar las actas y las decisiones adoptadas por el PRC.
- Enviar el material promocional y publicitario a los revisores de forma prioritaria y oportuna.
- Programar y dirigir todas las reuniones de revisión de conceptos, previas a la presentación y en directo con las partes interesadas.
- Realizar un seguimiento de las aprobaciones de los materiales y garantizar que las revisiones se incorporen correctamente.
- Garantiza que el material publicitario y promocional cumpla los criterios para su presentación.
Revisión de MLR de materiales promocionales
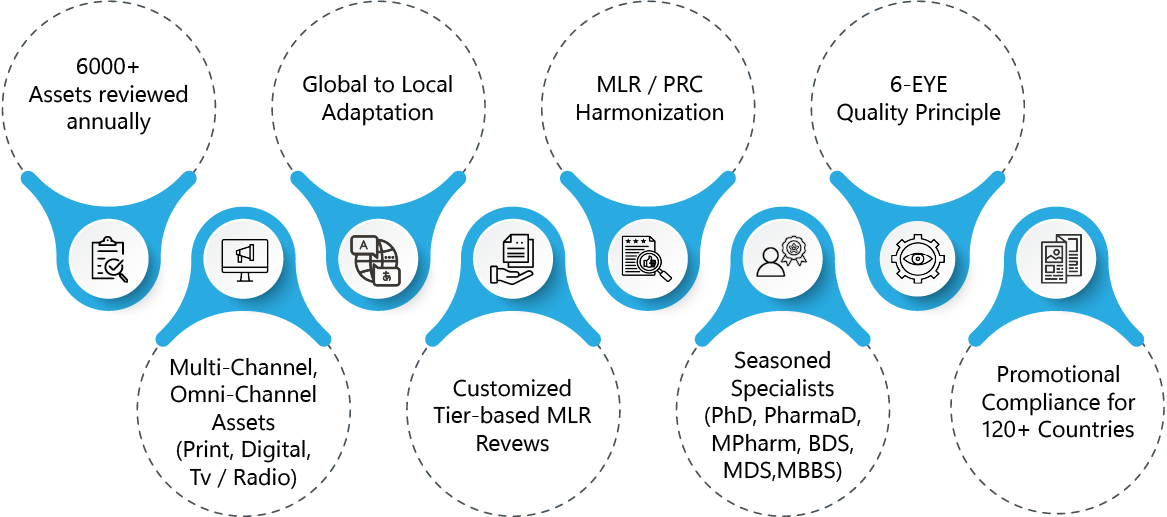
- Más de 6000 activos revisados anualmente para verificar MLR
- Experiencia en la adaptación de materiales promocionales de nivel global a local y en la armonización de los procesos MLR
- El principio de «6 ojos» para mejorar el control del cumplimiento normativo, adaptado a las complejidades de cada área terapéutica
- MLR cuenta con experiencia en una amplia gama de anuncios y materiales promocionales y no promocionales para múltiples canales de comunicación: digital, impreso, televisión y radio.
- MLR por niveles personalizada basada en la complejidad de los activos
- Especialistas en cumplimiento normativo promocional y MLR con experiencia en el sector y formación clínica o biomédica (Doctor en Farmacia, Doctorado, Máster en Farmacia, Licenciado en Odontología, Máster en Cirugía Dental, Licenciado en Medicina y Cirugía)
- Asesoramiento estratégico y específico para cada región sobre el cumplimiento normativo del material promocional en más de 120 países.
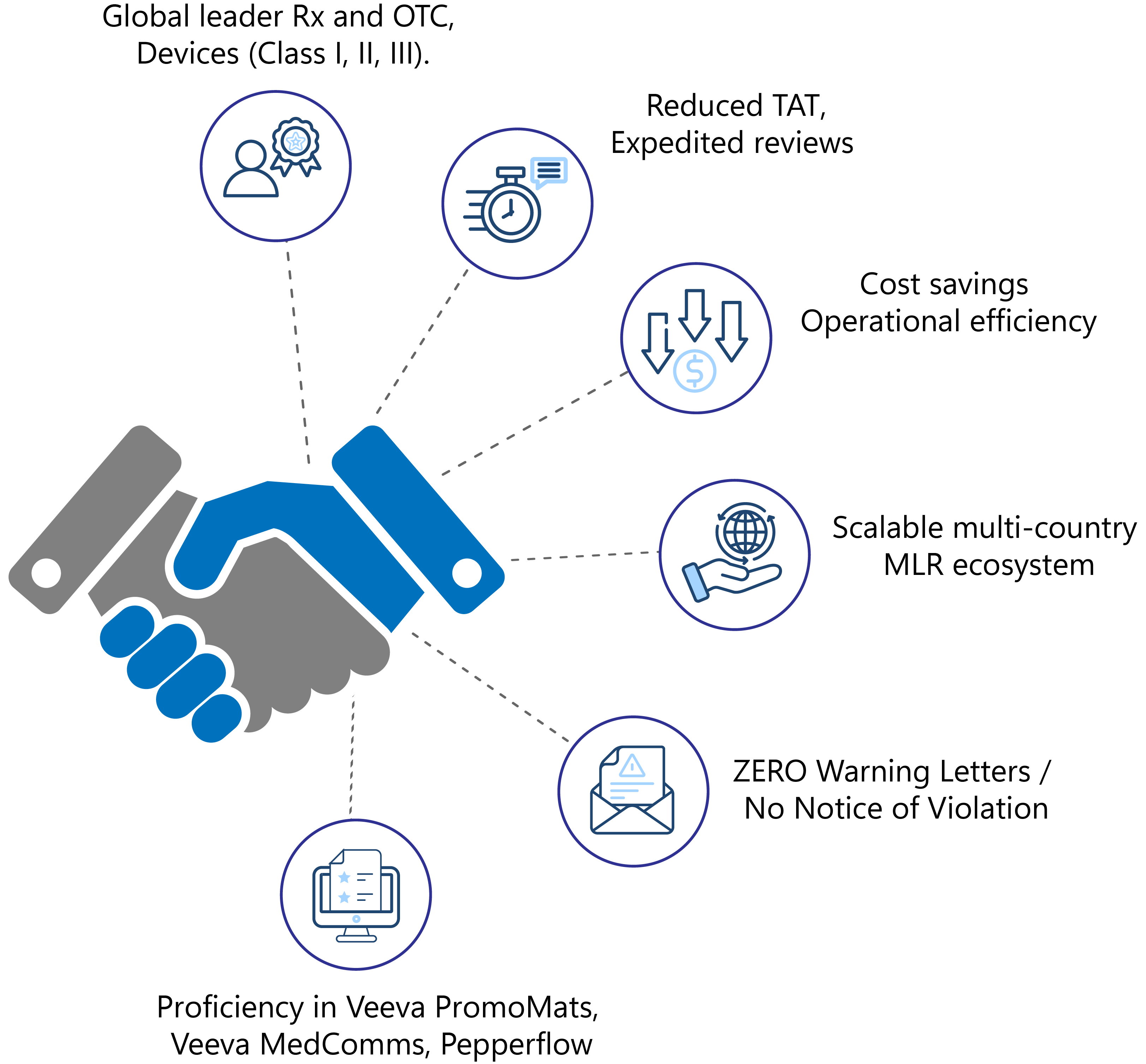
- Líder mundial en el sector farmacéutico, biofarmacéutico (medicamentos con receta y OTC) y de productos sanitarios (clases I, II y III).
- Reducir el tiempo total del ciclo de revisión.
- Reducción del TAT con revisiones aceleradas para cumplir los plazos
- Ahorros significativos de costes y una mejora de la eficiencia operativa
- Ecosistema MLR escalable para múltiples países
- CERO cartas de advertencia/Sin notificación de infracción
- Dominio de los sistemas de gestión de contenidos de marketing ( MLR ) como Veeva PromoMats, Veeva MedComms, Pepperflow, etc.