Auditoría de cumplimiento farmacéutico y servicios de validación
Aproveche una década de experiencia con nuestros servicios a través de evaluaciones de cumplimiento, auditorías meticulosas y procesos de validación sólidos.
Explorar temas
- ¿Qué son el cumplimiento, la auditoría y la validación farmacéutica?
- ¿Cuál es la importancia del cumplimiento, la auditoría y la validación en la industria farmacéutica?
- Principales desafíos en el ámbito del cumplimiento, la auditoría y la validación
- ¿Qué son las auditorías GxP?
- Entendiendo las Auditorías Remotas
- ¿Qué es la Validación de Sistemas Informáticos (CSV) y por qué es crucial en la industria farmacéutica?
- ¿En qué se diferencia la CSV de la Garantía de Sistemas Informáticos (CSA)?
- ¿Cuáles son los componentes de un programa CSA?
- Cómo contribuye la CSA a la integridad de los datos en la industria farmacéutica?
- ¿Qué papel desempeña el cumplimiento reglamentario en CSA?
- ¿Cómo ayuda un socio estratégico de cumplimiento reglamentario?
- ¿Por qué elegir a Freyr?
- Nuestros servicios
¿Qué son el cumplimiento, la auditoría y la validación farmacéutica?
Última actualización: Septiembre de 2024
En el ámbito farmacéutico, los procesos de cumplimiento, auditoría y validación son integrales, garantizando la adhesión a los estándares reglamentarios, la integridad de los datos y la producción de productos seguros y eficaces. El cumplimiento implica alinear las operaciones con las regulaciones de la industria y las políticas internas. Las auditorías, revisiones sistemáticas, verifican el cumplimiento, identifican áreas de mejora y mitigan riesgos. La validación garantiza que los sistemas, procesos y equipos cumplan consistentemente con los requisitos predefinidos.
Las empresas buscan el asesoramiento de expertos para desenvolverse con fluidez. Los líderes del sector gestionan estos procesos con destreza, garantizando el cumplimiento de las normas internacionales sin comprometer la eficacia ni la seguridad de los productos. A medida que evoluciona el sector farmacéutico, los enfoques estratégicos en materia de cumplimiento normativo, auditoría y validación se vuelven fundamentales para lograr un éxito duradero. Al mantener estos procesos, las empresas cumplen con los requisitos normativos y fomentan una cultura de excelencia e innovación en un sector dinámico y exigente.
Colabore con un socio de confianza para obtener orientación estratégica y soluciones personalizadas que permitan a sus operaciones farmacéuticas prosperar en un panorama reglamentario dinámico.

¿Cuál es la importancia del cumplimiento, la auditoría y la validación en la industria farmacéutica?
El cumplimiento, la auditoría y la validación son componentes críticos en la industria farmacéutica, asegurando que los productos sean seguros, efectivos y producidos de acuerdo con los estándares reglamentarios.
- Garantiza la seguridad y eficacia del producto: El cumplimiento de las regulaciones garantiza que los productos farmacéuticos cumplan con estrictos estándares de seguridad y eficacia antes de llegar al mercado. Esto implica rigurosos procesos de prueba y validación para confirmar que los productos funcionan según lo previsto y no representan riesgos para los pacientes.
- Mantiene la adhesión reglamentaria: Las auditorías y validaciones regulares ayudan a las empresas a adherirse a regulaciones complejas y en evolución establecidas por las autoridades sanitarias. Esto incluye el cumplimiento con las Buenas Prácticas de Fabricación (GMP), las Buenas Prácticas Clínicas (GCP) y otros estándares de la industria, reduciendo el riesgo de sanciones reglamentarias y retiradas de productos.
- Mejora la garantía de calidad: Los procesos de validación, incluidas las validaciones de equipos y sistemas, aseguran que los procesos de fabricación y prueba produzcan consistentemente productos de alta calidad. Las auditorías verifican que estos procesos se sigan correctamente, lo que lleva a una mejora en la calidad y confiabilidad del producto.
- Favorece el acceso al mercado y refuerza la reputación: unas prácticas eficaces de cumplimiento normativo y validación facilitan el acceso al mercado al demostrar el cumplimiento de los requisitos reglamentarios. Esto mejora la reputación y la credibilidad de la empresa, generando confianza entre los profesionales sanitarios, los pacientes y los organismos reguladores.
- Facilita la mejora continua: Las auditorías ofrecen información sobre la eficiencia de los procesos y las áreas de mejora, lo que lleva a un mejor control de calidad y a mejores prácticas operativas. Esta evaluación y ajuste continuos ayudan a mantener altos estándares y a adaptarse a los cambios en las normativas y las mejores prácticas de la industria.
Principales desafíos en el ámbito del cumplimiento, la auditoría y la validación
El ámbito de Cumplimiento, Auditoría y Validación se enfrenta a varios desafíos importantes que pueden afectar la capacidad de las empresas farmacéuticas para cumplir con los requisitos reglamentarios y mantener altos estándares de calidad y seguridad:
| Desafío | Descripción |
|---|---|
| Cumplimiento Reglamentario | Las empresas farmacéuticas deben cumplir con regulaciones estrictas de agencias como la FDA y la EMA, que exigen una documentación rigurosa y medidas de control de calidad. El incumplimiento puede dar lugar a sanciones severas, incluidas multas y retiradas de productos. |
| Control de Acceso y Seguridad | Es fundamental asegurar que solo el personal autorizado pueda acceder a áreas e información sensibles. Esto implica implementar sistemas avanzados de control de acceso y mantener la ciberseguridad frente a las amenazas, lo cual puede ser complejo y costoso. |
| Computer System Validation (CSV) | La validación de sistemas informáticos utilizados en entornos GxP es esencial, pero a menudo gravosa y mal definida. El proceso requiere tiempo y recursos significativos, especialmente cuando se aplica un enfoque estándar de forma indiscriminada. |
| Formación y concienciación de los empleados | Los programas de capacitación continua son necesarios para asegurar que los empleados comprendan los protocolos de cumplimiento y su importancia. Una capacitación inadecuada puede llevar al incumplimiento y a errores en los procesos. |
| Documentación y mantenimiento de registros | Mantener una documentación precisa y completa es vital para el cumplimiento. La documentación inadecuada es un problema común que puede dar lugar a observaciones reglamentarias y fallos durante las auditorías. |
| Integridad de los Datos | Garantizar la integridad y exactitud de los datos es crucial, especialmente al gestionar grandes volúmenes de información. Los desafíos incluyen el manejo manual de datos y la necesidad de sistemas robustos de gestión de datos. |
| Gestión de Proveedores | La dependencia de proveedores externos para software y servicios requiere validaciones y verificaciones de cumplimiento exhaustivas. Gestionar estas relaciones y asegurar que cumplan con los estándares reglamentarios puede ser un desafío. |
| Complejidad Tecnológica | La creciente complejidad de las tecnologías, incluidos los sistemas de IA y Cloud-based, presenta nuevos desafíos de validación y requiere una adaptación continua a los entornos reglamentarios en evolución. |
| Control de calidad inadecuado | Muchas empresas farmacéuticas tienen dificultades para mantener altos estándares de calidad en todos los procesos, lo que puede provocar contaminación, contaminación cruzada y otros problemas de calidad. |
| Mejora Continua y Seguimiento | Las auditorías e inspecciones regulares son esenciales para identificar debilidades en los sistemas de cumplimiento. Sin embargo, muchas organizaciones no implementan medidas proactivas para la mejora continua. |
- Regulaciones en evolución: Mantenerse al día con las regulaciones y directrices que cambian rápidamente en las diferentes regiones puede ser un desafío. Las empresas farmacéuticas deben actualizar continuamente sus prácticas de cumplimiento para adherirse a los estándares reglamentarios nuevos o revisados, lo que puede requerir recursos y ajustes significativos.
- Complejidad de los Estándares Globales: Navegar por los diversos y complejos requisitos reglamentarios de diferentes países y regiones aumenta el desafío. Cada jurisdicción puede tener su propio conjunto de reglas y estándares, lo que dificulta lograr un cumplimiento consistente en los mercados globales.
- Integridad y seguridad de los datos: Garantizar la integridad y seguridad de los datos a lo largo de los procesos de cumplimiento, auditoría y validación es fundamental. Las empresas deben implementar sistemas y controles robustos para protegerse contra las filtraciones de datos, la manipulación o las imprecisiones, lo que puede tener graves consecuencias para la aprobación del producto y la seguridad del paciente.
- Restricciones de recursos: Los recursos limitados, incluidos el tiempo, el personal y el presupuesto, pueden obstaculizar la eficacia de las actividades de cumplimiento y auditoría. Las empresas a menudo tienen dificultades para equilibrar las exigencias de mantener el cumplimiento con la necesidad de asignar recursos para otras funciones comerciales críticas.
- Gestión de la documentación y el mantenimiento de registros: Una documentación y un mantenimiento de registros adecuados son esenciales para demostrar el cumplimiento y realizar auditorías eficaces. Sin embargo, gestionar grandes cantidades de documentación, garantizar su precisión y mantener la accesibilidad puede ser un desafío, especialmente en un entorno altamente reglamentado.
- Integración de nuevas tecnologías: Incorporar tecnologías innovadoras en los procesos de cumplimiento y validación existentes puede ser complejo. Si bien tecnologías como la automatización y la IA (Inteligencia Artificial) ofrecen beneficios significativos, su integración debe gestionarse cuidadosamente para garantizar que cumplan con los requisitos reglamentarios y no introduzcan nuevos riesgos.
- Formación y Competencia: Es crucial asegurar que el personal esté adecuadamente formado y sea competente en los procesos de cumplimiento, auditoría y validación. Los programas de formación continua son necesarios para mantener al personal actualizado sobre los cambios reglamentarios y las mejores prácticas, lo que puede requerir muchos recursos.
- Abordar los hallazgos de auditoría: Abordar y corregir eficazmente los problemas identificados durante las auditorías puede ser un desafío. Las empresas deben implementar acciones correctivas y preventivas con prontitud, asegurándose de que estas acciones no interrumpan las operaciones en curso ni afecten la calidad del producto.
- Equilibrar el cumplimiento con la innovación: Lograr un equilibrio entre cumplir con las estrictas normativas y buscar la innovación puede ser difícil. Las empresas deben navegar por el panorama reglamentario mientras continúan desarrollando e introduciendo nuevos productos y tecnologías.
- Garantizar la coherencia en todas las operaciones: Mantener la coherencia en las prácticas de cumplimiento y los procesos de validación en diferentes departamentos, instalaciones y etapas del ciclo de vida del producto es esencial, pero desafiante. La variabilidad en las prácticas puede llevar al incumplimiento y a problemas de calidad.
¿Qué son las auditorías GxP?
¿Qué es una auditoría de cumplimiento independiente GxP y quién la realiza?
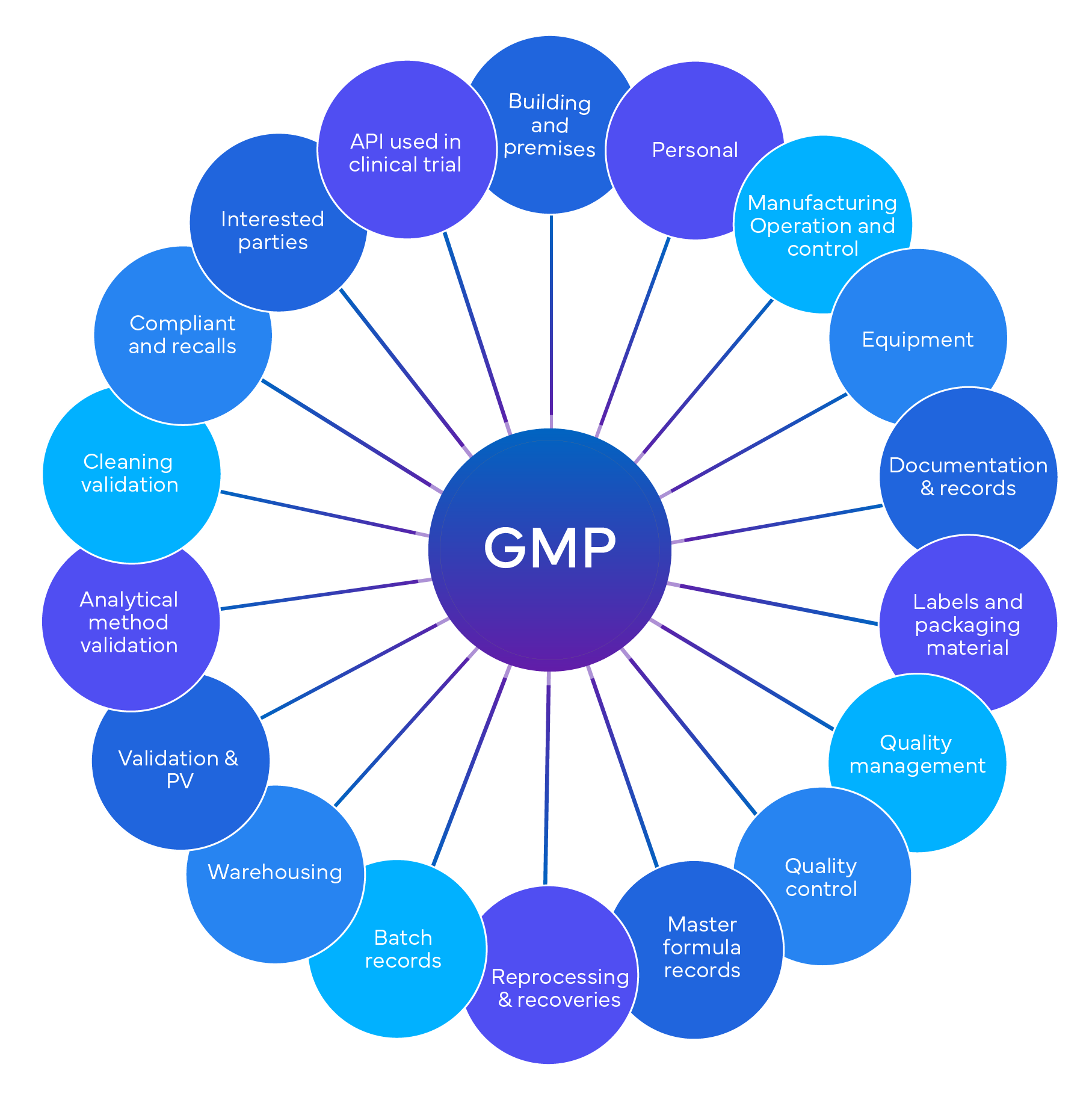
Una auditoría GxP es un proceso diseñado para garantizar que las empresas cumplan con las normas establecidas en materia de calidad, seguridad y cumplimiento normativo. Puede abarcar diversos aspectos de los productos y procesos farmacéuticos, tales como las buenas prácticas de laboratorio (GLP), las buenas prácticas clínicas (GCP), las buenas prácticas de fabricación (GMP) y las buenas prácticas de farmacovigilancia (GVP).
La auditoría evalúa el grado de cumplimiento de las leyes, reglamentos, directrices y procedimientos operativos estándar (SOP) aplicables, e identifica las deficiencias, los riesgos y las oportunidades de mejora. La auditoría también ofrece recomendaciones y medidas correctivas para abordar los resultados observados y mejorar los sistemas de calidad.
Los beneficios de una auditoría GxP incluyen:
- Proporcionar una evaluación imparcial y objetiva de los sistemas de calidad y el nivel de cumplimiento.
- Fomentando la confianza de los organismos reguladores, clientes, proveedores y otras partes interesadas.
- Reducir la probabilidad y la gravedad de las inspecciones, observaciones y sanciones reglamentarias.
- Mejora de la calidad, seguridad y eficacia de los productos y procesos.
- Aumentar la eficiencia y eficacia de las operaciones, y reducir los costos y errores.
- Apoyar la mejora continua y la innovación de los productos y procesos.
Una auditoría GxP es realizada por un auditor cualificado y experimentado o un equipo de auditores con conocimientos, habilidades y credenciales relevantes en la industria farmacéutica y el área GxP específica. El auditor o el equipo de auditoría debe ser independiente de la empresa auditada y seguir los estándares profesionales y principios éticos de la auditoría. También deben utilizar herramientas y métodos apropiados para realizar la auditoría, como listas de verificación, entrevistas, observaciones, revisiones de documentos, muestreo, pruebas, etc. Freyr ofrece soporte End-to-End en auditorías GxP. Como líder de la industria, nuestros expertos harán que su camino hacia el cumplimiento sea fluido.
Marco reglamentario para las auditorías GxP
El cumplimiento GxP es un conjunto de regulaciones que rigen diversas industrias reguladas, incluyendo productos farmacéuticos, Dispositivos Médicos, alimentos, bebidas y biotecnología. El objetivo principal del cumplimiento GxP es mantener la calidad del producto y garantizar la seguridad pública. A continuación, se presentan algunos puntos clave:
- Panorama general del cumplimiento GxP:
- GxP abarca varios estándares, incluyendo las Buenas Prácticas de Laboratorio (GLP), las Buenas Prácticas Clínicas (GCP), las Buenas Prácticas de Fabricación (GMP) y las Buenas Prácticas de Farmacovigilancia (GVP).
- Estas normas aseguran que los productos sean probados exhaustivamente, fabricados y manejados a lo largo de su ciclo de vida.
- Conferencia Internacional sobre Armonización (ICH):
- El ICH proporciona directrices para el cumplimiento GxP.
- La Guía de Buenas Prácticas de Fabricación ICH Q7A aborda específicamente las prácticas de fabricación de ingredientes farmacéuticos activos (APIs).
- Inspecciones de la FDA:
- La Administración de Alimentos y Medicamentos de US (FDA) realiza inspecciones para evaluar el cumplimiento de las regulaciones GxP.
- Estas inspecciones evalúan el cumplimiento de regulaciones y directrices específicas de la FDA.
- Inspecciones de Health Canada:
- Health Canada, la autoridad reglamentaria en Canadá, también realiza inspecciones para asegurar el cumplimiento GxP.
- Estas inspecciones se centran en varios aspectos, incluyendo la fabricación, el control de calidad y la distribución.
- Criterios de evaluación para auditorías GxP:
El cumplimiento en las auditorías independientes GxP se evalúa típicamente según una serie de criterios, que pueden incluir:
- Requisitos reglamentarios: Cumplimiento con regulaciones, directrices y leyes específicas aplicables al área GxP (por ejemplo, regulaciones de la FDA, directrices ICH o estándares ISO).
- Sistemas de calidad: Evaluación de los sistemas de gestión de calidad, las prácticas de documentación y el mantenimiento de registros.
- Validación de procesos: Verificación de que los procesos están validados y cumplen con criterios predefinidos.
- Formación y Competencia: Evaluación de la formación y cualificaciones del personal.
- Gestión de Riesgos: Identificación y mitigación de riesgos relacionados con la calidad y seguridad del producto.
Descubra cómo un experto reglamentario probado puede ayudarle a crear el marco ideal de auditoría GxP adaptado a sus necesidades y a mantenerse en cumplimiento con las regulaciones globales.
Beneficios de realizar auditorías de cumplimiento GxP.
Las auditorías GxP tienen numerosos beneficios para cualquier organización. En primer lugar, proporcionan una evaluación imparcial e independiente del riesgo y el cumplimiento dentro de la organización, permitiendo a las empresas identificar áreas de incumplimiento o riesgo potencial que podrían pasarse por alto en las auditorías internas. Estas auditorías son esenciales para garantizar que las empresas se adhieran a ciertos estándares de calidad, seguridad y cumplimiento reglamentario.
| Aspecto | Descripción |
|---|---|
| Revisión integral | Evaluación exhaustiva por un tercero cualificado para identificar áreas de incumplimiento. |
| Estándares Reglamentarios | Adhesión a los estándares GxP (buenas prácticas) como GMP, GCP y GLP. |
| Alcance Personalizado | Alcance de auditoría personalizado basado en productos y procesos específicos. |
| Auditores Cualificados | Auditores experimentados familiarizados con la normativa. |
| Marco Reglamentario | Sigue las directrices de ICH Q7A, la FDA y Health Canada. |
| Beneficios | Evaluaciones imparciales, prevención de riesgos, mantenimiento de la calidad y escalabilidad. |
Aquí hay algunos puntos clave sobre las auditorías de cumplimiento GxP:
- Revisión exhaustiva: Las auditorías GxP implican un proceso de revisión exhaustivo realizado por una organización o consultor externo cualificado. El objetivo es identificar cualquier área de incumplimiento dentro de la organización y proporcionar recomendaciones para la mejora.
- Estándares reglamentarios: Las regulaciones revisadas durante estas auditorías se definen por los estándares GxP (buenas prácticas), como las Buenas Prácticas de Fabricación (GMP), las Buenas Prácticas Clínicas (GCP) y las Buenas Prácticas de Laboratorio (GLP). Estos estándares garantizan que los productos, servicios y procesos cumplan consistentemente con los requisitos reglamentarios pertinentes.
- Alcance Personalizado: El alcance de una auditoría independiente se adapta a los productos y procesos específicos de la organización. Puede incluir la gestión de personal, la gestión de instalaciones, el mantenimiento de registros, el aseguramiento y control de calidad, el diseño de productos y procesos, y las operaciones técnicas.
- Auditores Cualificados: La auditoría debe ser realizada por un auditor cualificado y experimentado que esté familiarizado con las regulaciones aplicables y tenga la experiencia necesaria para evaluar eficazmente los procedimientos y procesos de la organización.
- Marco reglamentario: Las auditorías GxP siguen marcos como la Guía de Buenas Prácticas de Fabricación Q7A de la Conferencia Internacional sobre Armonización (ICH), las inspecciones de la FDA y las inspecciones de Health Canada. Estos marcos proporcionan orientación sobre los requisitos básicos para la producción, la garantía de calidad, la distribución y otras actividades críticas relacionadas con la fabricación segura de productos.
- Beneficios: Las auditorías GxP ofrecen evaluaciones imparciales, ayudan a prevenir problemas de incumplimiento, mantienen los estándares de calidad y garantizan la rendición de cuentas. La subcontratación de estas auditorías proporciona acceso a experiencia, objetividad, eficiencia de costos y escalabilidad, al tiempo que permite a las empresas centrarse en las competencias principales.
Si busca soluciones de cumplimiento GxP, considere Freyr. Nos especializamos en el cumplimiento reglamentario, la garantía de calidad y la seguridad en toda la industria de las ciencias de la vida. Con nuestra experiencia, puede garantizar la adhesión a los estándares GxP, optimizar los procesos y mantener productos y servicios de alta calidad.
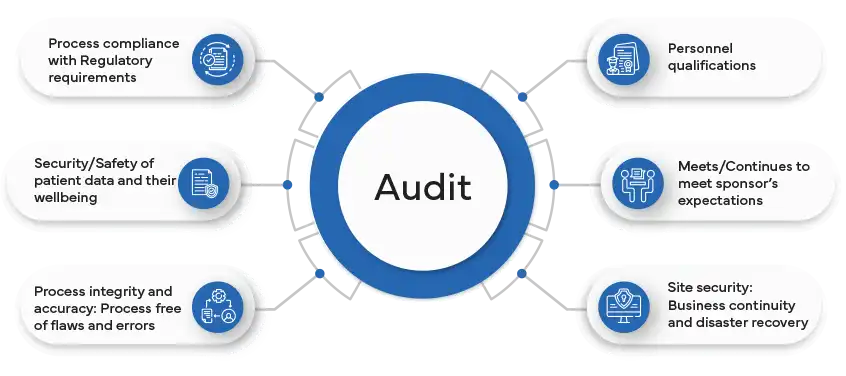
Consejos para Preparar su Organización para una Auditoría
Preparar su organización para una auditoría es un proceso estratégico que implica una planificación meticulosa y un enfoque proactivo. En primer lugar, asegúrese de que todos los registros, la documentación y los archivos relevantes estén organizados y sean fácilmente accesibles. Un sistema de archivo bien organizado facilita un proceso de auditoría más fluido y refleja positivamente el profesionalismo de su organización.
En segundo lugar, realice una preauditoría interna para identificar posibles áreas de preocupación. Esta autoevaluación le permite abordar cualquier problema o discrepancia antes de la auditoría externa. Al resolver los problemas de manera proactiva, demuestra su compromiso con el cumplimiento y la transparencia.
En tercer lugar, comuníquese y colabore eficazmente con el equipo de auditoría. Proporcione la información necesaria, acceso al personal relevante y un entorno de trabajo propicio. Una comunicación clara ayuda a establecer una relación positiva con los auditores, fomentando un ambiente de colaboración durante el proceso de auditoría.
Por último, asegúrese de que su equipo esté bien capacitado y conozca el proceso de auditoría. Eduque a los empleados sobre sus funciones, responsabilidades y la importancia del cumplimiento. Al inculcar una cultura de preparación y cooperación, su organización podrá afrontar las auditorías con confianza y profesionalidad.
Entendiendo las Auditorías Remotas
¿Qué es una auditoría remota en la industria farmacéutica y en qué se diferencia de las auditorías presenciales tradicionales?
Una auditoría a distancia en el sector farmacéutico es una evaluación exhaustiva de los procesos, las instalaciones y los sistemas de una empresa, llevada a cabo por autoridades reguladoras o auditores sin necesidad de estar físicamente presentes en las instalaciones. Esta auditoría se lleva a cabo mediante herramientas de comunicación digital, software colaborativo y acceso remoto a los documentos y sistemas pertinentes. Su objetivo es garantizar el cumplimiento de las normas reguladoras, evaluar los sistemas de gestión de la calidad y verificar el cumplimiento de las Buenas Prácticas de Fabricación (BPF), las Buenas Prácticas Clínicas (GCP) u otras normativas aplicables.
La diferencia entre las auditorías remotas y las tradicionales in situ es la ausencia de presencia física durante una auditoría remota. En lugar de visitar las instalaciones de la empresa, los auditores se basan en interacciones virtuales, documentación electrónica y acceso remoto a los sistemas. Este enfoque ofrece flexibilidad y eficiencia, permitiendo que las auditorías se realicen independientemente de las distancias geográficas y las restricciones de viaje. Sin embargo, es necesario abordar desafíos como la observación directa limitada de las instalaciones y las posibles preocupaciones de ciberseguridad para asegurar la eficacia de las auditorías remotas.
A pesar de las diferencias, los objetivos tanto de las auditorías remotas como de las tradicionales siguen siendo los mismos: verificar el cumplimiento, identificar áreas de mejora y garantizar la calidad y seguridad de los productos farmacéuticos. La elección entre auditorías remotas y presenciales depende de factores como la naturaleza de la auditoría, los requisitos reglamentarios y las capacidades de la empresa para facilitar una evaluación exhaustiva por medios remotos.
Freyr aprovecha una década de experiencia para proporcionar soluciones reglamentarias inigualables, garantizando el cumplimiento y el éxito en el dinámico panorama farmacéutico.
Descubra la excelencia reglamentaria con nosotros, su socio estratégico para el éxito del cumplimiento en la industria farmacéutica en constante evolución. Conéctese con nosotros para navegar las complejidades reglamentarias sin problemas.
¿Qué desafíos pueden surgir durante las auditorías remotas y cómo se abordan para garantizar evaluaciones exhaustivas?
Durante las auditorías remotas, pueden surgir varios desafíos, pero las organizaciones pueden tomar medidas para abordarlos y garantizar evaluaciones exhaustivas. Estos son algunos desafíos clave y sus posibles soluciones:
- Estableciendo relaciones clave con las partes interesadas de la auditoría:
- Desafío: El trabajo remoto puede dificultar el desarrollo de relaciones sólidas con las partes interesadas de la auditoría.
- Solución: Las reuniones virtuales regulares, la comunicación abierta y el compromiso activo pueden ayudar a construir y mantener relaciones. Utilice las videollamadas para establecer una conexión personal.
- Inversión en tecnología para el trabajo virtual.:
- Desafío: Las auditorías remotas dependen en gran medida de la tecnología, y las herramientas inadecuadas pueden dificultar la eficiencia.
- Solución: Invierta en software robusto de gestión de auditorías, plataformas de comunicación seguras y herramientas de colaboración. Asegúrese de que los auditores tengan el hardware y software necesarios.
- Desarrollo de empleados y promoción de una cultura positiva a distancia.:
- Desafío: El trabajo remoto puede llevar al aislamiento y dificultar el crecimiento profesional.
- Solución: Proporcione capacitación virtual, mentoría y oportunidades para el desarrollo de habilidades. Fomente una cultura positiva a través de actividades de creación de equipos, reconocimiento y controles regulares.
- Cultivar una mentalidad intencional y adaptable.:
- Desafío: Los auditores remotos deben adaptarse a las circunstancias cambiantes y mantenerse concentrados.
- Solución: Fomente la flexibilidad, la adaptabilidad y una mentalidad de crecimiento. Capacite a los auditores para manejar situaciones inesperadas y ajustar su enfoque según sea necesario.
Freyr es un socio de confianza en soluciones de cumplimiento normativo y seguridad para la industria de las ciencias de la vida. Con una profunda experiencia en el sector, tecnología innovadora y una presencia global, Freyr capacita a las organizaciones para navegar sin problemas por complejos panoramas normativos. Explore nuestros servicios y contáctenos hoy mismo para mejorar su camino hacia el cumplimiento.
¿Cómo está Freyr en mejor posición para ayudarle con sus auditorías remotas?
Freyr, con su experiencia de una década, destaca en la facilitación de auditorías remotas sin interrupciones para la industria farmacéutica. Aprovechando tecnologías avanzadas y un profundo conocimiento de los requisitos reglamentarios, Freyr garantiza un proceso de auditoría exhaustivo y eficiente, abordando desafíos como la presencia física limitada y las preocupaciones de ciberseguridad.
Nuestro equipo dedicado de expertos reglamentarios es experto en la utilización de soluciones digitales innovadoras, lo que garantiza una evaluación virtual integral de sus procesos, instalaciones y documentación. Nuestro historial probado en auditorías remotas refleja nuestro compromiso de ofrecer soluciones reglamentarias fiables y eficaces adaptadas a las necesidades cambiantes del panorama farmacéutico. Con Freyr, usted obtiene un socio de confianza que comprende las complejidades de las auditorías remotas y aporta un enfoque proactivo y colaborativo para mejorar su trayectoria de cumplimiento.
¿Qué es la Validación de Sistemas Informáticos (CSV) y por qué es crucial en la industria farmacéutica?
Validación de Sistemas Informáticos (CSV) es un proceso crítico en la industria farmacéutica que garantiza la integridad, fiabilidad y cumplimiento de los sistemas informatizados utilizados para diversos fines. Profundicemos en los detalles:
- Definición y propósito:
- CSV es el proceso documentado que asegura que un sistema informático producirá información o datos que cumplen con requisitos predefinidos.
- Su propósito principal es validar y verificar que los sistemas informáticos funcionan de forma consistente según lo previsto, manteniendo la exactitud, fiabilidad y seguridad de los datos.
- Importancia en la industria farmacéutica.:
- Cumplimiento reglamentario: La industria farmacéutica opera bajo regulaciones estrictas (como las Buenas Prácticas de Fabricación o GMP) para garantizar la calidad, seguridad y eficacia del producto.
- Integridad de los Datos: Los datos precisos y fiables son fundamentales para el desarrollo de fármacos, los ensayos clínicos, la fabricación y la distribución.
- Mitigación de Riesgos: La CSV ayuda a identificar y mitigar los riesgos asociados con los sistemas informáticos, previniendo errores, pérdida de datos e incumplimiento.
- Seguridad del Paciente: Los sistemas debidamente validados contribuyen a la seguridad de los pacientes al garantizar una calidad constante y el cumplimiento de los estándares.
- Aspectos clave de la CSV:
- Definición de requisitos: Definir claramente los requisitos del sistema, las funcionalidades y las expectativas del usuario.
- Diseño y Configuración: Desarrolle y configure el sistema según las especificaciones.
- Pruebas y cualificación: Pruebas rigurosas (incluidas las pruebas unitarias, las pruebas de integración y las pruebas de aceptación del usuario) para verificar el rendimiento del sistema.
- Documentación: Mantener una documentación completa durante todo el ciclo de vida del sistema.
- Control de cambios: Gestionar los cambios en el sistema, asegurando que no comprometan su integridad.
- Desafíos abordados por CSV:
- Integridad de los Datos: Prevenir el acceso no autorizado, la corrupción o la manipulación de datos.
- Seguridad del Sistema: Protege contra ciberamenazas y modificaciones no autorizadas.
- Pista de auditoría: Mantenga una pista de datos electrónica indeleble para las auditorías reglamentarias.
- Mantenimiento de la validación: Revise y actualice regularmente la validación para adaptarse a los cambios del sistema.
¿En qué se diferencia la CSV de la Garantía de Sistemas Informáticos (CSA)?
Computer System Validation (CSV) y Computer System Assurance (CSA) representan enfoques distintos para asegurar la integridad y el cumplimiento de los sistemas informatizados en la industria farmacéutica. CSV, una práctica de larga trayectoria, se centra principalmente en la fase de validación del ciclo de vida de un sistema, asegurando que los sistemas de software cumplen los requisitos reglamentarios a través de protocolos predefinidos. Por otro lado, CSA adopta un enfoque más amplio y dinámico, que abarca todo el ciclo de vida de un sistema informatizado, desde el desarrollo y la implementación hasta el uso operativo y su eventual retirada.
CSV aborda la necesidad de procesos de validación rigurosos, haciendo hincapié en enfoques basados en el riesgo para identificar y mitigar posibles problemas. Sin embargo, el panorama farmacéutico está evolucionando, lo que impulsa la aparición de CSA como una estrategia más integral. CSA amplía su enfoque más allá de la validación al adaptar metodologías ágiles e incorporar un monitoreo continuo a lo largo del ciclo de vida de un sistema. Esta perspectiva integral permite a las organizaciones gestionar los riesgos de forma proactiva, especialmente en ciberseguridad e integridad de datos, alineándose con el creciente énfasis de la industria en la tecnología y la seguridad de los datos.
La adaptabilidad del CSA resulta muy valiosa en un entorno normativo en rápida evolución. Mientras que el CSV se ajusta a las prácticas de validación tradicionales, el CSA se adapta a las expectativas cambiantes de las autoridades reguladoras. Va más allá de los esfuerzos de revalidación periódicos, incorporando una supervisión continua, el análisis de datos en tiempo real y estrategias proactivas de gestión de riesgos para garantizar el cumplimiento normativo constante y un rendimiento óptimo. A medida que la industria farmacéutica adopta la transformación digital, comprender las diferencias entre CSV y CSA se convierte en algo imprescindible para las empresas que desean mantenerse a la vanguardia en materia de cumplimiento normativo e integridad de los sistemas.
En este contexto, Freyr, con su amplia experiencia y conocimientos, está bien equipada para guiar a las empresas farmacéuticas a través de las complejidades tanto de CSV como de CSA, ofreciendo soluciones personalizadas para satisfacer las crecientes demandas del cumplimiento reglamentario y los avances tecnológicos.
¿Cuáles son los componentes de un programa CSA?
Garantía de Software Informático (CSA) es un enfoque moderno que mejora la fiabilidad, la seguridad y el cumplimiento en los sistemas informatizados. Exploremos sus componentes y beneficios a largo plazo:
- Enfoque Basado en Riesgos:
- Componente: CSA se enfoca en la evaluación y gestión de riesgos.
- Importancia: Identificar áreas críticas ayuda a asignar los esfuerzos de validación de manera eficaz.
- Pruebas No Guiadas:
- Componente: CSA incluye pruebas no guionadas que van más allá de los casos de prueba guionados tradicionales.
- Importancia: Las pruebas no guionizadas imitan escenarios del mundo real, revelando problemas ocultos.
- Monitoreo continuo del rendimiento:
- Componente: CSA implica la supervisión continua del rendimiento del sistema.
- Importancia: Detectar anomalías a tiempo previene fallos del sistema y problemas de integridad de los datos.
- Supervisión de Datos:
- Componente: CSA enfatiza la calidad y la integridad de los datos.
- Importancia: Asegura datos precisos para la toma de decisiones y el cumplimiento normativo.
- Actividades de validación externas:
- Componente: CSA colabora con proveedores de software para la validación externa.
- Importancia: La validación independiente aporta confianza y reduce el sesgo.
- Transición de CSV a CSA:
- Pasos Iniciales:
- Comprender los principios de CSA.
- Evaluar los sistemas existentes para detectar riesgos.
- Priorizar las funcionalidades críticas.
- Beneficios:
- Carga de trabajo de validación reducida.
- Respuesta ágil a los cambios.
- Fiabilidad del sistema mejorada.
- Pasos Iniciales:
- Fiabilidad del sistema a largo plazo:
- CSA garantiza:
- Adaptabilidad: Los sistemas evolucionan sin comprometer la fiabilidad.
- Seguridad: Protección contra ciberamenazas.
- Cumplimiento: Alineación continua con las regulaciones.
- Calidad: Calidad consistente de datos y productos.
- CSA garantiza:
Cómo contribuye la CSA a la integridad de los datos en la industria farmacéutica?
CSA mantiene la integridad de los datos en la industria farmacéutica al garantizar la exactitud, la coherencia y la fiabilidad de los datos a lo largo del ciclo de vida de un sistema. A diferencia de los enfoques tradicionales, CSA adopta una estrategia integral que va más allá de la validación, abordando activamente los posibles desafíos y discrepancias que puedan surgir con el tiempo.
Una contribución de CSA a la integridad de los datos reside en sus capacidades de monitoreo continuo. En lugar de depender únicamente de los esfuerzos de validación periódicos, CSA implica análisis de datos en tiempo real y medidas proactivas de gestión de riesgos. Este enfoque permite a las organizaciones detectar y abordar posibles discrepancias en los datos, evitando que las imprecisiones se acumulen con el tiempo. El énfasis de CSA en un modelo de ciclo de vida dinámico y adaptativo asegura que la integridad de los datos siga siendo un enfoque constante, alineándose con las expectativas reglamentarias.
Para prevenir discrepancias en los datos a lo largo del tiempo, CSA incorpora varias medidas estratégicas. En primer lugar, emplea procesos robustos de control de cambios, documentando meticulosamente cualquier modificación en los sistemas informatizados o procesos que puedan afectar la integridad de los datos. Se realizan auditorías y evaluaciones regulares del sistema para identificar y rectificar posibles problemas antes de que se agraven. Además, CSA enfatiza la importancia de los programas de capacitación y concienciación del usuario para asegurar que el personal comprenda la importancia de mantener la integridad de los datos y se adhiera a las mejores prácticas.
En conclusión, el enfoque proactivo y exhaustivo de CSA hacia la integridad de los datos lo distingue como una solución estratégica en la industria farmacéutica. Al incorporar monitoreo continuo, gestión de riesgos y medidas estrictas de control de cambios, CSA mantiene la integridad de los datos y asegura que las empresas farmacéuticas estén bien preparadas para navegar el panorama cambiante de las expectativas reglamentarias. A medida que las organizaciones se esfuerzan por mantener los más altos estándares en integridad de datos, CSA emerge como un aliado clave en su camino, alineándose con las tendencias de la industria y los avances reglamentarios.
Para las organizaciones que buscan orientación sobre cómo implementar estrategias CSA efectivas, Freyr es un socio fiable que ofrece soluciones personalizadas para abordar los desafíos únicos del panorama farmacéutico.
¿Qué papel desempeña el cumplimiento reglamentario en CSA?
El cumplimiento reglamentario es un pilar fundamental de la CSA, asegurando que las empresas farmacéuticas se adhieran a los estándares y directrices en constante evolución a lo largo del ciclo de vida de un sistema. A diferencia del enfoque tradicional de la Validación de Sistemas Computarizados (CSV), la CSA enfatiza el cumplimiento continuo y la adaptabilidad a los cambiantes panoramas reglamentarios. A medida que las empresas hacen la transición de CSV a CSA, mantenerse actualizado sobre las regulaciones en evolución se vuelve primordial.
En el contexto de la CSA, el cumplimiento reglamentario implica alinear los sistemas informatizados con los requisitos reglamentarios globales y locales, desde el desarrollo hasta el uso operativo y su eventual retirada. La CSA enfatiza el cumplimiento continuo en lugar de la validación periódica, fomentando un enfoque proactivo para abordar rápidamente los posibles cambios reglamentarios. Esta alineación estratégica garantiza que las empresas farmacéuticas estén bien preparadas para cumplir las expectativas reglamentarias, salvaguardando la integridad de los datos, la seguridad del paciente y la fiabilidad general del sistema.

El compromiso regular con las autoridades normativas, la participación en foros de la industria y la suscripción a publicaciones normativas proporcionan información valiosa sobre los estándares en evolución. Aprovechar la experiencia de los consultores normativos e invertir en formación continua para el personal involucrado en los procesos CSA mejora aún más la concienciación normativa. Colaborar con socios normativos, como Freyr Solutions, ofrece un enfoque proactivo, asegurando el acceso a inteligencia normativa actualizada y soluciones personalizadas para navegar sin problemas la transición.
El cumplimiento reglamentario en CSA es un compromiso dinámico y continuo que se alinea con el cambio de la industria hacia la adaptabilidad y la mejora continua. Mantenerse informado, ser proactivo y asociarse con expertos reglamentarios son aspectos cruciales para las empresas que hacen la transición de CSV a CSA, facilitando una evolución fluida y conforme en el panorama farmacéutico en constante cambio.
Como socio reglamentario de confianza, Freyr proporciona el apoyo y la experiencia necesarios para guiar a las empresas a través de esta transición, garantizando la excelencia reglamentaria y el cumplimiento en la era de la CSA.
¿Cómo ayuda un socio estratégico de cumplimiento reglamentario?
Un socio estratégico de cumplimiento reglamentario desempeña un papel fundamental para garantizar que las empresas farmacéuticas cumplan con los requisitos reglamentarios y mantengan altos estándares de calidad. Así es como pueden ayudar:
- Asesoramiento Experto: Un socio estratégico proporciona asesoramiento experto para navegar regulaciones complejas y en evolución en diferentes regiones. Ofrecen información sobre los últimos cambios reglamentarios, ayudando a las empresas a ajustar sus prácticas y mantener el cumplimiento.
- Procesos Optimizados: Ayudan a optimizar los procesos de cumplimiento mediante la implementación de mejores prácticas y flujos de trabajo eficientes. Esto incluye el desarrollo de sistemas robustos para la documentación, auditoría y validación, reduciendo las cargas administrativas y mejorando la eficiencia general.
- Mitigación de Riesgos: Al identificar posibles riesgos y vulnerabilidades de cumplimiento, un socio estratégico ayuda a mitigar los riesgos antes de que se conviertan en problemas. Realizan auditorías y evaluaciones exhaustivas para asegurar que todos los procesos cumplan con la normativa y aborden cualquier deficiencia de manera proactiva.
- Formación y apoyo: Ofrecen formación y apoyo para asegurar que el personal esté bien informado sobre los requisitos reglamentarios y las mejores prácticas. Esto ayuda a desarrollar la competencia interna y garantiza que todos los involucrados en las actividades de cumplimiento estén al día con los estándares actuales.
- Integración Tecnológica: Un socio estratégico ayuda con la integración de tecnologías innovadoras, como la automatización y la IA, en los procesos de cumplimiento. Garantizan que estas tecnologías se implementen de manera efectiva y de acuerdo con los requisitos regulatorios, mejorando la integridad de los datos y la eficiencia del proceso.
- Documentation and Record-Keeping: Gestionan la creación, organización y mantenimiento de documentación de cumplimiento crucial. Esto asegura que todos los registros sean precisos, completos y fácilmente accesibles para auditorías e inspecciones.
- Presentaciones y aprobaciones reglamentarias: Se encargan de la preparación y presentación de documentos y solicitudes reglamentarias. Esto incluye asegurar que las presentaciones cumplan con todos los requisitos necesarios y gestionar las comunicaciones con las autoridades reglamentarias para facilitar aprobaciones oportunas.
- Acciones Correctivas y Preventivas: Un socio estratégico apoya el desarrollo y la implementación de acciones correctivas y preventivas en respuesta a los hallazgos de auditorías o problemas de cumplimiento. Ayudan a asegurar que estas acciones sean efectivas y no interrumpan las operaciones en curso.
- Estrategia de cumplimiento global: Desarrollan e implementan estrategias para lograr el cumplimiento global, abordando los diversos requisitos reglamentarios de los diferentes mercados. Esto garantiza que los productos cumplan con todos los estándares necesarios para su distribución y uso internacional.
- Monitoreo continuo: Proporcionan monitoreo y soporte continuos para mantener a las empresas informadas de cualquier actualización o cambio reglamentario. Este enfoque proactivo ayuda a las empresas a mantenerse conformes y a adaptarse a las nuevas normativas a medida que surgen.
¿Por qué elegir a Freyr?
Más de diez años de excelencia en cumplimiento reglamentario.
Amplio espectro de cumplimiento, auditoría y validación.
Experiencia en diversas industrias y geografías.
Utiliza herramientas innovadoras para resultados precisos.
Profesionales cualificados con profundo conocimiento de la industria.
Gestión exitosa de desafíos complejos de cumplimiento.
Preguntas Frecuentes.
El cumplimiento farmacéutico implica adherirse a las leyes, regulaciones y directrices que rigen la industria farmacéutica. Asegura que las empresas alineen sus operaciones con los estándares de la industria, salvaguardando así la seguridad y eficacia del producto, al tiempo que mantienen la integridad de los datos.
El propósito de una auditoría es evaluar sistemáticamente la adhesión de una empresa a los estándares reglamentarios y las políticas internas. Las auditorías ayudan a identificar áreas de mejora, mitigar riesgos y asegurar que los procesos sean efectivos en la producción de productos farmacéuticos seguros y conformes.
La validación en la industria farmacéutica es el proceso de confirmar que los sistemas, procesos y equipos cumplen consistentemente con los requisitos predefinidos. Es esencial para asegurar el cumplimiento de los estándares reglamentarios y para mantener la calidad y seguridad de los productos farmacéuticos a lo largo de su ciclo de vida.
¿Cuál es la importancia del cumplimiento, la auditoría y la validación en la industria farmacéutica?
Estos procesos son críticos para asegurar la seguridad y eficacia del producto, mantener la adhesión reglamentaria, mejorar la garantía de calidad, apoyar el acceso al mercado y facilitar la mejora continua. Ayudan a las empresas a cumplir con estándares rigurosos y a generar confianza con las partes interesadas.
Los desafíos incluyen manejar las normativas en evolución, garantizar la integridad de los datos, gestionar las limitaciones de recursos y mantener una documentación adecuada. Además, integrar tecnologías innovadoras y asegurar la competencia del personal puede complicar los esfuerzos de cumplimiento.
Las auditorías GxP son evaluaciones realizadas para garantizar la adhesión a los estándares de Buenas Prácticas (GxP), que incluyen las Buenas Prácticas de Fabricación (GMP), las Buenas Prácticas Clínicas (GCP) y las Buenas Prácticas de Laboratorio (GLP). Estas auditorías ayudan a identificar brechas de cumplimiento y mejorar los sistemas de calidad.
Una auditoría de cumplimiento independiente GxP es una evaluación objetiva de la adhesión de una empresa a los estándares de calidad y reglamentarios. Realizada por auditores cualificados, identifica riesgos y áreas de mejora, mejorando el cumplimiento y la seguridad del producto.
Las auditorías GxP proporcionan evaluaciones imparciales, mejoran el cumplimiento reglamentario e identifican áreas para la mejora operativa. Ayudan a mantener altos estándares de calidad y a generar confianza con los reguladores y los clientes.
CSV garantiza que los sistemas informatizados utilizados en productos farmacéuticos produzcan datos fiables de forma consistente y cumplan con los requisitos reglamentarios. Es vital para mantener la integridad de los datos, mitigar los riesgos y garantizar la seguridad del paciente a lo largo del ciclo de vida del producto.
CSV se centra en validar que un sistema cumple con los requisitos reglamentarios y funciona según lo previsto, mientras que CSA abarca un enfoque más amplio que incluye la garantía continua del rendimiento y el cumplimiento del sistema a lo largo de su ciclo de vida.














