Servicios globales de etiquetado reglamentario farmacéutico
Aproveche una década de experiencia con nuestros servicios de Etiquetado Reglamentario, que cubren las autorizaciones de nuevos productos, las presentaciones a las Autoridades Sanitarias, las post-aprobaciones, el CMC y la gestión del ciclo de vida. Nuestro enfoque en la excelencia global y local garantiza la creación y actualización estratégica de documentos de etiquetado esenciales como IBs, CDS y CCDS, garantizando el cumplimiento y el éxito en la industria farmacéutica.
Explorar temas
- ¿Qué es el Etiquetado Reglamentario?
- ¿Por qué es importante el etiquetado reglamentario en la industria farmacéutica?
- ¿Qué es el proceso de aprobación de etiquetado?
- ¿Cuáles son los desafíos comunes en el etiquetado reglamentario?
- ¿Cuáles son las regulaciones clave que rigen el etiquetado farmacéutico?
- ¿Cómo puede un socio reglamentario ayudar a lograr el cumplimiento de los requisitos de etiquetado?
- ¿Cómo pueden las empresas empezar con los servicios de etiquetado reglamentario?
- ¿Pueden los servicios de etiquetado reglamentario ayudar en la vigilancia post-comercialización?
- ¿Por qué elegir a Freyr?
- Nuestros servicios
¿Qué es el Etiquetado Reglamentario?
Última actualización: Agosto de 2024
El etiquetado reglamentario farmacéutico implica la creación, revisión y gestión de documentos fundamentales que comunican información esencial del producto a las partes interesadas, asegurando el cumplimiento de las normas reglamentarias globales. Los componentes principales incluyen el Core Data Sheet (CDS) y el Company Core Data Sheet (CCDS), derivados de fuentes como los folletos para investigadores (IB) y los datos de poscomercialización. Este proceso es fundamental para transmitir información de seguridad y eficacia en las etiquetas específicas de cada país y para alinearse con los requisitos de las autoridades sanitarias (HA).
Con un enfoque en la armonización global, el etiquetado reglamentario farmacéutico aborda las demandas reglamentarias en evolución, que abarcan nuevas autorizaciones de productos, presentaciones a las autoridades sanitarias, aprobaciones posteriores y gestión del ciclo de vida. La precisión y la adhesión a las directrices en evolución son cruciales para un etiquetado reglamentario farmacéutico exitoso, influyendo en la autorización de comercialización de un producto, su perfil de seguridad y su viabilidad reglamentaria general.

Freyr, un líder en servicios End-to-End de etiquetado reglamentario de medicamentos, cuenta con un equipo dedicado de más de 180 expertos globales en etiquetado, que se destaca en la redacción de documentos cruciales como los Folletos del Investigador (IB), las Fichas de Datos Centrales de Desarrollo y la Información Central de Seguridad de Desarrollo. El aprovechamiento de la inteligencia artificial mejora la precisión y agiliza la implementación y revisión de las fichas de datos. Con una plantilla de CCDS optimizada y procesos impulsados por la precisión, los servicios integrales de Freyr satisfacen eficazmente las necesidades dinámicas de la industria farmacéutica, proporcionando un apoyo inigualable para el cumplimiento del etiquetado y el éxito reglamentario.
¿Por qué es importante el etiquetado reglamentario en la industria farmacéutica?
- Garantizar la seguridad del paciente y la comunicación de información: El etiquetado reglamentario es crucial para la seguridad del paciente. Las etiquetas proporcionan información esencial sobre el uso del medicamento, las dosis, los efectos secundarios y las contraindicaciones. Los pacientes, los médicos prescriptores, los profesionales de la salud y los cuidadores confían en estas etiquetas para tomar decisiones informadas. Un etiquetado claro y preciso reduce el riesgo de errores de medicación, eventos adversos y uso indebido.
Asegura que los pacientes reciban el tratamiento correcto y comprendan su uso adecuado. Además, las autoridades reglamentarias exigen que cada producto farmacéutico en el mercado tenga un etiquetado para comunicar la información del tratamiento de manera efectiva. - Cumplimiento y mitigación de riesgos: El cumplimiento de las normativas de etiquetado no es solo una formalidad; es un requisito legal. Organismos reglamentarios como la FDA de US, la EMA y otros exigen un etiquetado preciso y completo. El incumplimiento puede resultar en multas reglamentarias, daño a la reputación de la marca e incluso cierres temporales de la línea de producción. Las empresas farmacéuticas deben demostrar que sus procesos, métodos, pruebas y equipos de etiquetado son capaces de producir consistentemente productos seguros y efectivos. Un etiquetado correctamente validado mitiga los riesgos y asegura la adhesión a las buenas prácticas de fabricación (GMP).
- Acceso al mercado y armonización global: Las etiquetas bien estructuradas facilitan el acceso al mercado global. Un etiquetado consistente en todas las regiones agiliza los procesos, reduce las redundancias y se alinea con los estándares armonizados. A medida que los reguladores internacionales adoptan los requisitos de validación GMP, incluida la serialización, las cadenas de suministro farmacéuticas se enfrentan a una complejidad creciente. Las empresas que priorizan el cumplimiento del etiquetado generan confianza, mejoran la aceptación en el mercado y se posicionan para el éxito en un panorama competitivo.
¿Qué es el proceso de aprobación de etiquetado?
El proceso de aprobación del etiquetado en la industria farmacéutica implica múltiples etapas para asegurar que toda la información relacionada con el medicamento sea precisa, conforme y clara tanto para los profesionales de la salud como para los pacientes. Comienza con la redacción del contenido de la etiqueta, que incluye detalles sobre la dosificación, administración, seguridad y advertencias. Los equipos reglamentarios y médicos revisan internamente este borrador para asegurar que se alinee con los estándares reglamentarios locales e internacionales. Una vez finalizada, la etiqueta se presenta a las autoridades sanitarias para su aprobación, donde se somete a un escrutinio riguroso para verificar su cumplimiento con los requisitos de seguridad y eficacia. Solo después de recibir la aprobación oficial se puede utilizar la etiqueta para la comercialización del medicamento.
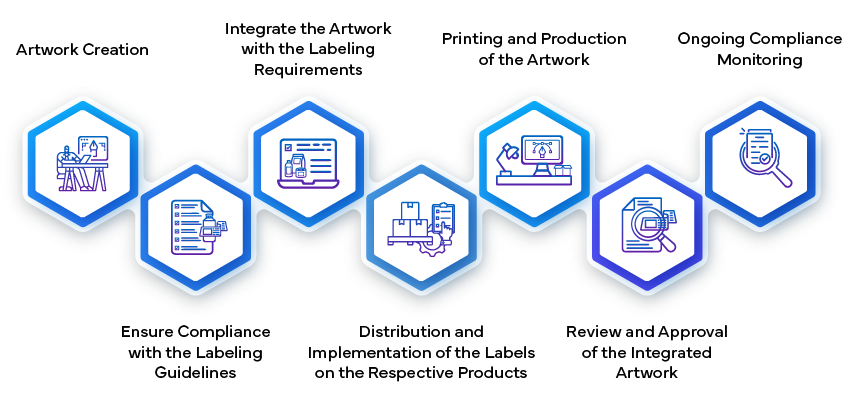
- Creación y presentación de la etiqueta:
- Recopilación inicial de datos: Las empresas farmacéuticas recopilan todos los datos relevantes para la etiqueta del medicamento. Esto incluye información sobre la eficacia, seguridad, dosis, indicaciones, contraindicaciones y riesgos potenciales. La etiqueta sirve como una herramienta de comunicación fundamental para los profesionales de la salud y los pacientes.
- Presentación a las Autoridades Reglamentarias: La empresa presenta los datos de la etiqueta a los organismos reglamentarios, como la Administración de Alimentos y Medicamentos de US (FDA) o la Agencia Europea de Medicamentos (EMA). Estas agencias evalúan los datos para asegurar que el medicamento proporciona beneficios que superan sus riesgos conocidos y potenciales para la población prevista.
- Análisis contextual: Los revisores analizan la condición o enfermedad objetivo para la cual está destinado el medicamento. Consideran el panorama de tratamiento existente, sopesando los riesgos del medicamento frente a sus beneficios. Por ejemplo, un medicamento que trata una enfermedad potencialmente mortal sin terapia alternativa puede ser aprobado incluso si los riesgos serían inaceptables para una condición no potencialmente mortal.
- Evaluación de datos clínicos: Los revisores de la FDA evalúan la información sobre el beneficio clínico y el riesgo presentada por el fabricante del medicamento. Tienen en cuenta cualquier incertidumbre que surja de datos imperfectos o incompletos. Normalmente, la agencia espera resultados de ensayos clínicos bien diseñados para validar la eficacia y seguridad del medicamento.
- Establecimiento del Artwork:
- Una vez que se aprueba el contenido de la etiqueta, el siguiente paso es crear el Artwork de la etiqueta. Esto implica diseñar los elementos visuales, el diseño, las fuentes y los gráficos. El Artwork debe alinearse con las directrices reglamentarias y representar con precisión la información de la etiqueta.
- El artwork de la etiqueta se somete a revisiones internas dentro de la empresa farmacéutica para garantizar la coherencia y el cumplimiento. Incluye detalles como instrucciones de dosificación, advertencias, condiciones de almacenamiento e información de contacto.
- La Artwork final se presenta a las autoridades reglamentarias para su aprobación. Este paso asegura que la presentación visual de la etiqueta cumple con los estándares de calidad y comunica eficazmente información esencial a los usuarios.
- Fabricación e Implementación:
- Una vez aprobado, el Artwork de la etiqueta se convierte en una parte integral del empaque del medicamento. Los fabricantes se aseguran de que las etiquetas se adhieran correctamente a cada unidad de producto (por ejemplo, frascos, blísteres, viales).
- Los procedimientos de control de calidad verifican que las etiquetas cumplan con las especificaciones, incluyendo contenido preciso, legibilidad y adhesión a las directrices de diseño.
- La etiqueta sirve como un puente entre la compañía farmacéutica, las agencias reglamentarias, los profesionales de la salud y los pacientes. Desempeña un papel vital para asegurar el uso seguro y efectivo de los medicamentos a lo largo del ciclo de vida del producto.
¿Cuáles son los desafíos comunes en el etiquetado reglamentario?
Los desafíos comunes en el etiquetado reglamentario incluyen mantenerse al día con los requisitos reglamentarios en evolución, la gestión del etiquetado multilingüe y la garantía de coherencia en diversas carteras de productos. La naturaleza dinámica de las normas reglamentarias para el etiquetado farmacéutico exige una vigilancia continua para mantenerse al día con los últimos requisitos. Adaptarse a los cambios en la normativa e implementar rápidamente las actualizaciones necesarias en el contenido y formato del etiquetado es esencial para mantener el cumplimiento y garantizar la seguridad del paciente.
| Desafío | Descripción |
|---|---|
| Requisitos reglamentarios en evolución | Gestionar los cambios continuos en las regulaciones y directrices, lo que requiere actualizaciones constantes de la documentación de etiquetado. |
| Armonización Global | Garantizar la coherencia en la información del producto en diversas regiones, alineándose con los variados requisitos de las diferentes autoridades sanitarias. |
| Integración de datos post-comercialización | Gestión de la incorporación de datos de seguridad y eficacia poscomercialización en el etiquetado, manteniendo la precisión y la relevancia. |
| Cumplimiento con los estándares de etiquetado locales | Adherirse a los estándares de etiquetado específicos de cada país, abordando las variaciones lingüísticas, culturales y de formato. |
| Gestión eficiente de cambios en el etiquetado | Agilizar los procesos para el seguimiento, la implementación y la documentación de los cambios en el etiquetado de manera rápida y precisa. |
El etiquetado multilingüe representa un desafío significativo para las compañías farmacéuticas que operan en mercados globales. Traducir con precisión el contenido del etiquetado a múltiples idiomas, mientras se adhiere a los matices lingüísticos y reglamentarios regionales, requiere atención al detalle y procesos robustos de gestión de traducción. Asegurar la consistencia y claridad entre las diferentes versiones lingüísticas es crucial para comunicar eficazmente información vital a diversas poblaciones de pacientes.
Mantener la coherencia en todas las carteras de productos presenta otro desafío común en el etiquetado reglamentario. Las empresas farmacéuticas a menudo gestionan varios productos con diferentes requisitos de etiquetado, formulaciones e indicaciones. Lograr la coherencia y el cumplimiento en diversas líneas de productos, al tiempo que se satisfacen las demandas reglamentarias específicas para cada producto, requiere procesos y sistemas eficientes para garantizar la uniformidad en el contenido, formato y mensaje del etiquetado.
¿Cuáles son las regulaciones clave que rigen el etiquetado farmacéutico?
El etiquetado farmacéutico se rige por un conjunto complejo de regulaciones diseñado para asegurar la seguridad, eficacia y uso preciso de los medicamentos. A continuación se enumeran algunas de ellas:
US FDA (Administración de Alimentos y Medicamentos de los Estados Unidos)
La US FDA rige el etiquetado farmacéutico a través de un conjunto estricto de regulaciones descritas en el Título 21 del Código de Regulaciones Federales (CFR). Estas regulaciones requieren que las etiquetas proporcionen información completa, incluyendo indicaciones del medicamento, instrucciones de uso, contraindicaciones y posibles efectos secundarios. La FDA enfatiza la importancia de un lenguaje claro, preciso e inequívoco para garantizar la seguridad del paciente y la toma de decisiones informada por parte de los profesionales de la salud. Además, los requisitos de etiquetado de la FDA se extienden a varios aspectos como el empaque, los prospectos y el etiquetado electrónico, asegurando que toda la información sea accesible y estandarizada en diferentes formatos. El cumplimiento de estas regulaciones es obligatorio para la aprobación de medicamentos y su presencia continua en el mercado de los Estados Unidos.
EMA (Agencia Europea de Medicamentos)
La EMA supervisa el etiquetado farmacéutico en la Unión Europea a través de directivas y directrices diseñadas para armonizar el etiquetado en los Member States. La Directiva 2001/83/CE de la Comisión Europea es fundamental para estos esfuerzos, especificando los requisitos para el Resumen de las Características del Producto (SmPC), los prospectos para pacientes y las etiquetas de los envases. La EMA garantiza que el etiquetado incluya información esencial tanto para los profesionales de la salud como para los pacientes, promoviendo el uso seguro y eficaz de los medicamentos en toda la EU (European Union). Además, el etiquetado debe estar disponible en los idiomas oficiales de los Member States donde se comercializa el medicamento, lo que refleja el compromiso de la EMA con la accesibilidad y la atención centrada en el paciente.
TGA (Therapeutic Goods Administration)
En Australia, la TGA es responsable de regular el etiquetado farmacéutico bajo la Ley de Productos Terapéuticos de 1989. Las directrices de la TGA exigen que las etiquetas de los medicamentos proporcionen información clara, precisa y completa sobre el producto, incluyendo sus ingredientes, indicaciones, dosificación y riesgos potenciales. Los requisitos de etiquetado están diseñados para proteger la salud pública, asegurando que los consumidores y los profesionales de la salud tengan la información necesaria para usar los medicamentos de manera segura y efectiva. La TGA también pone un énfasis significativo en la legibilidad de las etiquetas, exigiendo que estén escritas en inglés sencillo y que la información crítica se muestre de manera destacada para prevenir el uso indebido y los errores de medicación.
Health Canada
Health Canada regula el etiquetado farmacéutico a través de un marco que prioriza la seguridad y el bienestar de los pacientes y los profesionales de la salud. La Ley de Alimentos y Medicamentos y sus reglamentos asociados establecen los requisitos para las etiquetas de los medicamentos, que deben incluir información detallada sobre la composición del producto, indicaciones, contraindicaciones y posibles efectos secundarios. Health Canada también exige que las etiquetas sean bilingües, presentadas tanto en inglés como en francés, para adaptarse a la diversidad lingüística del país. Además, Health Canada actualiza regularmente sus requisitos de etiquetado para reflejar nuevas pruebas científicas y las necesidades cambiantes de salud pública, asegurando que el etiquetado siga siendo relevante y eficaz para promover el uso seguro de los medicamentos.
PMDA (Agencia de Productos Farmacéuticos y Dispositivos Médicos)
La PMDA, la autoridad reglamentaria de Japón, supervisa el etiquetado farmacéutico de acuerdo con la Ley de Asuntos Farmacéuticos y las directrices relacionadas. La PMDA exige que las etiquetas de los medicamentos proporcionen información completa, incluidas las indicaciones, las instrucciones de dosificación y los posibles efectos adversos, en un formato que sea fácilmente comprensible tanto para los profesionales de la salud como para los pacientes. La PMDA también exige que las etiquetas incluyan advertencias y precauciones específicas para la población japonesa, considerando factores como las diferencias genéticas y las prácticas culturales. Este enfoque garantiza que los medicamentos se utilicen de forma segura y eficaz en Japón, con un etiquetado adaptado a las necesidades únicas del mercado local.
NMPA (Administración Nacional de Productos Médicos)
En China, la NMPA rige el etiquetado farmacéutico a través de un marco reglamentario que enfatiza la precisión, la claridad y la seguridad. La Ley de Administración de Medicamentos de la República Popular China describe los requisitos para las etiquetas de los medicamentos, que deben incluir información sobre las indicaciones, la dosificación, las contraindicaciones y los posibles efectos secundarios del medicamento. La NMPA también exige que el etiquetado se presente en chino simplificado para garantizar la accesibilidad a la población local. Además, la NMPA exige que las etiquetas se sometan a una revisión rigurosa durante el proceso de aprobación de medicamentos para garantizar el cumplimiento de las normas nacionales y proteger la salud pública previniendo errores de medicación y uso indebido.
¿Cómo puede un socio reglamentario ayudar a lograr el cumplimiento de los requisitos de etiquetado?
Un socio reglamentario es fundamental para lograr el cumplimiento de los requisitos de etiquetado al ofrecer experiencia especializada y soporte integral. Guían a las empresas a través del complejo panorama reglamentario, asegurando que los materiales de etiquetado —incluidos envases, prospectos y etiquetas electrónicas— cumplan con los requisitos específicos de diferentes autoridades sanitarias como la US FDA, EMA, TGA, Health Canada, PMDA y NMPA. Esto implica comprender y aplicar las últimas normativas, que pueden variar significativamente entre regiones, para garantizar que toda la información del producto sea precisa, completa y conforme a la normativa.
Además, un socio reglamentario ayuda a optimizar el proceso de etiquetado al proporcionar servicios esenciales como la creación, revisión y validación de contenido. Ayudan a redactar y revisar el contenido del etiquetado para alinearlo con las normas reglamentarias y a garantizar que se incluya toda la información necesaria, desde las listas de ingredientes y las instrucciones de uso hasta las advertencias de seguridad y las condiciones de almacenamiento. Esto reduce el riesgo de errores y omisiones que podrían provocar retrasos reglamentarios o retiradas del mercado, acelerando el tiempo de comercialización de nuevos productos.

Además, un socio reglamentario apoya a las empresas en el mantenimiento del cumplimiento continuo mediante el monitoreo de las actualizaciones reglamentarias y la implementación de cambios según sea necesario. Ofrecen asesoramiento estratégico sobre cómo adaptar las etiquetas a las nuevas directrices o a los requisitos de los mercados emergentes, ayudando a las empresas a evitar problemas de incumplimiento y asegurando que sus productos se mantengan en línea con las regulaciones actuales. Al aprovechar su experiencia y mantenerse al tanto de los cambios reglamentarios, un socio reglamentario ayuda a las empresas a navegar por el dinámico panorama del etiquetado de manera eficiente y efectiva.
¿Cómo pueden las empresas empezar con los servicios de etiquetado reglamentario?
Para empezar con los servicios de etiquetado reglamentario, las empresas deben evaluar primero sus necesidades específicas de etiquetado en función de los mercados objetivo y los requisitos reglamentarios. A continuación, deben asociarse con un proveedor de servicios reglamentarios fiable con experiencia en estándares de etiquetado globales. Este proveedor puede ayudar en la redacción, revisión y actualización de etiquetas para garantizar el cumplimiento. Además, la implementación de un sistema centralizado de gestión de etiquetado ayuda a agilizar el proceso, asegurando la coherencia en todas las etiquetas de los productos. Las auditorías y actualizaciones periódicas son esenciales para mantener las etiquetas alineadas con las regulaciones en evolución.
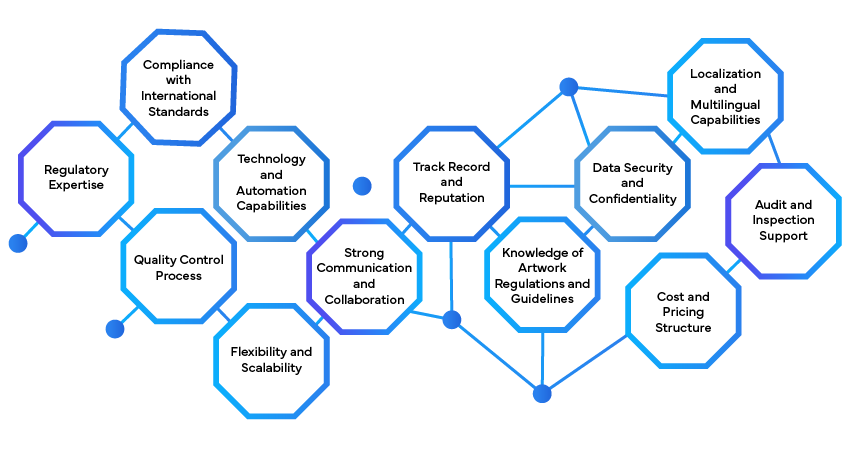
Evaluar las necesidades reglamentarias:
- Identifique los requisitos reglamentarios específicos aplicables a su producto y mercados objetivo.
- Comprenda los documentos críticos, como las Fichas de Datos Centrales (CDS), los Folletos del Investigador (IB) y los requisitos de etiquetado locales.
Seleccione un Socio de Etiquetado Reglamentario:
- Investigue y elija un proveedor de servicios de etiquetado reglamentario de buena reputación con experiencia en su industria.
- Considere factores como la experiencia, el conocimiento reglamentario global y la capacidad para manejar diversos desafíos de etiquetado.
Definir el alcance del proyecto:
- Defina claramente el alcance de su proyecto de etiquetado reglamentario, incluyendo el tipo de servicios requeridos (p. ej., redacción de IB, creación de CCDS, revisión de cumplimiento del etiquetado).
- Establecer plazos, hitos y entregables para cada fase del proyecto.
Colabore en la recopilación de datos:
- Colabore estrechamente con su socio de etiquetado reglamentario elegido para recopilar datos esenciales, incluyendo información de ensayos clínicos, datos de seguridad y eficacia, y cualquier dato de farmacovigilancia poscomercialización.
Iniciar la Creación y Revisión de Documentos:
- Comience la creación o revisión de documentos cruciales como IBs, DCDS, CCDS y el contenido de etiquetado local.
- Facilitar revisiones periódicas y sesiones de retroalimentación para garantizar la precisión y la alineación con los requisitos reglamentarios.
Implementar procesos de control de cambios:
- Desarrollar procesos sólidos de control de cambios para las actualizaciones de etiquetado y realizar un seguimiento rápido de cualquier modificación en los documentos principales.
- Asegurar que los cambios se implementen de manera consistente en las etiquetas globales y regionales.
Supervisar el cumplimiento:
- Establecer mecanismos para el monitoreo continuo del cumplimiento con los estándares reglamentarios en evolución.
- Manténgase informado sobre los cambios en las regulaciones y actualice los documentos de etiquetado según corresponda.
Utilice la Tecnología y la Automatización:
- Utilizar software y tecnología de etiquetado reglamentario para mejorar la precisión, la eficiencia y la gestión de documentos.
- Explore herramientas que utilizan inteligencia artificial para agilizar los procesos de implementación y revisión de fichas técnicas.
Contratar Expertos Reglamentarios:
- Contratar a expertos o consultores reglamentarios dentro de su organización o a través de su proveedor de servicios elegido para proporcionar conocimientos y orientación durante todo el proceso de etiquetado.
Mejora Continua:
- Establecer una cultura de mejora continua, revisando y perfeccionando regularmente los procesos de etiquetado basándose en la retroalimentación, los cambios de la industria y los panoramas reglamentarios en evolución.
¿Pueden los servicios de etiquetado reglamentario ayudar en la vigilancia post-comercialización?
Sí, los servicios de etiquetado reglamentario pueden, de hecho, ayudar en el seguimiento post-comercialización de productos farmacéuticos. Estos servicios desempeñan un papel crucial en el apoyo a la vigilancia post-comercialización al facilitar la gestión de las actualizaciones de etiquetado, gestionar los cambios de etiquetado relacionados con la seguridad y asegurar el cumplimiento de los requisitos reglamentarios post-aprobación. Al mantener información de etiquetado precisa y actualizada, los servicios de etiquetado reglamentario ayudan a las empresas farmacéuticas a responder a las preocupaciones de seguridad e implementar los cambios necesarios de manera oportuna para apoyar el cumplimiento reglamentario continuo y la seguridad del paciente.
Además, los servicios de etiquetado reglamentario pueden ayudar en la difusión eficiente de información de seguridad actualizada a profesionales de la salud y pacientes. En caso de nuevos hallazgos de seguridad o cambios en los perfiles de riesgo de los productos farmacéuticos, los expertos en etiquetado reglamentario pueden ayudar a actualizar rápidamente el contenido del etiquetado para reflejar los últimos datos de seguridad y los requisitos reglamentarios. Este enfoque proactivo para la monitorización post-comercialización y las actualizaciones de etiquetado apoya la comunicación oportuna de información de seguridad importante a los proveedores de atención médica y a los pacientes, contribuyendo a una farmacovigilancia y atención al paciente mejoradas.
En general, los servicios de etiquetado reglamentario proporcionan un apoyo valioso en la vigilancia post-comercialización al asegurar que los productos farmacéuticos mantengan un etiquetado preciso y conforme a la normativa a lo largo de su ciclo de vida. Al aprovechar la experiencia de los profesionales reglamentarios y los procesos eficientes de gestión de etiquetado, las empresas pueden abordar eficazmente las consideraciones de seguridad post-comercialización y las obligaciones reglamentarias, contribuyendo así a la seguridad y eficacia continuas de sus productos en el mercado.
¿Por qué elegir a Freyr?
Una década de excelencia en etiquetado reglamentario
Más de 180 expertos globales en servicios de etiquetado
Se especializa en la creación y gestión de documentos esenciales
Experiencia en folletos para investigadores, hojas de datos centrales y hojas de datos centrales de la empresa
Comprometidos con el cumplimiento global y la precisión.
Utiliza IA (Inteligencia Artificial) para una navegación reglamentaria eficiente
Datos clave
+
+
+
Preguntas Frecuentes.
Las Fichas de Datos Centrales (CDS) proporcionan un resumen consolidado de información fundamental sobre medicamentos, incluyendo indicaciones, dosis y perfiles de seguridad. Aseguran una comunicación coherente de los detalles esenciales en los mercados globales, facilitando el cumplimiento reglamentario y la toma de decisiones informadas. Las CDS también sirven como referencia para la creación de etiquetas de productos locales.
Los Folletos del Investigador (IB) detallan los datos de ensayos clínicos y la información sobre el desarrollo de fármacos para uso en investigación, mientras que los Company Core Data Sheets (CCDS) resumen los datos clave de seguridad y eficacia para fines reglamentarios globales, guiando el contenido y las actualizaciones de las etiquetas. Los CCDS se utilizan para crear etiquetas específicas de productos para la aprobación de comercialización.
La inteligencia artificial mejora el etiquetado reglamentario al automatizar el análisis de datos, mejorar la precisión en la creación de contenido y agilizar las revisiones de documentos. Las herramientas de IA optimizan los procesos de etiquetado y garantizan la coherencia en los diversos requisitos reglamentarios. También ayudan a predecir y abordar posibles problemas de cumplimiento.
El etiquetado multilingüe asegura que los productos farmacéuticos sean accesibles para diversas poblaciones de pacientes, cumpliendo con los requisitos reglamentarios regionales y mejorando la seguridad al proporcionar instrucciones y advertencias claras y comprensibles en varios idiomas. Esto reduce el riesgo de errores de comunicación y de administración de medicamentos.
Un sistema centralizado de gestión de etiquetado coordina la creación, revisión y actualización de los documentos de etiquetado, garantizando la coherencia y el cumplimiento en todos los mercados globales. Agiliza los procesos y mantiene la información del producto precisa y actualizada. Este sistema también facilita el manejo eficiente de los cambios de etiquetado y las actualizaciones reglamentarias.
Structured Product Labeling (SPL) es un formato basado en XML utilizado para el etiquetado de medicamentos que estandariza y organiza la información del producto. Asegura la coherencia y facilita el intercambio de datos entre las agencias reglamentarias y los fabricantes. El SPL permite la gestión eficiente de la información de etiquetado durante todo el ciclo de vida de un producto.
El Número de Localización Global (GLN) es un identificador único utilizado para identificar ubicaciones y entidades dentro de la cadena de suministro. Ayuda a rastrear y gestionar productos farmacéuticos con precisión en los mercados globales. Los GLN garantizan una distribución de productos y una gestión de inventario precisas y eficientes.
El Código Nacional de Medicamentos (NDC) es un identificador único para medicamentos, asignado por la FDA. Ayuda en la identificación precisa de productos farmacéuticos y facilita la gestión y el seguimiento del inventario. El NDC es crucial para una dispensación precisa de medicamentos y para la presentación de informes reglamentarios.
Un Folleto del Investigador (IB) proporciona información detallada sobre los datos clínicos y preclínicos de un fármaco en investigación. Se utiliza para informar a los investigadores de ensayos clínicos sobre la seguridad, eficacia y dosificación del fármaco para fines de estudio. El IB también apoya la toma de decisiones éticas e informadas en la investigación clínica.















