
Idea elektronicznych zgłoszeń regulacyjnych dla produktów farmaceutycznych istniała jeszcze przed samym narzędziem eCTD. Pod koniec lat 80. XX wieku, inicjatywy takie jak CANDA (Wniosek o nowy lek wspomagany komputerowo) były badane przez US FDA (Food and Drug Administration) i agencje europejskie. Te wczesne wysiłki miały na celu zwiększenie efektywności i dostępu do danych dla recenzentów.
Wprowadzenie standardu eCTD (2003):
Międzynarodowa Konferencja Harmonizacyjna (ICH) wprowadziła w 2003 roku przełomowy standard: eCTD (elektroniczny Wspólny Dokument Techniczny). Ten ustandaryzowany format został zaprojektowany w celu ustanowienia uniwersalnego języka dla elektronicznych zgłoszeń na całym świecie.
Pojawienie się narzędzi eCTD:
Wraz z przyjęciem standardu eCTD, wzrosło zapotrzebowanie na specjalistyczne narzędzia eCTD. Narzędzia te przyniosły kilka kluczowych korzyści:
- Usprawnione tworzenie treści: Użytkownicy mogli bez wysiłku tworzyć i porządkować dokumenty zgodnie ze strukturą eCTD.
- Solidna walidacja: Narzędzia eCTD zapewniły zgodność zgłoszeń ze specyfikacjami technicznymi, zapobiegając opóźnieniom spowodowanym błędami formatowania.
- Efektywne zarządzanie cyklem życia: Zarządzanie poprawkami, śledzenie wersji i utrzymywanie zgodności z przepisami staje się łatwiejsze.
Te innowacje zrewolucjonizowały proces składania dokumentacji regulacyjnej, czyniąc go bardziej wydajnym i niezawodnym.
Jak oprogramowanie Freyr Digital automatyzuje tworzenie eCTD
Zaawansowane oprogramowanie Freyr Digital, Freyr SUBMIT PRO, rozwiązuje te wyzwania, automatyzując kluczowe aspekty tworzenia eCTD, co zwiększa wydajność i zmniejsza liczbę błędów ludzkich.
Optymalizacja zasobów: Automatyzując powtarzalne zadania, nasze oprogramowanie uwalnia cenne zasoby ludzkie. Specjaliści mogą skupić się na bardziej strategicznych i wartościowych działaniach, takich jak analiza danych, rozwój strategii regulacyjnych i angażowanie interesariuszy. Ta zmiana nie tylko zwiększa produktywność, ale także obniża koszty operacyjne, zapewniając znaczący zwrot z inwestycji.
Zminimalizowane ryzyko błędu ludzkiego: Automatyzacja minimalizuje ryzyko błędu ludzkiego, zapewniając dokładny transfer danych i prawidłowe formatowanie dokumentów. Wbudowane w oprogramowanie kontrole walidacyjne i mechanizmy wykrywania błędów dodatkowo poprawiają jakość i zgodność zgłoszeń regulacyjnych. Zmniejsza to potrzebę poprawek i pomaga zapewnić terminowe zatwierdzenia.
Narzędzie do śledzenia zgłoszeń dla kompleksowego przeglądu zgłoszeń eCTD
Przyjazny dla użytkownika zautomatyzowany system do planowania i śledzenia złożonych globalnych działań związanych ze zgłoszeniami eCTD, zarządzania przepływem pracy oraz przechowywania i zarządzania wnioskami regulacyjnymi i informacjami o zgłoszeniach jest niezbędny, aby zapewnić, że wnioskodawcy sprostają związanym z tym wyzwaniom na długo przed terminem. Uzyskanie wglądu w operacje zgłaszania i publikowania na szczegółowym poziomie sprawia, że cały proces zgłoszeń jest płynniejszy i szybszy.
Śledzenie zgłoszeń
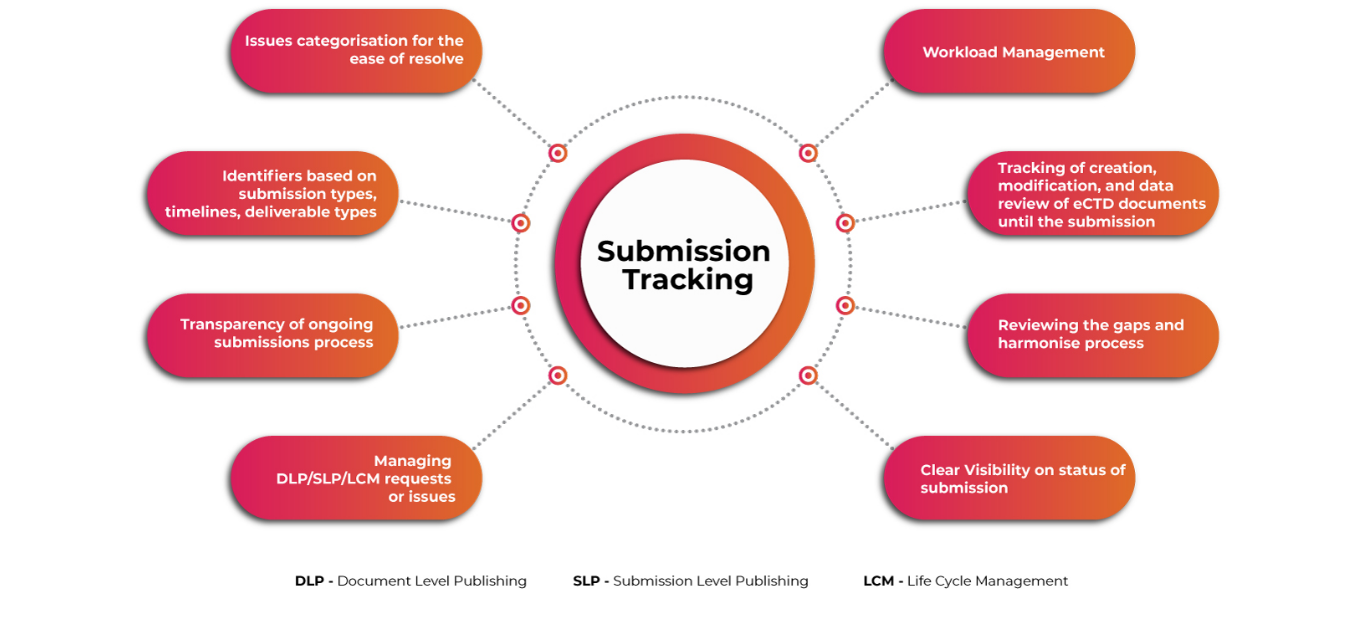
Najnowsza aktualizacja w eCTD
Przejście na eCTD 4.0 zapowiada zwiększoną wydajność i globalną standaryzację w procesie dopuszczania produktów leczniczych do obrotu. Przygotowując się do tej zmiany, Państwa firma może płynnie przez nią przejść i wykorzystać liczne możliwości, jakie oferuje ta nowa era. Chociaż przejście na eCTD 4.0 może wiązać się z wyzwaniami, są one do pokonania dzięki zaangażowaniu i determinacji wszystkich zaangażowanych krajów. Mimo że konieczne będą znaczne inwestycje i wysiłek, istotne korzyści płynące z eCTD 4.0 sprawiają, że przedsięwzięcie jest naprawdę wartościowe.
Przemiana procesu składania wniosków: eCTD 4.0 obiecuje zrewolucjonizować sposób, w jaki firmy farmaceutyczne przesyłają dane dotyczące rozwoju leków do organów ds. zdrowia. Ma na celu usprawnienie procesu składania wniosków.
Harmonogram wdrożenia: FDA planuje przyjmować nowe wnioski w formacie eCTD 4.0 począwszy od 2024 roku. Przyszłe fazy będą dotyczyć istniejących wniosków w wersji 3.2.2 oraz dwukierunkowej komunikacji.
Zgodność z przyszłymi wersjami: eCTD 4.0 obejmuje zgodność z przyszłymi wersjami, umożliwiając ponowne wykorzystanie cyklu życia i dokumentów z wersji 3.2.2. Upraszcza to konwersję aplikacji z wersji 3.2.2 do eCTD 4.0.
Kryteria Walidacji: Dostępne są specyfikacje kryteriów walidacji eCTD 4.0. Kryteria te zapewniają jakość i dokładność zgłoszeń.
Zgodność globalna: Do 2026 roku organy regulacyjne na całym świecie mogą wymagać zgodności ze standardami eCTD 4.0. Chociaż obecnie jest to dobrowolne, egzekwowanie przepisów rozpocznie się między 2026 a 2029 rokiem.
Przyszłość eCTD:
Musisz przyjąć sztuczną inteligencję i sprawić, by Twoja funkcja regulacyjna była dynamiczna, ponieważ dodaje ona wartości Twojej firmie. Freya Fusion to nowoczesna, oparta na sztucznej inteligencji, natywna dla chmury platforma do zarządzania informacjami regulacyjnymi (RIM), która zapewnia wyjątkową wydajność, bezpieczeństwo i skalowalność, jednocześnie utrzymując ścisłą zgodność z GxP. Wzbogacona o zaawansowane funkcje AI/ML i automatyzacji, Freya Fusion wyróżnia się w świecie cyfrowym, oferując doskonałą funkcjonalność i wyjątkowe doświadczenie użytkownika. Postępy w sztucznej inteligencji od Freyr Digital obiecują moduły do tworzenia i śledzenia zgłoszeń, obejmujące funkcje do płynnej kompilacji, publikowania i walidacji zgłoszeń regulacyjnych, gwarantując skrupulatną zgodność z wytycznymi eCTD. Wyprzedzanie konkurencji w dziedzinie zgodności regulacyjnej dzięki SaaS opartemu na sztucznej inteligencji z pewnością przyniesie korzyści Twojej firmie. Niezależnie od tego, czy chodzi o system wczesnego ostrzegania przed zmianami regulacyjnymi, usprawnioną analizę i przegląd dokumentów regulacyjnych, czy analitykę predykcyjną do zarządzania ryzykiem, Freyr Digital zapewnia kompleksowe wsparcie. Skontaktuj się z hello@freyrdigital.com, aby odkryć nasze innowacje oparte na AI/ML, usprawniające operacje regulacyjne w branży medycznej.
Bądź na bieżąco dzięki regularnym aktualizacjom i postępom technologicznym. Współpracuj z nami, aby usprawnić swoje operacje regulacyjne, zwiększyć produktywność i podnieść jakość zgłoszeń. Poproś o demo już dziś i doświadcz idealnego połączenia wiedzy i narzędzi. Przenieś swoją organizację z dobrej na doskonałą. Skontaktuj się z nami już dziś.









