
Dla większości Sprawy regulacyjne przedłużenie rejestracji to nie tylko kolejny etap procedury administracyjnej. To moment, w którym wieloletnie dane dotyczące jakości, dane po wprowadzeniu do obrotu oraz historia zmian poddawane są szczegółowej analizie organów regulacyjnych.
Jednak do kwestii przedłużania umów często podchodzi się w sposób reaktywny.
Pliki są gromadzone w ostatniej chwili. Dane dotyczące PMS są przechowywane w różnych folderach. Certyfikaty są śledzone w arkuszach kalkulacyjnych. I nagle to, co powinno być uporządkowanym procesem, zamienia się w wyścig z czasem.
Przedłużenie ważności wyrobów medycznych nie kończy się niepowodzeniem z powodu braku zaangażowania zespołów. Nie udaje się to, ponieważ planowanie przedłużenia rozpoczyna się zbyt późno, tuż przed upływem terminu ważności.
Skuteczna strategia odnowy zmienia tę sytuację. Traktuje ona odnowę jako ciągły proces w ramach cyklu życia, a nie jako działanie podejmowane w ostatniej chwili.
Przyjrzyjmy się, co to tak naprawdę oznacza dla RA .
Dlaczego przedłużanie ważności wyrobów medycznych wymaga strategii
Większość rejestracji urządzeń obowiązuje przez okres od 3 do 5 lat, w zależności od rynku. W niektórych regionach obowiązują coroczne przedłużenia, podczas gdy w innych stosuje się modele utrzymania ważności oparte na okresowych opłatach. Niezależnie od struktury, po wygaśnięciu licencji urządzenie nie może być legalnie produkowane, importowane ani dystrybuowane.
Wnioski o przedłużenie są obarczone wysokim ryzykiem, ponieważ organy dokonują ponownej oceny:
- Wyniki po wprowadzeniu na rynek
- Tendencje dotyczące skarg i zdarzenia niepożądane
- Zmiany w procesie produkcji i systemie jakości
- Dane kliniczne i dotyczące bezpieczeństwa
- Historia zgodności z przepisami regulacyjnymi
W wielu regionach, w tym w Indiach i UE, organy regulacyjne oczekują przedłożenia skonsolidowanych danych dotyczących systemu monitorowania wydajności (PMS), dokumentacji działań korygujących i zapobiegawczych (CAPA) oraz aktualnej dokumentacji technicznej w ramach przeglądu wniosku o przedłużenie.
Właśnie dlatego proces odświeżania należy traktować jako element procedury operacyjnej, który towarzyszy produktowi przez cały cykl życia.
Nie jako zadanie, które musi być wykonane przed upływem terminu.
Zacznij od kalendarza wydarzeń regulacyjnych – to Twoja pierwsza linia obrony
Jedną z najczęstszych przyczyn niepowodzeń związanych z odnowieniem jest fragmentaryczne śledzenie. Różne rynki. Różne harmonogramy. Różne wymagania.
Scentralizowany kalendarz regulacyjny powinien zawierać:
- Numery certyfikatów i daty ważności według kraju
- Okresy składania wniosków o przedłużenie
- Terminy uiszczania opłat za przedłużenie
- Okres ważności certyfikatu ISO 13485 oznaczenia CE
- Wewnętrzne terminy (12 miesięcy, 6 miesięcy, 3 miesiące przed przedłużeniem)
Z praktycznego punktu RA planowanie należy rozpocząć co najmniej 12 miesięcy przed upływem terminu ważności.
Wiele zespołów korzysta obecnie ze zintegrowanych platform RIMS, aby uzyskać spójny obraz statusu rejestracji na wszystkich rynkach, co pozwala uniknąć uzależnienia od arkuszy kalkulacyjnych, a jednocześnie zapewnia przejrzystość harmonogramów odnowień i umożliwia podejmowanie odpowiednich działań.
freya fusion pierwsze tego rodzaju rozwiązanie, które pozwala organizacjom dysponować jednym wiarygodnym źródłem wszystkich danych dotyczących zgodności z przepisami.
Podstawowe materiały, które zawsze będą Ci potrzebne
Dokumentacja dotycząca przedłużenia rejestracji jest bardzo podobna do dokumentacji wymaganej przy pierwszej rejestracji, jednak kładzie większy nacisk na ciągłość działalności i wyniki.
Większość organów przewiduje, że:
- List motywacyjny, w którym wyraźnie zaznaczono zamiar przedłużenia umowy
- Oświadczenie o utrzymaniu zgodności (produkcja, projekt, własność)
- Zaktualizowany plik główny urządzeń oraz plik główny zakładu (jeśli dotyczy)
- Ważny ISO 13485
- Certyfikaty CE lub certyfikaty zgodności z normami jakości, jeśli są wymagane
- Licencje produkcyjne i dokumentacja potwierdzająca zgodność z GMP
- Deklaracja zgodności
- Historia korespondencji regulacyjnej
Wszelkie zmiany wprowadzone w okresie ważności należy zgłaszać zgodnie z odpowiednimi procedurami obowiązującymi po wydaniu zezwolenia. Nieujawnione zmiany to jeden z najpewniejszych sposobów na wywołanie pytań ze strony organów regulacyjnych.
Właśnie w tym przypadku kluczowe znaczenie ma uporządkowane zarządzanie dokumentami. RA odnoszą korzyści, gdy wszystkie zgłoszenia, poprawki i zatwierdzenia są przechowywane w jednym, kontrolowanym środowisku, a nie rozrzucone po różnych dyskach i skrzynkach odbiorczych.
Nadzór po wprowadzeniu do obrotu stanowi sedno procesu przedłużania ważności
Jeśli istnieje jakaś dziedzina, którą organy regulacyjne powinny dokładnie zbadać w trakcie procesu odnowienia, to jest nią nadzór po wprowadzeniu do obrotu.
Władze oczekują dowodów na to, że urządzenie nadal działa bezpiecznie i skutecznie w rzeczywistych warunkach użytkowania.
Zazwyczaj obejmuje to:
- Dane dotyczące sprzedaży w podziale na rok i wersję urządzenia
- Rejestry skarg i zgłoszenia zdarzeń niepożądanych
- Analiza przyczyn źródłowych każdego problemu
- Rejestry CAPA zawierające dowody zamknięcia
- Historia wycofań (ogólna i dotycząca poszczególnych krajów)
- Analiza trendów w całym okresie ważności
Urządzenia o podwyższonym ryzyku mogą również wymagać:
- Raporty PMS
- Aktualizacje raportu z oceny klinicznej
- PMCF
- Okresowe raporty dotyczące bezpieczeństwa
Skuteczność działań związanych z odnową zależy od tego, jak konsekwentnie dane te są gromadzone na bieżąco, a nie od tego, jak dobrze zostaną one zestawione na końcu.
Wiele RA integruje obecnie monitorowanie PMS bezpośrednio ze swoimi procesami regulacyjnymi za pomocą ujednoliconych platform, takich jak freya fusion, dzięki czemu zgłoszenia, działania korygujące i zapobiegawcze (CAPA) oraz rejestracje pozostają ze sobą powiązane, co ułatwia śledzenie zmian podczas przygotowań do przedłużenia certyfikacji.
Dostosuj swój system jakości do gotowości na odnowę
Twój system zarządzania jakością nie jest czymś odrębnym od procesu odnowy. Stanowi on podstawę tego procesu.
Organy regulacyjne poszukują dowodów w kluczowych obszarach, takich jak:
- Kontrola dokumentów i historia wersji
- Zarządzanie zmianami w zakresie produkcji, etykietowania i pakowania
- Kwalifikacja dostawców i audyty
- Rozpatrywanie skarg i analizowanie trendów
- Skuteczność CAPA
- Audyty wewnętrzne
- Dokumentacja szkoleń i kompetencji
Praktycznym rozwiązaniem jest przeprowadzenie analizy luk przed przedłużeniem umowy na około sześć miesięcy przed złożeniem wniosku:
- Certyfikaty zachowają ważność do czasu przeprowadzenia przeglądu
- Sprawdź, czy dane PMS są kompletne
- Sprawdź zamknięcia w systemie CAPA
- Przejrzyj dzienniki zmian
- Należy zadbać o to, by dokumentacja szkoleniowa była aktualna
Taki proaktywny audyt często pozwala uniknąć konieczności podejmowania działań naprawczych w ostatniej chwili.
Warto wcześnie przygotować się na złożoność związaną z działaniem na wielu rynkach
Odnowienia rzadko mają charakter odosobniony. Globalne portfele obejmują różnych przedstawicieli, dystrybutorów, jednostki notyfikowane i organy.
Koordynacja zazwyczaj obejmuje:
- Producent dostarczający dokumentację techniczną i dane dotyczące systemu zarządzania jakością
- Lokalni agenci zajmujący się rozpatrywaniem wniosków i wydawaniem licencji
- Dystrybutorzy przekazujący dane dotyczące sprzedaży i reklamacji
- Jednostki notyfikowane wydające certyfikaty audytowe
Bez jasnego podziału obowiązków i harmonogramu opóźnienia się mnożą.
Scentralizowany system, który śledzi wymagania poszczególnych jurysdykcji, status składanych wniosków oraz korespondencję regulacyjną, może znacznie ograniczyć utrudnienia. Właśnie w tym zakresie freya fusion RA , skupiając rejestracje, dokumenty i współpracę z interesariuszami w jednym, ujednoliconym środowisku pracy.
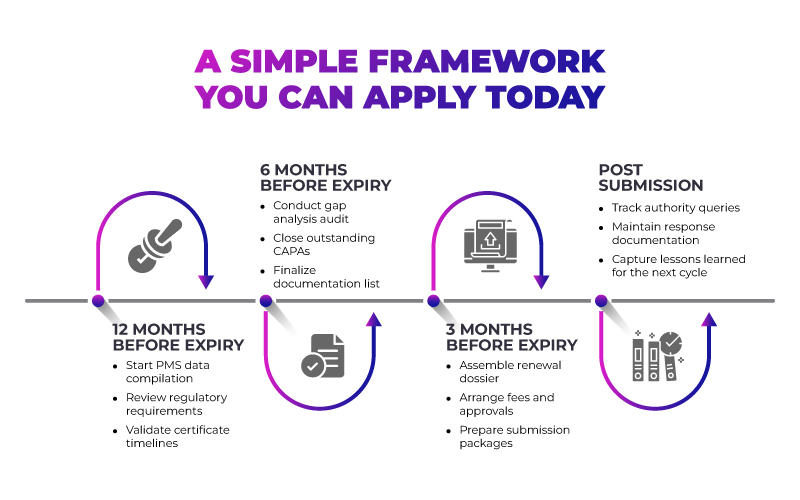
Takie stopniowe podejście sprawia, że odnowa staje się procesem przewidywalnym, a nie powracającym kryzysem.
Odnowa polega na ciągłości, a nie tylko na przestrzeganiu przepisów
Przedłużenie rejestracji wyrobów medycznych ma na celu przede wszystkim zapewnienie nieprzerwanego dostępu do rynku. Strategiczne podejście do tego procesu wzmacnia systemy jakości, poprawia przestrzeganie zasad nadzoru po wprowadzeniu do obrotu oraz buduje zaufanie organów regulacyjnych.
RA już teraz codziennie wykonują ciężką pracę. Wyzwaniem jest nadanie tej pracy odpowiedniej struktury, widoczności i ciągłości.
W tym przypadku platformy takie jak freya fusion . Dzięki ujednoliceniu rejestracji, dokumentów, systemów PMS i współpracy pomagają RA przejść od reaktywnego przedłużania rejestracji do proaktywnego zarządzania cyklem życia produktów regulacyjnych.
Chcesz uprościć proces przedłużania certyfikatów dla swoich wyrobów medycznych?
Jeśli proces odnawiania licencji nadal wydaje się chaotyczny, wymaga ręcznej obsługi lub jest stresujący, być może nadszedł czas, aby przemyśleć strukturę działań związanych z przestrzeganiem przepisów.
Zobacz, jak freya fusion, dzięki swoim funkcjom opartym na sztucznej inteligencji, wspiera RA urządzeń medycznych, zapewniając scentralizowane śledzenie rejestracji, kontrolę dokumentów i wgląd w cykl życia produktu — a wszystko to zaprojektowane z myślą o specjalistach ds. regulacji, a nie zespołach IT.
Umów się na prezentację już dziś i zrób pierwszy krok w kierunku odzyskania pewności siebie, stałej zgodności z przepisami oraz płynniejszego funkcjonowania na rynku.









