Garantizar el cumplimiento riguroso de Dispositivos Médicos y el registro de Dispositivos Médicos del Reino Unido
Los fabricantes extranjeros deben cumplir con el Reglamento sobre productos sanitarios del Reino Unido de 2002 (en su versión modificada). Todos los productos sanitarios y los productos para diagnóstico in vitro deben registrarse ante la MHRA su comercialización en el Reino Unido. Los fabricantes no británicos están obligados a designar a una persona responsable en el Reino Unido (UKRP) que los represente. La MHRA requisitos estrictos en materia de documentación, etiquetado y notificación de casos de vigilancia para garantizar la seguridad de los pacientes y la trazabilidad de los productos.
Orientarse entre los nuevos requisitos propuestos en el resultado de la consulta para el Reino Unido puede resultar complejo en lo que respecta al marcado UKCA, los requisitos en materia de datos y las expectativas posteriores a la comercialización. Muchas empresas se enfrentan a dificultades debido a expedientes técnicos incompletos, clasificaciones de productos divergentes y un conocimiento limitado del Sistema de Registro Electrónico de Productos Sanitarios (DORS). Las actualizaciones normativas y la evolución MHRA complican aún más la planificación y la asignación de recursos.
Freyr simplifica cada paso del proceso de entrada en el mercado británico. Nos encargamos de presentar las solicitudes al DORS, actuamos como su UKRP, garantizamos que la documentación esté lista y subsanamos las deficiencias de cumplimiento normativo durante la transición del marcado CE al UKCA. Nuestros expertos en normativa le orientan sobre los cambios MHRA , ayudándole a lograr un acceso al mercado que cumpla con la normativa, sea oportuno y resulte rentable.
Proceso paso a paso para Dispositivos Médicos en el Reino Unido
El registro de Dispositivos Médicos el Reino Unido conlleva varias etapas bien definidas. A continuación te explicamos cómo Freyr gestiona todo el proceso por ti:
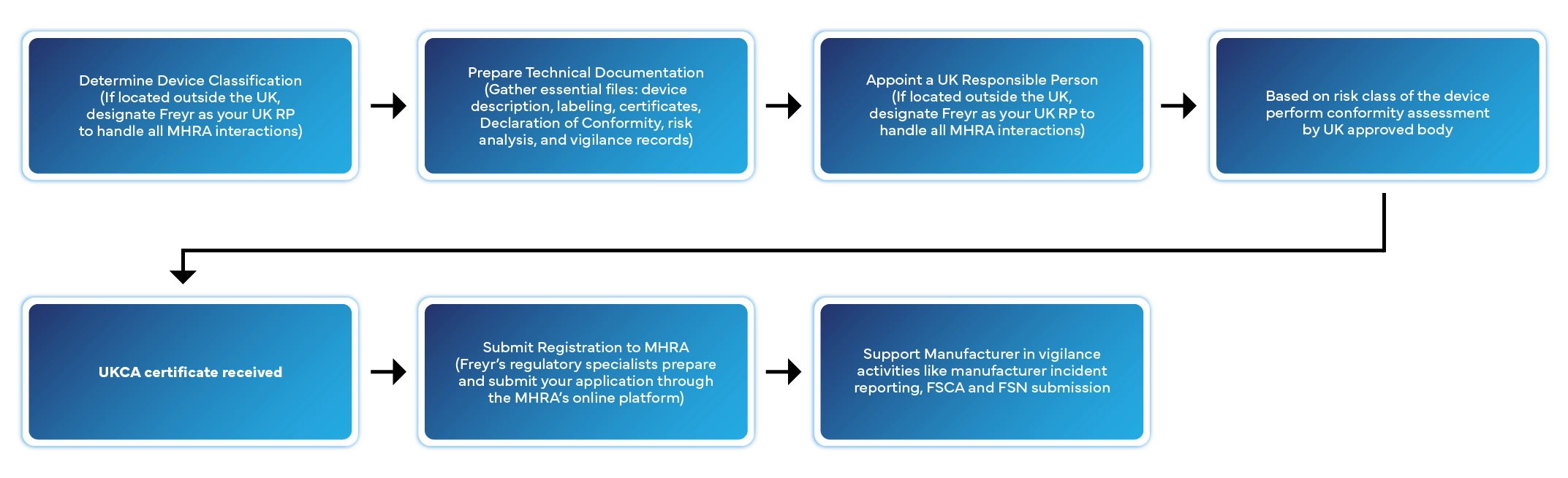
Plazo de tramitación habitual: entre 2 y 6 semanas, dependiendo de la clase del dispositivo y de que la documentación esté completa.
Freyr Dispositivos Médicos : principales productos y servicios
Registro de productos sanitarios: Freyr gestiona MHRA completo MHRA a través de la plataforma DORS, garantizando que las solicitudes cumplan con la normativa, que los datos sean precisos y que las aprobaciones se obtengan a tiempo para todas las categorías de productos sanitarios.
Persona responsable en el Reino Unido: en su calidad de UKRP designada, Freyr actúa en su nombre ante la MHRA, se encarga de todas las comunicaciones y garantiza el cumplimiento normativo y la vigilancia continuos.
TF / Recopilación de expedientes: Freyr recopila expedientes técnicos y documentación que cumplen los requisitos normativos del Reino Unido para el marcado UKCA, garantizando la preparación para auditorías, inspecciones y presentaciones.
Asistencia en sistemas de gestión de la calidad: le ayudamos a implementar y mantener sistemas de gestión de la calidad ISO 13485 y adaptados a MHRA del Reglamento sobre productos sanitarios (MDR) del Reino Unido y de la Agencia Reguladora de Medicamentos y Productos Sanitarios ( MHRA .
Asistencia en la redacción de documentos reglamentarios: Freyr ofrece servicios especializados de elaboración de informes de seguridad (CER), planes de seguimiento poscomercialización (PMS), informes periódicos de seguridad (PSUR) y documentación sobre gestión de riesgos, garantizando la claridad técnica y la precisión normativa.
Etiquetado y cumplimiento normativo: nuestro equipo se asegura de que el etiquetado, las instrucciones de uso y el embalaje cumplan los requisitos de etiquetado y lingüísticos de la marca UKCA, garantizando la coherencia y el cumplimiento normativo.
Vigilancia poscomercialización: Freyr presta apoyo en las actividades de vigilancia poscomercialización, lo que incluye la notificación de reacciones adversas, la presentación de informes de vigilancia y MHRA , con el fin de mantener el acceso al mercado.
Oferta de servicios de Freyr UK Responsible Person (UKRP)
Freyr actúa como su UKRP autorizado en el Reino Unido ( UKRP), garantizando el pleno cumplimiento del Reglamento sobre productos sanitarios del Reino Unido de 2002 MHRA. Representamos a su empresa a nivel local en el Reino Unido y nos encargamos de toda la comunicación con la MHRA.
- Registro de productos sanitarios ante MHRA
Freyr actúa como su persona responsable designada en el Reino Unido (UKRP) para gestionar todo el proceso MHRA a través de la plataforma DORS, garantizando que cada producto se incluya, verifique y sea apto para su venta en el Reino Unido. - Documentación y garantía de conformidad
Nuestros expertos en materia de normativa se aseguran de que su declaración de conformidad, la documentación técnica y las certificaciones de los productos estén disponibles, y conservan una copia para poder facilitarla a MHRA cuando esta lo solicite. - Respuesta a MHRA
Freyr se encarga directamente de todas las comunicaciones y aclaraciones con la MHRA su nombre, garantizando respuestas puntuales y precisas a las consultas reglamentarias o a las revisiones posteriores a la comercialización. - Vigilancia y comunicación de incidentes
En su calidad de UKRP, Freyr actúa como principal punto de contacto para cuestiones relacionadas con la seguridad. Nos encargamos de la coordinación entre fabricantes, profesionales sanitarios, pacientes y la MHRA acontecimientos adversos, garantizando su correcta notificación y la adopción de medidas correctivas. - Preparación para inspecciones y auditorías
Freyr conserva toda la documentación y la correspondencia necesarias para MHRA y auditorías MHRA . Nuestro equipo se asegura de que los expedientes técnicos, el etiquetado y los registros posteriores a la comercialización estén fácilmente disponibles.
Programe una reunión con nuestros expertos hoy mismo.
¿Por qué asociarse con Freyr?
- Experiencia End-to-end que abarca desde el registro previo a la comercialización hasta la vigilancia poscomercialización, gestionando todas las fases del cumplimiento normativo.
- Una trayectoria contrastada con más de 1500 registros de dispositivos completados con éxito en diversas categorías.
- Presencia local en el Reino Unido con especialistas en normativa sobre el terreno en Reading, con el respaldo de equipos de prestación de servicios a nivel mundial.
- Una planificación de la transición a medida que ofrece apoyo estratégico para pasar de la certificación CE a la UKCA de forma fluida y rentable.
- Una comunicación transparente mediante el contacto directo con MHRA el envío proactivo de información actualizada sobre el cumplimiento normativo a los clientes.
- Contamos con la confianza de marcas internacionales, y Freyr colabora con más de 470 fabricantes de todo el mundo como su socio en materia de normativa.
Preguntas Frecuentes (PF)
01. ¿En qué consiste el proceso Dispositivos Médicos en el Reino Unido?
El proceso Dispositivos Médicos en el Reino Unido consiste en notificar a MHRA Agencia Reguladora de Medicamentos y Productos Sanitarios) los datos de su dispositivo antes de su comercialización en Gran Bretaña. Los fabricantes deben facilitar los datos de la empresa, la clasificación del dispositivo y la documentación técnica. Los fabricantes no británicos también deben designar a una persona responsable en el Reino Unido (UK RP) para que se encargue del registro y de las comunicaciones relativas al cumplimiento normativo.
02. ¿Quién debe designar a un responsable en el Reino Unido (UK RP)?
Todo fabricante con sede fuera del Reino Unido debe designar a una persona responsable en el Reino Unido antes de comercializar productos sanitarios en dicho país. La persona responsable en el Reino Unido actúa como contacto regulatorio del fabricante, garantizando que toda la documentación técnica, las declaraciones y MHRA se gestionen adecuadamente. Los fabricantes con sede en el Reino Unido pueden interactuar directamente con la MHRA una persona responsable en el Reino Unido.
03. ¿Qué documentación se necesita para MHRA ?
La MHRA una documentación esencial, que incluye la declaración de conformidad, la descripción y clasificación del producto, los datos del fabricante y la información sobre el etiquetado. En el caso de los productos de mayor riesgo, también pueden revisarse los expedientes técnicos y la evidencia clínica. Contar con una documentación completa y preparada para una auditoría garantiza unas aprobaciones más rápidas y unas inspecciones posteriores a la comercialización más fluidas por parte de la MHRA los representantes autorizados.
04. ¿Cuánto tiempo dura el proceso MHRA ?
Por lo general, MHRA tarda entre 2 y 6 semanas, dependiendo de la clase del producto, de si la documentación está completa y de si interviene un responsable en el Reino Unido. Los productos sencillos de clase I pueden tramitarse más rápidamente, mientras que los productos complejos o de mayor riesgo pueden tardar más tiempo debido a la validación adicional de los datos y a las revisiones de la documentación técnica.
05. ¿Cuál es la diferencia entre el marcado CE y el marcado UKCA?
El marcado CE acredita el cumplimiento de la normativa de la Unión Europea, mientras que el marcado UKCA (UK Conformity Assessed) se aplica a los productos comercializados en Gran Bretaña. Desde el Brexit, el marcado UKCA ha sustituido al CE en el mercado británico, aunque el marcado CE sigue siendo aceptado de forma temporal. Irlanda del Norte sigue reconociendo los marcados CE y CE UKNI en virtud de las normas de armonización de la UE.
06. ¿Cuáles son las responsabilidades posteriores a la comercialización tras el registro?
Tras el registro, los fabricantes y los responsables en el Reino Unido deben llevar a cabo la vigilancia poscomercialización, notificar los incidentes adversos, informar a MHRA cualquier cambio MHRA el producto o MHRA el etiquetado y renovar los registros cuando sea necesario. Asimismo, deben conservar la documentación técnica durante al menos 10 años. Estas actividades garantizan el cumplimiento continuo de la normativa y protegen la salud de los pacientes a lo largo de todo el ciclo de vida del producto sanitario.
07. ¿Con qué frecuencia debe actualizarse la información MHRA ?
La información de registro debe actualizarse sin demora siempre que se produzca un cambio en la clasificación del producto, el etiquetado, el centro de fabricación o la entidad responsable. La MHRA la persona responsable en el Reino Unido o el fabricante realicen actualizaciones inmediatas para mantener registros de mercado precisos. Las auditorías internas periódicas ayudan a garantizar que sus datos se mantengan actualizados y cumplan con la normativa en constante evolución.
08. ¿Cuáles son las sanciones por incumplir MHRA de MHRA ?
El incumplimiento de los requisitos Dispositivos Médicos o de poscomercialización Dispositivos Médicos en el Reino Unido puede dar lugar a advertencias reglamentarias, la retirada del producto, multas o acciones judiciales. La MHRA tiene competencia para suspender o revocar la autorización de comercialización. Un cumplimiento proactivo y el nombramiento de una persona responsable cualificada en el Reino Unido ayudan a los fabricantes a evitar sanciones y a mantener la continuidad comercial.
09. ¿Cómo simplifica Freyr Dispositivos Médicos en el Reino Unido?
Freyr ofrece end-to-end , desde actuar como su persona responsable en el Reino Unido (UKRP) hasta gestionar MHRA , la documentación técnica y el cumplimiento normativo continuo. Nuestros consultores experimentados agilizan el proceso, reducen los plazos de aprobación y ayudan a garantizar un acceso continuo al mercado.













