Registrazione dei Dispositivi Medici negli EAU – Panoramica
Gli Emirati Arabi Uniti (EAU), una nazione membro di spicco del GCC, vantano un sistema sanitario avanzato. Il suo potenziale di mercato è comprovato e in costante crescita, regolato dal Dipartimento per il Controllo dei Farmaci del Ministero della Salute e della Prevenzione (MOHAP). La governance centralizzata e le barriere linguistiche sono i principali ostacoli alla registrazione dei dispositivi medici negli EAU, insieme alle complessità linguistiche e alla mancanza di canali di comunicazione efficienti con le Autorità Sanitarie.
Autorità Regolatoria: Dipartimento per il Controllo dei Farmaci del Ministero della Salute e della Prevenzione (MOHAP)
Regolamentazione: Linea guida per la registrazione dei dispositivi medici negli EAU
Percorso regolatorio: Registrazione del Prodotto
Rappresentante autorizzato: È richiesto un Rappresentante autorizzato locale negli EAU
Requisito QMS: ISO 13485:2016
Valutazione dei dati tecnici: Comitato per la Registrazione dei Dispositivi Medici
Validità della Licenza: 5 anni
Requisiti di etichettatura: Allegato 2 (2.5) della Linea guida per la registrazione dei dispositivi medici negli EAU
Formato di sottomissione: Cartaceo
Lingua: Inglese
Classificazione dei dispositivi medici negli EAU
Gli EAU hanno regole di classificazione separate per i dispositivi medici e gli IVD. Le regole di classificazione dei dispositivi medici degli EAU sono in linea con le regole di classificazione delle Direttive sui dispositivi medici dell'UE. Le classi di dispositivi secondo le regole di classificazione degli EAU sono le seguenti
| Criteri di Rischio | Classe di Dispositivo Medico |
|---|---|
| Basso Rischio | I |
| Rischio Basso Moderato | IIa |
| Rischio moderato – alto | IIb |
| Rischio Elevato | III |
| Criteri di Rischio | Classe IVD |
|---|---|
| Basso rischio individuale e basso rischio per la salute pubblica | A |
Rischio individuale moderato e/o Basso rischio per la salute pubblica | B |
Rischio individuale elevato e/o Rischio moderato per la salute pubblica | C |
| Rischio individuale elevato e rischio per la salute pubblica elevato | D |
Rappresentante Locale Autorizzato negli EAU
I produttori esteri, senza un ufficio fisico, devono nominare un Rappresentante Locale (LR) che agisca per loro conto. Il rappresentante locale dovrebbe essere autorizzato dal Ministero della Salute come negozio medico o ufficio scientifico (nel caso di ufficio scientifico, le attività di importazione e distribuzione dovrebbero essere eseguite da un Negozio Medico Autorizzato designato). I richiedenti possono nominare il loro distributore come Rappresentante Locale. Tuttavia, avere un Rappresentante Locale indipendente, senza interessi commerciali, fornirebbe la flessibilità necessaria per nominare più distributori negli Emirati Arabi Uniti. I dettagli sia del LR che del distributore devono essere forniti durante la registrazione del dispositivo.
Processo di classificazione ufficiale con il MoHAP degli EAU.
Il MoHAP degli Emirati Arabi Uniti ha introdotto un servizio ufficiale di classificazione, particolarmente utile quando non si è sicuri se il proprio prodotto richieda la registrazione. Questo servizio classifica prodotti di tutti i tipi e forme in base alla loro presentazione, composizione, uso e design. I requisiti possono variare a seconda della natura del prodotto, della classe di rischio e dello stato normativo.
La lettera di classificazione indica se un prodotto deve essere registrato presso il MOHAP. Se la registrazione è richiesta, il prodotto deve essere registrato secondo la classe identificata nella lettera di classificazione. Questa lettera è valida per tre anni dalla data di emissione.
I risultati ufficiali della classificazione possono essere:
- Non richiede la registrazione MOHAP
- Approvato dal MOHAP degli EAU come dispositivo medico, limitato all'uso professionale
- Approvato dal MOHAP degli EAU come dispositivo medico da banco
Registrazione dei Dispositivi Medici negli EAU
Alcuni dispositivi non richiedono la registrazione del prodotto, la pre-registrazione o l'approvazione per l'importazione. Tali prodotti esentati dalla registrazione o dall'elencazione devono richiedere e ottenere un permesso di importazione per essere commercializzati negli EAU.
Per altri dispositivi, le importazioni non saranno sdoganate a meno che non venga rilasciata una pre-approvazione per l'importazione della spedizione da parte del DRCD. Tali dispositivi dovranno essere elencati o registrati per l'importazione negli EAU.
Elenco dei Dispositivi: Generalmente, i prodotti utilizzati negli ospedali sotto supervisione professionale e i dispositivi di Classe I non sono soggetti a valutazione dettagliata e devono essere elencati. Un Certificato di Elenco sarà rilasciato dall'agenzia. I dispositivi, dopo l'inserimento nell'elenco, dovranno ottenere un permesso di importazione per commercializzarli negli EAU.
Registrazione dei Dispositivi: L'attività di registrazione include la Registrazione del Sito e del Prodotto.
- Registrazione del Sito:Il sito di produzione deve essere registrato se il dispositivo fabbricato in tale Sito viene importato negli EAU per la prima volta. Per i dispositivi successivi fabbricati nello stesso sito, sarà sufficiente la sola registrazione del dispositivo e la registrazione del sito non sarà richiesta.
- Registrazione del dispositivo: Questi dispositivi sono soggetti a revisione da parte del comitato tecnico che, previa approvazione, rilascerà un certificato di licenza.
Flusso del processo
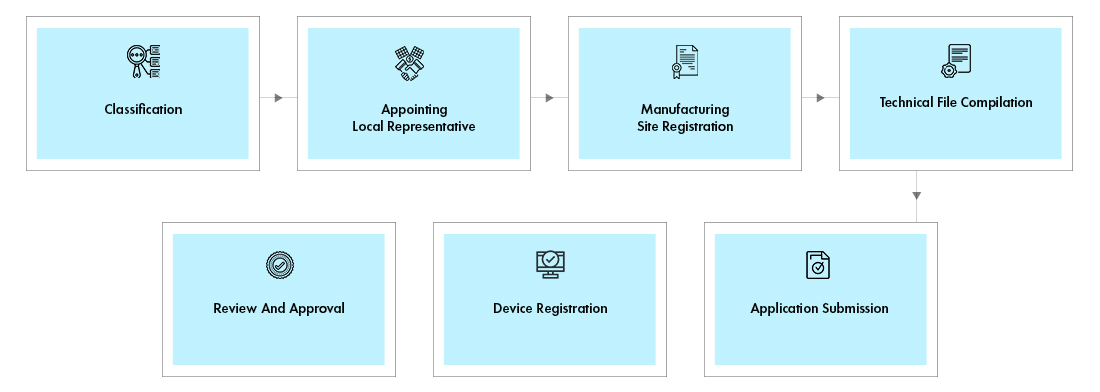
Gestione del ciclo di vita del dispositivo post-approvazione
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici come l'aggiunta di nuove varianti, accessori; l'aggiunta di nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e della registrazione attraverso il pagamento tempestivo delle tasse amministrative e di registrazione
- Rinnovo delle licenze
- Collegamento tra il MoH e il fabbricante
- Gestione dell'Importazione
Con un centro di consegna esclusivo a Dubai, Freyr detiene una posizione autorevole nel mercato dei dispositivi medici degli EAU e delinea la classificazione dei dispositivi, oltre a decodificare le normative guida per una migliore conformità. Supportiamo i clienti nella compilazione dei documenti secondo gli standard, garantendo così approvazioni rapide. Freyr offre una gamma completa di servizi normativi relativi alla commercializzazione di successo dei dispositivi.
Riepilogo
| Tipo di Dispositivo | Registrazione del dispositivo | Registrazione dei dispositivi | Licenza di importazione |
|---|---|---|---|
Dispositivo esente da approvazione pre-importazione (Come elencato nell'Allegato 3) | Nord America | Nord America | SÌ |
| SÌ | Nord America | SÌ |
| Tutti gli altri dispositivi | Nord America | SÌ | SÌ |
Freyr Competenza
- Intelligence normativa
- Due Diligence Regolatoria
- Classificazione Formale dei Dispositivi Medici
- Registrazione dei dispositivi
- Rappresentanza autorizzata negli EAU
- Supporto per la traduzione
- Supporto all'etichettatura
- Identificazione e qualificazione del distributore
- Gestione delle modifiche post-approvazione
- Rinnovo e trasferimento della licenza
- Sdoganamento