Garantire la piena conformità alle normative e alle procedure di registrazione dei dispositivi medici nel Regno Unito
produttori stranieri produttori conformarsi al Regolamento britannico sui dispositivi medici del 2002 (e successive modifiche). Tutti i dispositivi medici e i dispositivi per la diagnosi in vitro devono essere registrati presso MHRA della loro commercializzazione nel Regno Unito. produttori non britannici produttori tenuti a nominare un responsabile nel Regno Unito (UKRP) che li rappresenti. MHRA requisiti rigorosi in materia di documentazione, etichettatura e segnalazione dei casi di vigilanza per garantire la sicurezza dei pazienti e la tracciabilità dei prodotti.
Orientarsi tra i nuovi requisiti proposti nell'esito della consultazione per il Regno Unito può risultare complesso, soprattutto per quanto riguarda il marchio UKCA, i requisiti relativi ai dati e le aspettative post-commercializzazione. Molte aziende si trovano ad affrontare difficoltà legate a fascicoli tecnici incompleti, classificazioni dei dispositivi discordanti e una conoscenza limitata del Sistema di registrazione online dei dispositivi (DORS). Gli aggiornamenti normativi e l'evoluzione MHRA complicano ulteriormente la pianificazione e l'allocazione delle risorse.
Freyr semplifica ogni fase dell'ingresso nel mercato britannico. Ci occupiamo delle richieste DORS, fungiamo da UKRP, garantiamo la correttezza della documentazione e colmiamo le lacune normative durante la transizione dal marchio CE al marchio UKCA. I nostri esperti in materia normativa vi guidano attraverso MHRA mutevoli MHRA , aiutandovi a ottenere un accesso al mercato conforme, tempestivo ed economico.
Procedura dettagliata per la registrazione dei dispositivi medici nel Regno Unito
La registrazione di un dispositivo medico nel Regno Unito prevede diverse fasi ben definite. Ecco come Freyr gestisce l'intero processo per te:
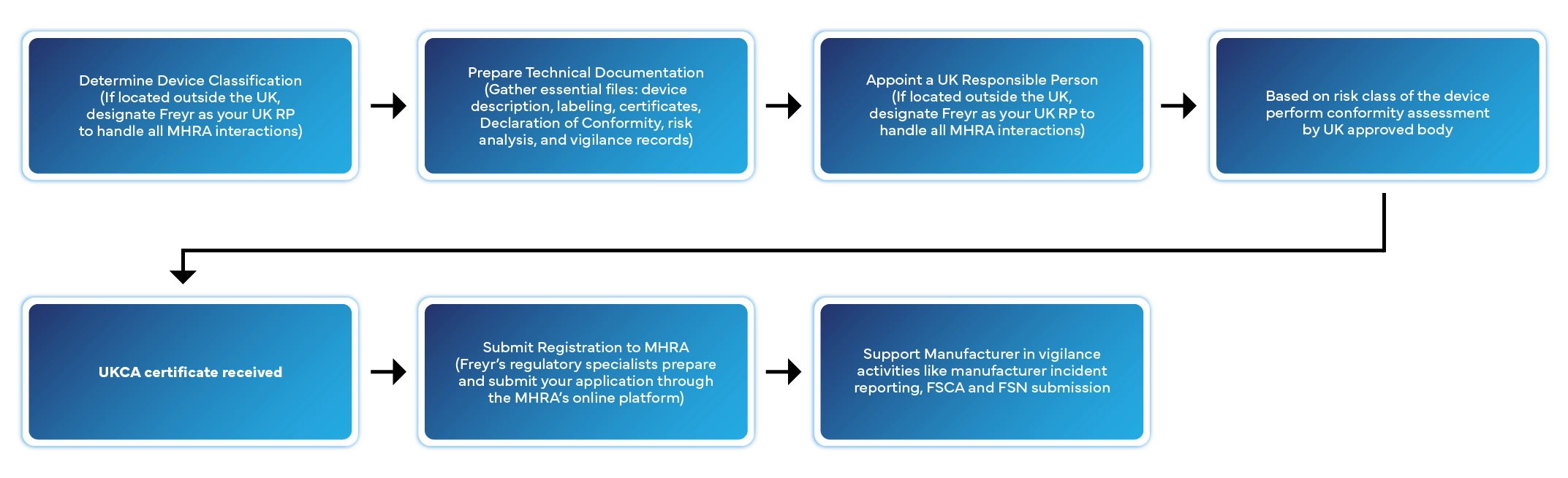
Tempi di elaborazione standard: 2–6 settimane, a seconda della classe del dispositivo e della completezza della documentazione.
Principali offerte di Freyr Medical Device UK
Registrazione dei dispositivi Freyr gestisce l'intero MHRA tramite la piattaforma DORS, garantendo la conformità delle richieste, l'accuratezza dei dati e l'approvazione tempestiva per tutte le categorie di dispositivi.
Responsabile nel Regno Unito In qualità di UKRP designato, Freyr agisce in vostra rappresentanza presso MHRA, gestisce tutte le comunicazioni e garantisce il monitoraggio continuo della conformità e della vigilanza.
TF / Redazione di dossier: Freyr redige schede tecniche e dossier conformi ai requisiti normativi del Regno Unito per il marchio UKCA, garantendo la piena preparazione in vista di audit, ispezioni e presentazioni.
Supporto per i sistemi di gestione della qualità Forniamo assistenza nell'implementazione e nella gestione di sistemi di gestione della qualità ISO 13485, in linea con MHRA del MDR britannico e MHRA .
Supporto alla redazione di documenti normativi Freyr offre un servizio di redazione professionale di CER, piani di monitoraggio post-commercializzazione (PMS), PSUR e documentazione sulla gestione dei rischi, garantendo chiarezza tecnica e accuratezza normativa.
Etichettatura e conformità Il nostro team garantisce che le vostre etichette, le istruzioni per l'uso e il packaging soddisfino i requisiti di etichettatura e linguistici UKCA, assicurando coerenza e conformità.
Sorveglianza post-commercializzazione Freyr supporta le attività di sorveglianza post-commercializzazione, tra cui la segnalazione di eventi avversi, la presentazione di rapporti di vigilanza e MHRA , al fine di garantire il mantenimento dell'accesso al mercato.
Offerta di servizi del Responsabile Freyr per il Regno Unito (UKRP)
Freyr funge da vostro UKRP autorizzato UKRP, garantendo la piena conformità al Regolamento britannico sui dispositivi medici del 2002 MHRA. Rappresentiamo la vostra azienda a livello locale nel Regno Unito e gestiamo tutte le comunicazioni con MHRA.
- Registrazione dei dispositivi presso MHRA
Freyr agisce in qualità di vostro Responsabile designato nel Regno Unito (UKRP) per gestire l'intero processo MHRA tramite la piattaforma DORS, garantendo che ogni dispositivo sia correttamente registrato, verificato e idoneo alla vendita nel Regno Unito. - Documentazione e garanzia di conformità
I nostri esperti in materia normativa si assicurano che la vostra dichiarazione di conformità, la documentazione tecnica e le certificazioni dei prodotti siano disponibili e ne conservano una copia per poterla fornire MHRA su richiesta. - Risposta alle MHRA
Freyr gestisce direttamente, MHRA vostro conto, tutte le comunicazioni e i chiarimenti con MHRA , garantendo risposte tempestive e accurate alle richieste normative o alle revisioni post-commercializzazione. - Vigilanza e comunicazione degli incidenti
In qualità di UKRP, Freyr funge da referente principale per le questioni relative alla sicurezza. Ci occupiamo del coordinamento tra produttori, operatori sanitari, pazienti e MHRA eventi avversi, garantendo una corretta segnalazione e l'adozione di misure correttive. - Preparazione alle ispezioni e agli audit
Freyr conserva tutta la documentazione e la corrispondenza necessarie per MHRA e gli audit MHRA . Il nostro team garantisce che i fascicoli tecnici, l'etichettatura e la documentazione post-commercializzazione siano prontamente disponibili.
Prenota un incontro con i nostri esperti oggi stesso
Perché collaborare con Freyr?
- Competenza End-to-end , che spazia dalla registrazione pre-commercializzazione alla sorveglianza post-commercializzazione, gestendo ogni fase del processo di conformità.
- Una comprovata esperienza con oltre 1500 registrazioni di dispositivi completate con successo in diverse categorie.
- Presenza locale nel Regno Unito con esperti in materia normativa sul posto a Reading, supportati da team operativi a livello globale.
- Una pianificazione personalizzata della transizione che offre un supporto strategico per passare dalla certificazione CE alla certificazione UKCA in modo agevole ed economico.
- Comunicazione trasparente grazie al contatto diretto con MHRA aggiornamenti proattivi in materia di conformità forniti ai clienti.
- Scelta da marchi internazionali, Freyr è partner normativo di oltre 470 produttori .
Domande frequenti (FAQ)
01. In cosa consiste la procedura di registrazione dei dispositivi medici nel Regno Unito?
La procedura di registrazione dei dispositivi medici nel Regno Unito prevede la notifica del dispositivo alla MHRA Medicines and Healthcare products Regulatory Agency) prima della sua immissione sul mercato in Gran Bretagna. produttori fornire i dati aziendali, la classificazione del dispositivo e la documentazione tecnica. produttori non residenti nel Regno Unito produttori inoltre nominare un responsabile nel Regno Unito (UK RP) incaricato di gestire la registrazione e le comunicazioni relative alla conformità.
02. Chi deve nominare un responsabile nel Regno Unito (UK RP)?
Qualsiasi fabbricante con sede al di fuori del Regno Unito deve nominare un responsabile nel Regno Unito prima di immettere i dispositivi sul mercato britannico. Il responsabile nel Regno Unito funge da referente normativo del fabbricante, garantendo che tutta la documentazione tecnica, le dichiarazioni e MHRA siano gestite correttamente. produttori con sede nel Regno Unito produttori interagire direttamente con MHRA un responsabile nel Regno Unito.
03. Quali documenti sono necessari per MHRA ?
MHRA una documentazione essenziale, tra cui la dichiarazione di conformità, la descrizione e la classificazione del dispositivo, i dati del fabbricante e le informazioni relative all'etichettatura. Per i dispositivi a rischio più elevato, possono essere esaminati anche i fascicoli tecnici e le prove cliniche. Disporre di una documentazione completa e pronta per le verifiche garantisce approvazioni più rapide e ispezioni post-commercializzazione più agevoli da parte MHRA dei rappresentanti autorizzati.
04. Quanto tempo richiede la procedura MHRA ?
In genere, MHRA richiede da 2 a 6 settimane, a seconda della classe del dispositivo, della completezza della documentazione e dell'eventuale coinvolgimento di un responsabile nel Regno Unito. I dispositivi semplici di Classe I possono essere trattati più rapidamente, mentre i prodotti complessi o a rischio più elevato potrebbero richiedere più tempo a causa della necessità di ulteriori verifiche dei dati e revisioni della documentazione tecnica.
05. Qual è la differenza tra il marchio CE e il marchio UKCA?
Il marchio CE attesta la conformità alle normative dell'Unione Europea, mentre il marchio UKCA (UK Conformity Assessed) si applica ai dispositivi commercializzati in Gran Bretagna. A seguito della Brexit, il marchio UKCA ha sostituito il marchio CE per il mercato britannico, sebbene quest'ultimo continui ad essere accettato in via temporanea. L'Irlanda del Nord continua a riconoscere i marchi CE e CE UKNI in base alle norme di allineamento dell'UE.
06. Quali sono le responsabilità post-commercializzazione dopo la registrazione?
Dopo la registrazione, produttori i responsabili nel Regno Unito devono svolgere attività di sorveglianza post-commercializzazione, segnalare gli incidenti indesiderati, informare MHRA eventuali modifiche al prodotto o all’etichettatura e rinnovare le registrazioni secondo necessità. Devono inoltre conservare la documentazione tecnica per almeno 10 anni. Queste attività garantiscono la conformità continua e tutelano la salute dei pazienti per tutto il ciclo di vita del dispositivo.
07. Con quale frequenza devono essere aggiornate le informazioni MHRA ?
Le informazioni relative alla registrazione devono essere aggiornate tempestivamente ogni volta che si verificano modifiche alla classificazione del dispositivo, all'etichettatura, al sito di produzione o al soggetto responsabile. MHRA aggiornamenti immediati da parte del soggetto responsabile nel Regno Unito o del fabbricante, al fine di garantire l'accuratezza dei dati di mercato. L'esecuzione di regolari audit interni contribuisce a garantire che i dati rimangano aggiornati e conformi alle normative in continua evoluzione.
08. Quali sono le sanzioni previste in caso di mancato rispetto delle MHRA ?
Il mancato rispetto degli obblighi di registrazione dei dispositivi medici nel Regno Unito o dei requisiti post-commercializzazione può comportare avvertimenti da parte delle autorità di regolamentazione, il ritiro del prodotto dal mercato, sanzioni pecuniarie o azioni legali. MHRA ha MHRA la facoltà di sospendere o revocare l'autorizzazione all'immissione in commercio. Una conformità proattiva e la nomina di un responsabile qualificato nel Regno Unito aiutano produttori sanzioni e a garantire la continuità della commercializzazione.
09. In che modo Freyr semplifica la registrazione dei dispositivi medici nel Regno Unito?
Freyr offre end-to-end , dal ruolo di Responsabile nel Regno Unito (UKRP) alla gestione MHRA , della documentazione tecnica e della conformità continua. I nostri consulenti esperti semplificano il processo, riducono i tempi di approvazione e contribuiscono a garantire un accesso continuo al mercato.













