Servizi di etichettatura clinica - Panoramica
Durante lo sviluppo di un farmaco, le aziende utilizzano una serie di strumenti relativi all'etichettatura clinica che si avvalgono dell'etichettatura mirata per facilitare tale processo. Questi strumenti allineano contemporaneamente gli obiettivi desiderati in materia di etichettatura commerciale e di sperimentazione clinica con lo sviluppo della struttura del programma o del disegno dello studio e facilitano la stesura della panoramica clinica (CO). Alcuni degli strumenti di etichettatura clinica che utilizzano l'etichettatura mirata durante lo sviluppo di un farmaco sono:
- Brochure per lo sperimentatore (IB)
- Etichettatura Target (TL)/Profilo Target
- Scheda Dati Core di Sviluppo (DCDS).
- Sviluppo delle Informazioni di Sicurezza Core (DCSI).
- Profilo del Prodotto Target (TPP) della FDA
È importante per le aziende adottare un approccio modulare nella raccolta delle informazioni sulla sicurezza e l'efficacia attraverso diversi tipi di etichette cliniche per integrare i requisiti di etichettatura clinica. Ciò soddisferebbe la necessità di aiutare efficacemente investigatori e sponsor presentando e aggiornando una sezione DCSI focalizzata e dedicata che può essere comodamente inserita in diverse categorie cliniche.
Inoltre, il DCSI è incluso nelle Informazioni Fondamentali di Sicurezza dell'Azienda (CCSI), che costituisce la base per il primo Foglio Dati Fondamentale dell'Azienda (CCDS) ed è utilizzato per l'immissione in commercio del prodotto. È inoltre richiesta la stesura di un CO dettagliato che comprenda l'ambito e le questioni critiche nel programma di sviluppo clinico del farmaco, a supporto della documentazione per i valutatori.
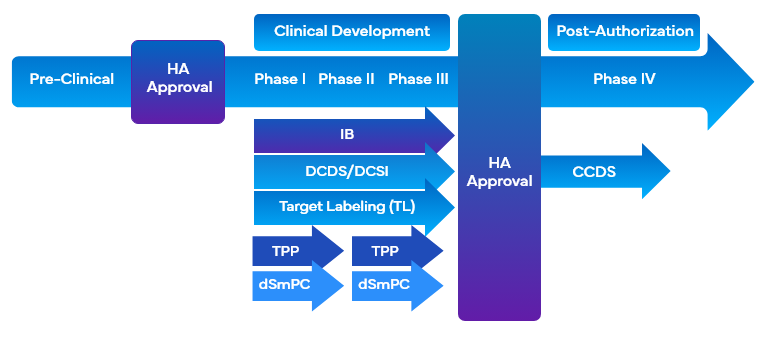
I Servizi di Etichettatura Clinica di Freyr
Servizi di etichettatura clinica
Creazione e revisione della Brochure per lo Sperimentatore (IB)
Freyr vanta una notevole esperienza nella creazione, redazione e revisione dei protocolli di studio (IB) per vari programmi in fase clinica dei nostri clienti. Gli IB sono le forme più preliminari di etichette volte a fornire allo sperimentatore o al medico curante informazioni rilevanti relative al farmaco/intervento. Il loro scopo è quello di fornire agli sperimentatori e alle altre persone coinvolte nella sperimentazione le informazioni necessarie per facilitare la comprensione delle motivazioni alla base di molte caratteristiche chiave del protocollo e la loro osservanza. Queste includono la dose, la frequenza/l'intervallo di somministrazione, i metodi di somministrazione e le procedure di monitoraggio della sicurezza. IB informazioni precliniche e cliniche relative a un farmaco sperimentale.

Durante la preparazione degli IB, gli esperti di etichettatura clinica di Freyr presentano le informazioni in forma concisa, semplice, obiettiva ed equilibrata. Le stesse qualità possono essere considerate anche nella traduzione dei documenti. Oltre alla redazione degli IB, Freyr supporta anche la revisione annuale degli IB e lavora alle revisioni necessarie, in conformità con le procedure standard stabilite da clienti e sponsor.
Sviluppo dell'Etichettatura Target (TL)/Profilo Target
Sviluppo e revisione di DCDS e DCSI.
Freyr vanta una comprovata esperienza nella creazione di Developmental Core Data Sheets (DCDS) di alta qualità. Il DCDS è un'etichetta centrale intermedia vitale per ricavare il contenuto per le prime etichette nazionali da presentare (come USPI, SmPC, ecc.). Il DCDS/DCSI è preparato dall'etichetta di riferimento e fornisce sicurezza ed efficacia integrate a un intervento o farmaco. Il DCDS/DCSI aiuta gli investigatori e gli sponsor presentando e aggiornando sezioni DCDS mirate e dedicate che possono essere comodamente inserite nell'IB. Il DCSI facilita lo sviluppo del CCSI, che in seguito costituisce parte integrante del Core Data Sheet (CCDS) dell'azienda.
Sviluppo e revisione del Profilo Prodotto Target (TPP) della FDA e del progetto di SmPC (dSmPC) dell'UE.
Il Target Product Profile (TPP)/bozza del riassunto delle caratteristiche del prodotto (dSmPC) è una forma di etichetta clinica che facilita il dialogo tra le aziende farmaceutiche e le autorità sanitarie. Il TPP viene utilizzato durante l'intero processo di sviluppo del farmaco, dalle fasi precedenti alla richiesta di autorizzazione per un nuovo farmaco sperimentale (IND) e dalla fase di richiesta di autorizzazione per un nuovo farmaco sperimentale (IND) fino ai programmi post-commercializzazione, al fine di perseguire nuove indicazioni o altre modifiche sostanziali nell'etichettatura delle sperimentazioni cliniche. Le aziende farmaceutiche specificano i concetti di etichettatura che costituiscono gli obiettivi del programma di sviluppo del farmaco sotto forma di TPP. TPP fornisce una dichiarazione dell'intento generale del programma di sviluppo del farmaco e fornisce informazioni sul farmaco in una particolare fase di sviluppo. In qualità di partner strategico in materia di regolamentazione, Freyr ha esperienza nella preparazione di TPP per gli US dSmPC per l'UE.
- Risorse con una conoscenza normativa approfondita nel confezionamento e nell'etichettatura clinica
- Competenza nella gestione efficace dell'etichettatura globale e regionale dei farmaci per clienti farmaceutici Fortune negli STATI UNITI D'AMERICA, in Europa, APAC, MENA, ecc.
- Competenza normativa globale nell'aiutare le organizzazioni delle scienze della vita, ovvero produttori farmaceutici, biotecnologici e nutrizionali
- Redattori medici altamente qualificati con ampia esperienza nell'etichettatura normativa
- Una comprensione approfondita e aggiornata delle modifiche apportate alle etichette dei farmaci a livello globale da diverse autorità sanitarie, quali laFDA US , EMA, la TGA, ecc.
- Team di conformità dedicato che monitora lo stato di implementazione delle schede dati centrali e aziendali (CDS/CCDS) nelle etichette regionali
- Competenza nell'etichettatura per studi clinici e nei servizi di etichettatura clinica
- Professionisti dell'etichettatura farmaceutica, biotecnologica e nutrizionale altamente esperti









