Servizi di Conformità IVDR UE: Panoramica
Il Regolamento Europeo sui Dispositivi Medico-Diagnostici in Vitro (EU IVDR) è una nuova base normativa per l'immissione di IVD sul mercato europeo. Il Regolamento EU IVDR è destinato a sostituire l'attuale Direttiva UE sui dispositivi medico-diagnostici in vitro (UE 98/79/CE). In quanto regolamento europeo, sarà efficace in tutti i Member States dell'UE e negli stati dell'Associazione Europea di Libero Scambio (EFTA) senza necessità di essere recepito nella legislazione dei rispettivi Stati. In qualità di partner normativo comprovato, Freyr fornisce servizi di conformità EU IVDR e servizi di consulenza IVDR ai produttori per regolamenti sui dispositivi medico-diagnostici in vitro conformi e marcatura CE.
Il Regolamento IVDR - Tempistiche di Transizione
Con l'obbligo di entrare in vigore dal 26 maggio 2022, il nuovo Regolamento UE IVDR è considerato un cambiamento significativo nella supervisione normativa dei dispositivi medico-diagnostici in vitro (IVD). Di seguito una panoramica della transizione IVDR –
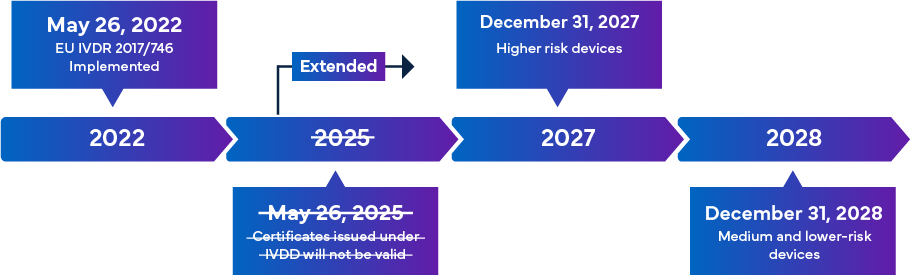
Una volta pienamente implementate, le norme di conformità IVDR garantiscono che quasi tutti gli IVD che entrano nel mercato europeo siano soggetti alla revisione dell'Organismo Notificato (NB) IVDR e alla certificazione di marcatura CE come parte del Processo di Approvazione IVD. In questo scenario, oltre all'allineamento con la classificazione IVDR aggiornata, vi è un requisito immediato per i produttori di esaminare efficacemente la documentazione tecnica chiave per una registrazione IVD e una marcatura CE di successo. I requisiti IVDR variano in base alla classe di rischio dell'IVD. In generale, per la Certificazione IVD, i produttori devono eseguire:
- Revisioni del fascicolo tecnico secondo il regolamento IVDR (Regolamento UE 2017/746)
- Preparazione del Rapporto di Valutazione delle Prestazioni (PER) per tutti i dispositivi IVD
- Follow-up delle prestazioni post-commercializzazione (PMPF) come da Allegato XIII Parte B del Regolamento IVDR
- Segnalazione di vigilanza ai sensi dell'articolo 82 del Regolamento IVDR
Freyr supporta i clienti nell'esecuzione di una revisione sistematica della letteratura scientifica e nell'assistenza alla pianificazione e preparazione di un PER per la conformità al Regolamento sui Dispositivi Medico-Diagnostici in Vitro. Freyr dispone di esperti dedicati che forniscono servizi di consulenza IVDR e supporto per la Post-market Surveillance (PMS), che è parte integrante del sistema di gestione della qualità del produttore, insieme al Follow-up delle Prestazioni Post-commercializzazione (PMPF).
Ottieni consulenza esperta sulla conformità al Regolamento IVDR dell'UE
Servizi di Conformità IVDR UE: Competenza e Vantaggi
- Piano di transizione per la conformità all'IVDR
- Revisione tecnica e analisi delle lacune dei requisiti IVDR per i GSPR (Requisiti Generali di Sicurezza e Prestazione)
- Supporto alla compilazione del fascicolo tecnico secondo i requisiti IVDR.
- Rapporti di validità scientifica basati su letteratura e/o dati interni
- Rapporti sulle prestazioni cliniche basati su letteratura e/o dati interni
- Evidenza clinica o rapporti di valutazione delle prestazioni
- Protocolli e rapporti di follow-up delle prestazioni post-commercializzazione (PMPF)
- Protocolli e rapporti di Post-market Surveillance (PMS)
- Stesura/revisione di altri documenti come il foglietto illustrativo/IFU (Istruzioni per l'uso), le Istruzioni di Riferimento Rapido (QRI), il Manuale Operativo/Utente ecc.

- Conformità IVDR garantita, registrazione IVD e marcatura CE
- Solida comprensione e competenza normativa nelle aree chiave di impatto del Regolamento UE IVDR
- Solido modello di consegna basato sulla gestione dei progetti per garantire il rispetto delle scadenze.
- Esperti NB interni (revisione del rapporto da parte dei revisori interattivi NB)
- Team dedicati con competenze trasversali su aree di impatto specifiche e categorie di dispositivi.
- Contributi interfunzionali da esperti di dispositivi medici per conformarsi ai requisiti
- Ampia gamma di servizi che include conformità, revisione e pianificazione
- Solida competenza nel mantenere la coerenza nelle consegne (Tempi e Qualità)









