Evoluzione dei farmaci generici - Panoramica.
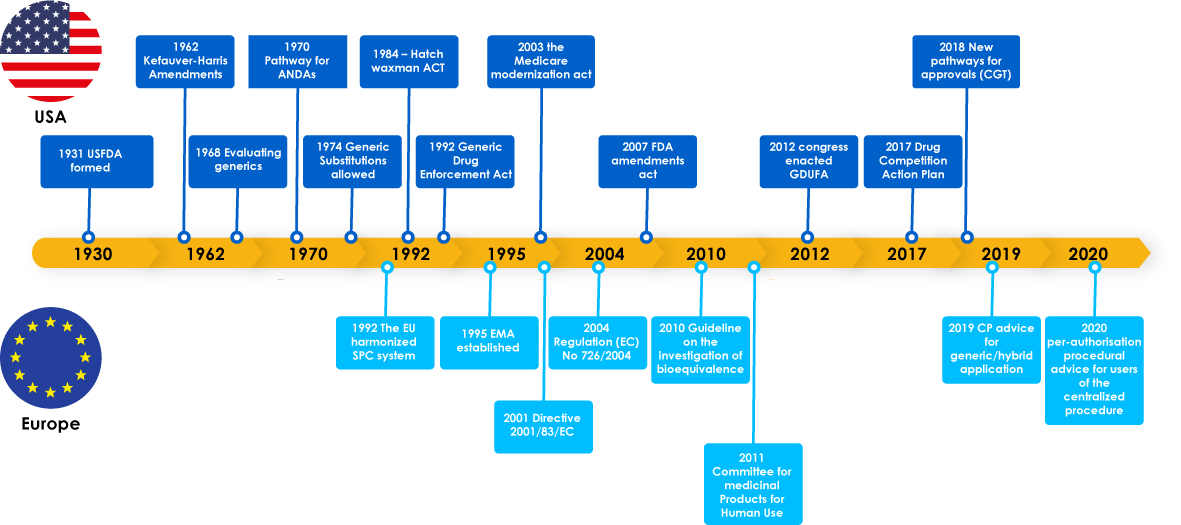
I farmaci generici hanno raggiunto importanti traguardi, tra cui le leggi di regolamentazione a supporto dello sviluppo dei generici, che hanno incoraggiato i produttori a esplorare il mercato dei generici. Queste legislazioni hanno anche dato ai medici la fiducia di prescrivere un sostituto per un farmaco di marca e alla fine hanno beneficiato i pazienti, poiché i produttori di generici hanno soddisfatto le esigenze critiche dei pazienti in tutto il mondo.
Domande frequenti sui farmaci generici
D1: Cosa sono i farmaci generici?
Risposta: I farmaci generici sono farmaci farmaceutici, che sono copie identiche del farmaco originale e hanno lo stesso API, dosaggio, uso previsto, effetti collaterali, via di somministrazione, rischi, sicurezza e potenza del farmaco innovatore, ma possono differire in alcune caratteristiche come il processo di produzione, la formulazione, gli eccipienti, il colore, il gusto e il confezionamento. In altre parole, un farmaco generico è terapeuticamente equivalente a un farmaco di marca e, pertanto, può essere sostituito con il suo equivalente di marca.
D2: Perché i farmaci generici costano meno di un farmaco innovatore?
Risposta: I farmaci generici sono più convenienti rispetto al farmaco innovatore, perché non devono ripetere gli studi preclinici e clinici costosi e lunghi, che sono richiesti per i farmaci innovatori per dimostrare sicurezza ed efficacia e, invece, i farmaci generici devono provare solo l'equivalenza farmaceutica per il loro prodotto.
D3: I farmaci generici sono efficaci quanto il farmaco innovatore?
Risposta: Sì, i farmaci generici hanno la stessa qualità, efficacia e sono sicuri come i farmaci di marca. Il prezzo inferiore di questi farmaci non indica che siano di qualità inferiore, perché i farmaci generici, proprio come i farmaci di marca, devono superare un rigoroso processo di approvazione per commercializzare il loro prodotto e le aziende farmaceutiche sono tenute a presentare la domanda di registrazione del farmaco generico, dimostrando che il loro farmaco ha lo stesso beneficio clinico dei farmaci di marca e sono idonei ad essere usati come sostituti del rispettivo farmaco di marca.
D4: Perché i farmaci generici hanno un aspetto diverso rispetto al prodotto farmaceutico di marca?
Risposta: I farmaci generici devono essere bioequivalenti ai farmaci di marca e avere lo stesso API dei farmaci innovatori. Tuttavia, possono esserci piccole differenze nei farmaci generici per quanto riguarda forma, etichettatura (differenze minori), confezionamento e ingredienti inattivi come colore, aromi e conservanti; ma l'efficacia del farmaco deve rimanere la stessa.
D5: Cosa comporta la revisione e l'approvazione delle domande di farmaci generici negli US?
Risposta: Qualsiasi azienda farmaceutica che debba commercializzare il proprio farmaco generico negli US deve rispettare tutti i requisiti normativi della FDA US per la registrazione dei farmaci generici e deve dimostrare che:
- Il farmaco generico è “farmaceuticamente/terapeuticamente equivalente” al farmaco di marca
- Il fabbricante è in grado di produrre il farmaco in modo corretto e costante.
- Il «principio attivo» è lo stesso di quello del marchio
- La giusta quantità del principio attivo raggiunge il punto nel corpo dove ha effetto.
- Gli ingredienti "inattivi" del farmaco sono sicuri.
- Il farmaco non si degrada nel tempo
- Il contenitore in cui il farmaco sarà spedito e venduto è appropriato
- L'etichetta è la stessa dell'etichetta del farmaco di marca
- Brevetti pertinenti o esclusive legali sono scaduti
D6: Ogni farmaco di marca ha un farmaco generico?
Risposta: No. Non tutti i farmaci di marca hanno una versione generica. I nuovi farmaci sono prodotti sotto protezione brevettuale per un massimo di venti anni. Ciò significa che nessun altro farmaco può essere prodotto e commercializzato durante questo periodo, fino alla scadenza del brevetto. Tuttavia, alcuni farmaci potrebbero non avere mai versioni generiche per il loro prodotto, a causa di difficoltà nella produzione o nel caso in cui il farmaco generico possa essere considerato non redditizio.








