Il mercato nordamericano dei dispositivi medici è uno dei più interessanti e altamente regolamentati al mondo. Negli Stati Uniti, la registrazione dei dispositivi medici è supervisionata dalla FDA, principalmente attraverso il Center for Devices and Radiological Health (CDRH), mentre in Canada è disciplinata da Health Canada nell'ambito di un quadro normativo basato sul rischio.
Per produttori, orientarsi in questi mercati può risultare complesso. Entrambi i paesi si basano su una classificazione dei dispositivi medici basata sul rischio (Classe I, II, III e, in Canada, Classe IV), supportata da solide prove di sicurezza e prestazioni e da un sistema di gestione della qualità (SGQ) conforme. Programmi come MDSAP standard come ISO 13485, insieme alle differenze di terminologia, percorsi e requisiti di documentazione, aggiungono ulteriori livelli di complessità quando si pianifica l'ingresso nei mercati US canadese.
Freyr aiuta produttori questa complessità in un piano chiaro e concreto per l'accesso al mercato US canadese. Conosciamo bene le interazioni tra FDA e le normative di Health Canada in materia di dispositivi medici, e vi aiutiamo ad allineare classificazioni, documentazione di supporto, sistemi di gestione della qualità e dossier, in modo che possiate seguire un'unica strategia efficiente per le approvazioni, i lanci e la conformità a lungo termine in entrambi i paesi.
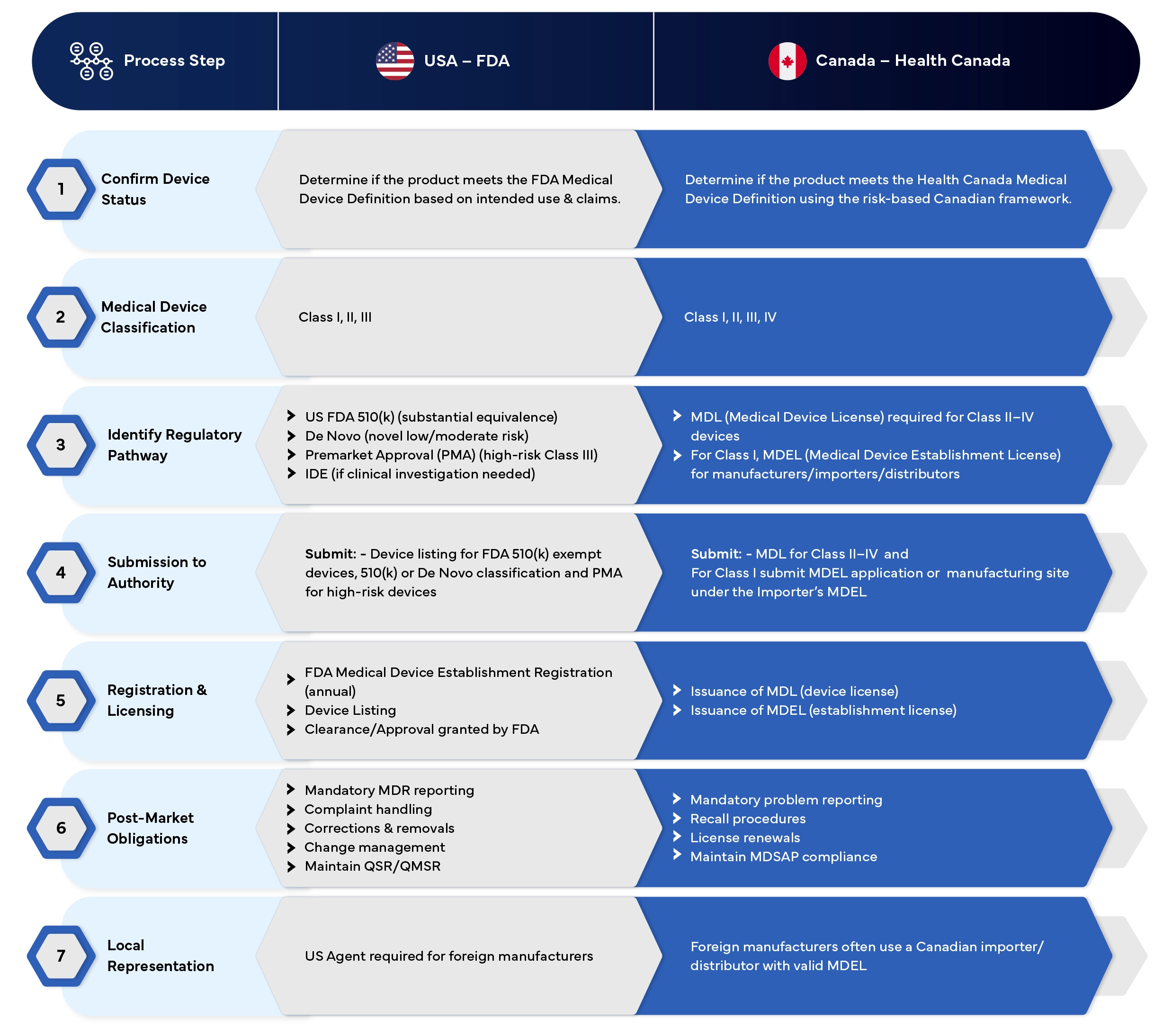
Stati Uniti contro Canada
Procedura di registrazione dei dispositivi medici - Tabella comparativa
Servizi di Registrazione di Dispositivi Medici di Freyr
Registrazione dei Dispositivi Medici nelle Americhe
- Supporto di intelligence normativa e di mercato
- Classificazione dei Prodotti secondo i requisiti normativi
- Registrazione dei Dispositivi Medici negli US - 513 (G) e (Percorso Corretto tra 510 (K)/De-NOVO/PMA/IDE)
- Riunione di pre-presentazione con le Agenzie Sanitarie
- Supporto normativo per i documenti di prodotto, come il Design History File (DHF).
- Analisi delle Lacune dei Documenti Tecnici e dei Sistemi di Buone Pratiche di Fabbricazione (GMP)
- Supporto normativo per la compilazione del Fascicolo Tecnico come richiesto dal rispettivo percorso di registrazione
- Strategia di conformità del sistema qualità USFDA (21 CFR 820)
- Servizi di conformità al Programma di Audit Unico per Dispositivi Medici (MDSAP)
- Registrazione dei dispositivi medici in Canada - Licenza per dispositivi medici (MDL) e Registrazione della licenza di stabilimento per dispositivi medici (MDEL)
- Interazione e supporto con l'Agenzia Sanitaria
- Rappresentanza locale – Servizi di Agente US e Persona Responsabile Sanitaria
- Attività di conformità post-approvazione.

- Presentazioni riuscite per una classe variegata di dispositivi, che vanno dal software alle suture
- Accesso dell'affiliata locale per affrontare le sfide dell'autorità e i requisiti linguistici specifici
- Personale dedicato ed esperto per fornire supporto normativo per dispositivi medici e IVD
- Modello conveniente per il supporto alla rappresentanza in loco o legale
- Aver completato con successo diversi progetti negli US e in Canada
- Con sede negli US.

Perché collaborare con Freyr?
- Competenza normativa End-to-end America, che copre ogni aspetto, dalle notifiche pre-commercializzazione (presentazione delle domande) FDA a Health Canada fino alla sorveglianza post-commercializzazione e alla conformità durante l'intero ciclo di vita del prodotto.
- Un successo comprovato con oltre 1500 registrazioni di dispositivi medici in tutto il mondo, che spaziano dai dispositivi di Classe I-III negli Stati US quelli di Classe I-IV in Canada.
- Presenza sul territorio grazie ai servizi US e al supporto normativo in Canada, con il supporto di team di esperti distribuiti a livello globale per garantire un'esecuzione senza intoppi.
- Una strategia integrata US il Canada che semplifica i requisiti in materia di prove, documentazione e qualità, al fine di ridurre i costi, le duplicazioni e i tempi di approvazione.
- Collaborazione diretta con FDA Health Canada, garantendo una comunicazione chiara, risposte tempestive e un allineamento proattivo alle aspettative normative.
- Scelta da oltre 470 produttori di dispositivi medici produttori , dalle start-up alle multinazionali, come partner di fiducia a lungo termine per la regolamentazione in Nord America.












