Panoramica sull'eSTAR della FDA
L'iniziativa FDA è stata concepita per migliorare l'efficienza e l'uniformità nella preparazione e nella valutazione delle domande FDA (k), De Novo e PMA FDA . Partendo dall'approccio iniziale eSubmitter, che prevedeva la presentazione elettronica delle domande relative a dispositivi medici e dispositivi diagnostici in vitro (IVD), è stato istituito il programma eSTAR, attingendo all'esperienza pregressa FDA. La FDA un programma diverso chiamato Programma pilota Electronic Submission Template and Resource (eSTAR). Le richieste 510(k) devono essere presentate tramite eSTAR a partire dal 1° ottobre 2023; le richieste De Novo (salvo esenzioni) devono essere presentate tramite eSTAR a partire dal 1° ottobre 2025. I modelli sono disponibili online, anche se per il processo di presentazione vero e proprio è necessario utilizzare le credenziali FDA .
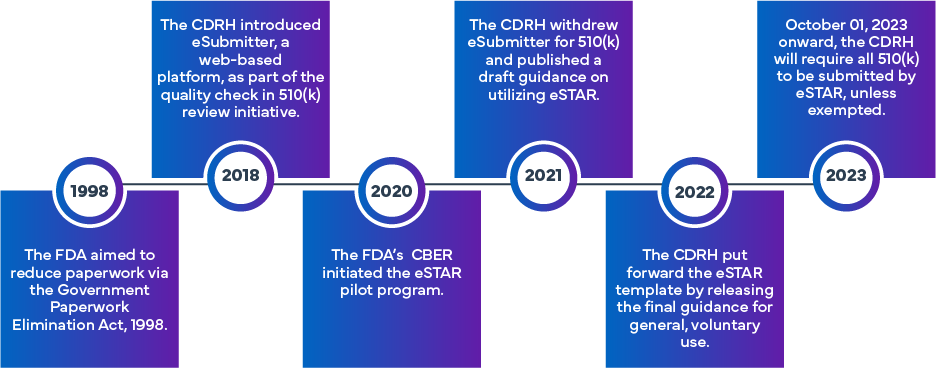
Cos'è l'FDA eSTAR?
eSTAR è un modello PDF interattivo progettato per facilitare la preparazione di una domanda completa di immissione in commercio di dispositivi medici da presentare alla FDA Inoltre, i richiedenti possono utilizzare eSTAR per inviare le risposte alle richieste di informazioni aggiuntive FDA. Il suo obiettivo è migliorare la qualità delle domande relative a vari dispositivi medici, garantendo che i richiedenti forniscano dati completi e di alta qualità per la valutazione pre-commercializzazione FDA.
Adottando il formato eSTAR, i richiedenti possono essere certi della completezza delle loro richieste; ciò consentirà a sua volta alla FDA condurre le valutazioni pre-commercializzazione in modo più efficiente e FDA garantire un accesso tempestivo a dispositivi medici sicuri ed efficaci. Il modello eSTAR è disponibile gratuitamente e può essere utilizzato da tutti i richiedenti di dispositivi medici per le richieste 510(k), De Novo e, su base volontaria, per le richieste Q e le richieste di integrazione della Notifica PMA a 30 giorni presentate alla FDA. Esistono due tipi di modelli eSTAR: uno per i dispositivi medici e l'altro per i dispositivi diagnostici in vitro (IVD). PreSTAR beta si è evoluto; utilizzare i modelli di presentazione Q più recenti tramite il Portale di collaborazione con i clienti (CCP) del CDRH. Il modello eSTAR 6.0 per De Novo/510(k) non IVD è stato rilasciato nell'ottobre 2025.
Caratteristiche e limitazioni delle presentazioni eSTAR
Sebbene il programma eSTAR offra un modulo PDF interattivo progettato per aiutare i richiedenti a preparare presentazioni complete di dispositivi medici e IVD, esso presenta sia vantaggi che svantaggi. I richiedenti devono comprendere questi benefici e limitazioni, in base ai quali possono fare scelte informate sull'integrazione di eSTAR nel loro processo di presentazione. Nella tabella seguente, esploreremo gli attributi e le restrizioni del programma eSTAR.

Aspetti da considerare per un uso efficace di eSTAR
Una caratteristica vantaggiosa del modello eSTAR, che contribuisce all'ottimizzazione del processo di presentazione, è la sua incorporazione automatizzata di normative pertinenti e standard riconosciuti per la citazione. Ciò non solo accelera il processo di presentazione riducendo l'inserimento manuale dei dati, ma mitiga anche la possibilità di errori umani che potrebbero verificarsi durante l'inserimento di normative e standard. Attraverso una costruzione guidata per ogni sezione di presentazione, l'utilizzo di eSTAR nel processo di presentazione può essere facilmente ottimizzato.
- La FDA suggerisce Adobe Acrobat Pro o Foxit PDF Editor per la modifica dei modelli eSTAR.
- eSTAR include alcuni moduli integrati, eliminando così la necessità di una compilazione separata. Questi includono il Modulo 3514 (il foglio di copertina della presentazione) e il Modulo 3881 (indicazioni d'uso). Inoltre, la dichiarazione veritiera e accurata, che in precedenza era richiesta su carta intestata di un'azienda, è ora integrata all'interno di eSTAR.
- eSTAR supporta vari formati di allegati oltre ai semplici PDF, come fogli di calcolo Excel e file video (mp4).
- I file in formati abilitati alle macro ed eseguibili non sono consentiti.
- La dimensione totale del file PDF eSTAR, insieme ai suoi allegati, non deve superare 1GB, poiché i file di dimensioni superiori a 4GB non saranno accettati.
- Se i vostri file elettronici superano i limiti tecnici, potete inviare la presentazione digitale al CDRH Document Control Center (DCC) via posta.
Buone pratiche per la preparazione delle sottomissioni eSTAR
Seguire alcune delle migliori pratiche per la preparazione delle presentazioni eSTAR può aiutare i richiedenti a semplificare il processo di presentazione e migliorare le loro possibilità di un esito positivo. Ecco alcune delle migliori pratiche:
- Attenersi alle FDA :la FDA delle linee guida per aiutare i richiedenti a utilizzare correttamente il modello eSTAR. Seguire queste linee guida garantisce che le richieste presentate siano conformi ai requisiti e alle aspettative FDA.
- Assicurarsi che il modulo sia compilato in ogni sua parte:il modello eSTAR guida i richiedenti attraverso le informazioni essenziali da fornire. I richiedenti devono fornire tutti i dati richiesti per ridurre al minimo il rischio di lacune o richieste di informazioni aggiuntive.
- Garantire la coerenza:il modello eSTAR favorisce l'uniformità dei contenuti e della struttura delle domande 510(k). La struttura guidata per ciascuna sezione della domanda aiuta a ricavare le informazioni relative al dispositivo medico.
- Dare priorità alla chiarezza:fornire informazioni chiare e concise nelle richieste inviate tramite eSTAR per facilitare un processo di revisione snello. Tale livello di dettaglio e precisione riduce al minimo ritardi ed errori, garantendo inoltre un accesso tempestivo alle richieste di autorizzazione all'immissione in commercio dei dispositivi medici.
- Precisione garantita:la verifica automatica delle informazioni contenute in ogni sezione delle richieste inviate tramite eSTAR contribuisce a ridurre i ritardi nella revisione e le potenziali carenze.
Importanza della codifica a colori nella presentazione eSTAR della FDA
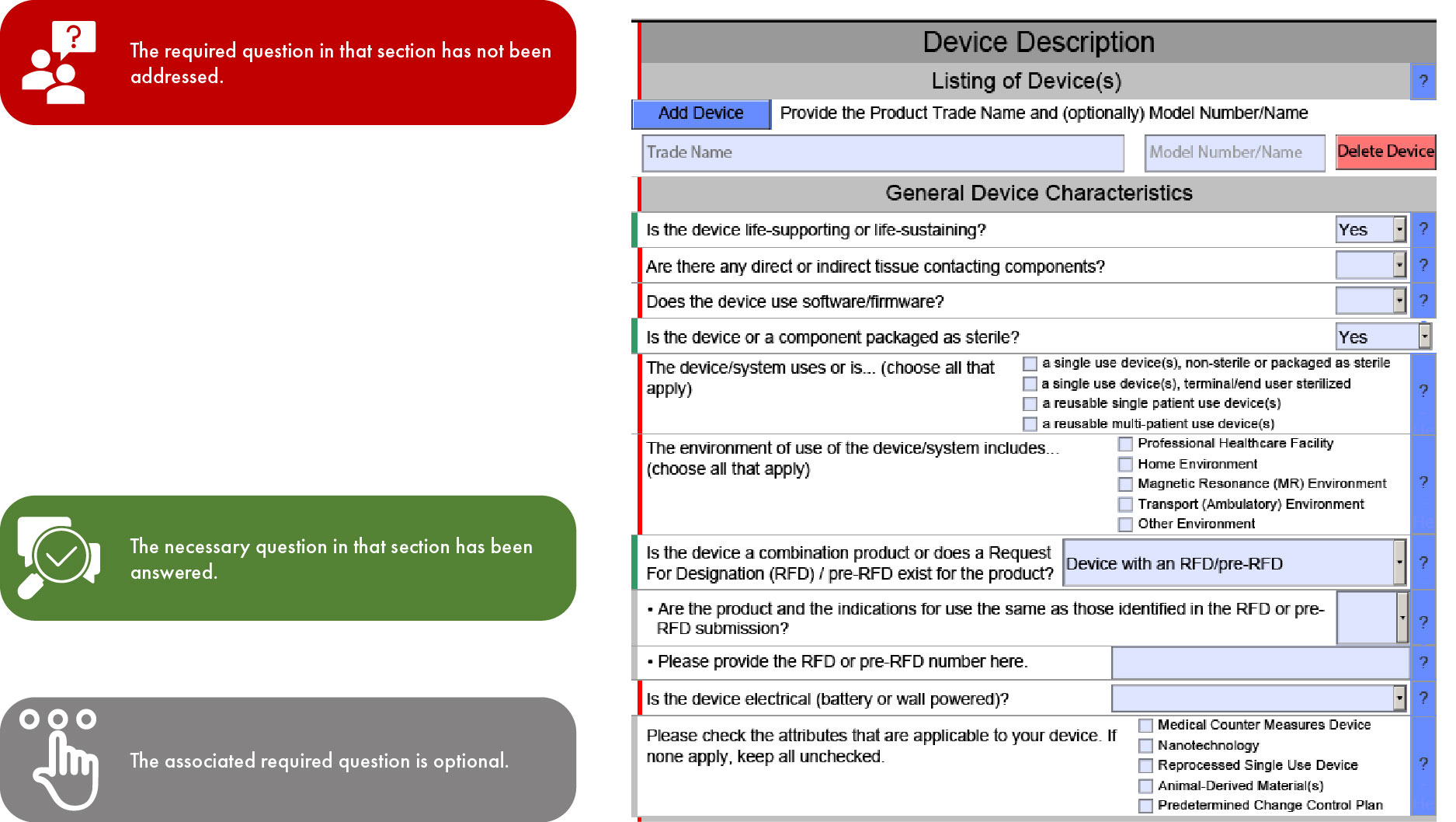
L'uso di eSTAR sarà obbligatorio per le domande 510(k) a partire dal 1° ottobre 2023 e per le domande De Novo a partire dal 1° ottobre 2025; l'ordine di compilazione delle sezioni del modello dipende dal tipo di domanda. Questo tipo di semplificazione facilita una revisione più rapida da parte dellaFDA US , riducendo così al minimo le incongruenze e le omissioni nella vostra domanda. Tuttavia, è importante notare che la FDA ritardare la revisione se mancano le traduzioni in inglese della documentazione fornita.

Allinea i tuoi allegati
Esaminate in anticipo il modello eSTAR per capire come sono suddivisi gli allegati e assicuratevi che i vostri documenti siano allineati con le sezioni degli allegati. Questo passaggio è cruciale, in particolare per le aziende con precedenti presentazioni 510(k), poiché il vostro approccio esistente all'organizzazione dei documenti potrebbe richiedere degli aggiustamenti. Potrebbe anche comportare l'estrazione di contenuti dagli allegati.
- eSTAR richiede allegati concisi, che differiscono dalle presentazioni tradizionali.
- Prevedere numerosi allegati, potenzialmente decine.
- Gli allegati consentono l'inclusione di dati come fogli di calcolo Excel, file video MP4, documenti Word, file JPEG, ecc.
- eSTAR richiede i numeri di pagina per le informazioni sugli allegati, ma non suggerisce l'uso di una checklist di rifiuto all'accettazione per le linee guida FDA.
Modelli: sono disponibili i modelli della versione 6.0 più recente ; per gli invii in corso è accettabile la versione 5: fda.
Il Futuro di eSTAR
Si prevede che eSTAR subirà aggiornamenti una volta finalizzati i documenti di orientamento applicabili completi. Con questi aggiornamenti, il produttore potrà fare riferimento alle versioni più recenti emesse dalla US FDA.
Health Canada (HC) ha introdotto un'iniziativa pilota per l'utilizzo di eSTAR per i dispositivi di Classe III e IV. Esiste la congettura che altre nazioni possano emulare l'esempio del Canada nel rendere discrezionale l'adozione di eSTAR, in particolare all'interno del consorzio IMDRF. Tuttavia, va notato che non ci sono state dichiarazioni esplicite in tal senso.
Perché scegliere Freyr?
Freyr vanta una vasta esperienza acquisita grazie al suo coinvolgimento in numerosi progetti passati incentrati sulle sottomissioni alla FDA. Offrendo due percorsi per assistere proattivamente l'industria nell'accelerare le sottomissioni 510(k) e De Novo, Freyr fornisce una serie di servizi ai clienti, che includono un elenco completo di documenti di sottomissione essenziali e informazioni richieste, la conduzione di analisi delle lacune meticolose sulla documentazione, la compilazione delle sottomissioni tramite eSTAR e la finalizzazione del pacchetto di sottomissione pre-commercializzazione alla FDA. Inoltre, Freyr estende il suo supporto alle attività post-sottomissione, come la fornitura di informazioni aggiuntive e la revisione delle risposte del settore a qualsiasi richiesta di informazioni supplementari avanzata dalla FDA.
Come può aiutare Freyr?
Freyr offre supporto che può essere utile per prepararsi alle sottomissioni 510(k) e De Novo. I servizi includono:
- Supporto al Percorso Normativo: Ciò comporta l'identificazione del codice del prodotto, del nome e numero della regolamentazione, dei potenziali dispositivi precedenti/di riferimento, dei test di performance, nonché degli standard applicabili e dei documenti guida pertinenti al dispositivo specifico in questione.
- Supporto per Q-submission (Pre-presentazioni): Ciò comporta l'assistenza nel chiarire le domande relative ai prerequisiti di una presentazione pre-commercializzazione, organizzare la presentazione, prepararsi per una riunione con la FDA, interagire con la FDA durante la riunione in modo interattivo e redigere i verbali della riunione.
L'esperienza nel programma eSTAR della FDA
- Strategia normativa FDA completa.
- Identificazione del dispositivo di riferimento.
- Stabilire l'equivalenza sostanziale con il dispositivo di riferimento.
- Analisi delle Lacune per la conformità FDA.
- Compilazione di ventuno sezioni del fascicolo tecnico 510(k).
- Pubblicazione e creazione dell' eCopy.
- Convalida e presentazione dell'eCopy.
- Servizi di collegamento per l'approvazione dei dispositivi.
- La risoluzione della risposta RTA e delle carenze.
- Servizi di consulenza per affrontare le carenze.
- Manutenzione dell'elenco dei dispositivi e del database FURLS.